Las Enzimas
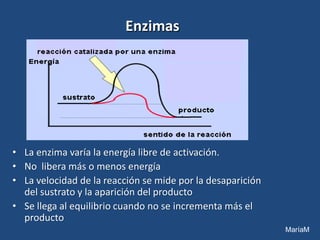
- 1. Enzimas • La enzima varía la energía libre de activación. • No libera más o menos energía • La velocidad de la reacción se mide por la desaparición del sustrato y la aparición del producto • Se llega al equilibrio cuando no se incrementa más el producto MaríaM
- 2. Enzimas Maud Menten y Leonor Michelis (1882) Introducen “el concepto enzima sustrato” Explican el comportamiento cinético de las enzimas MaríaM
- 3. S + E ES E + P MaríaM Enzimas Función de la enzima en la reacción química enzima enzima enzima Sustrato + Enzima Complejo Enzima-Sustrato Producto + Enzima Las enzimas son específicas, hay miles de enzimas Actúan sobre el sustrato específico Las enzimas se recuperan indefinidamente Arriaga, Esteban. Bioquímica
- 4. Centro activo de las enzimas • Las enzimas contienen hendiduras o cavidades denominadas sitio activo. • Formado por las cadenas laterales de residuos específicos de aminoácidos, con un arreglo tridimensional particular, afín con la estructura del sustrato. MaríaM http://laguna.fmedic.unam.mx/ Enzima Sitio Activo Sustrato Complejo ES
- 5. MaríaM Enzimas Concentración sustrato Velocidad de la reacción enzimática
- 6. Velocidad de reacciones MaríaM Se llega al equilibrio cuando no se incrementa más el producto En condiciones de Tº [temperatura óptima]
- 7. Velocidad de reacciones MaríaM 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Velocidad de reacción Se llega al equilibrio cuando no se incrementa más el producto En condiciones de pH óptimo
- 8. Regulación actividad enzimática • Modificando el sitio activo • A través del sitio alostérico se regula positiva (estimula) o negativamente (inhibe) • Inhibidores enzimáticos. Interactúan disminuyendo el efecto de la enzima sobre el sustrato • Inhibidor competitivo: ocupa el lugar en el sitio activo de sustrato • Inhibidor no competitivo: altera la conformación del sitio activo • Ejemplos: en caso de “hipercolesterolemia” un inhibidor (medicina), disminuye la síntesis de colesterol MaríaM Arriaga, Esteban. Bioquímica
- 9. Modificadores alostéricos MaríaM Enzimas Activador alostérico (+) Inhibidor alostérico (-)
- 10. Inhibidores Inhibidor competitivo Inhibidor no competitivos MaríaM Enzimas INHIBIDOR COMPETITIVO INHIBIDOR NO COMPETITIVO
- 11. Cofactores y coenzimas • Las enzimas pueden ser: • Simples: formadas por solo aminoácidos • Complejas, holoenzima, denominándose apoenzimas, algunas unidas fuertemente a las enzimas: • Contribuyen a la eficacia de la reacción enzimática • Cofactores • Coenzimas: sustancias derivadas de las vitaminas. MaríaM Arriaga, Esteban. Bioquímica
- 12. MaríaM Enzimas Cofactor Fe++ Mg++ Mn++ Cu++ Zn++ Coenzima Vitamina B1 Riboflabina, Vitamina B2 Ac. pantoténico. Vitamina B3 Niacina Vitamina B5 Biotina Vitamina B6 Ácido fólico Cobalamina, Vitamina B12 Las reacciones metabólicas requiere además de la enzima componentes inorgánicos (cofactores) y orgánicos: (coenzimas)
- 13. Clases de Enzimas: Oxidorreductasas MaríaM Catalizan reacciones de Oxidorreducción. Se acepten o cedan los electrones [protones] Redox NADH NAD+ FADH FAD+
- 14. Clases de Enzimas: Transferasas MaríaM Transfieren grupos a otras sustancias. Transferencia de grupos ejemplo en monosacáridos, aminoácidos. Transaminasas QuinasasGli 3P gliceraldehido 3 -P H – C = O H – C – OH CH2O – P 2 fosfogliceraldehido COO - H – C – O – P CH2OH
- 15. Clases de Enzimas: Hidrolasas MaríaM Catalizan reacciones de hidrólisis Digestión de macromoléculas: proteínas, lípidos, carbohidratos en presencia de moléculas de agua. Hidrolizan enlaces: Pépticos [proteínas]. Pepsina Ester [lípidos]. Lipasas. Esterasas Glucosídicos [carbohidratos]. Glucosidasas
- 16. Clases de Enzimas: Isomerasas MaríaM Transfieren cambiando de posición un grupo en una molécula, convirtiéndola en isómero Ejemplo Mutasas. Glucosa 6 P Fructosa 6 P Isomerasa CH20P 0H 0H 0H 0H CH20P CH20H 0H 0H 0H
- 17. Clases de Enzimas: Isomerasas MaríaM Transfieren cambiando de posición un grupo en una molécula, convirtiéndola en isómero Ejemplo Mutasas. Glucosa 6 P Fructosa 6 P Isomerasa CH20P 0H 0H 0H 0H CH20P CH20H 0H 0H 0H
- 18. Clases de Enzimas: Liasas MaríaM Catalizan reacciones en las que se eliminan dobles enlaces, adicionándose grupos: PIRUVATO NAD+ NADH+H+ Lactato deshidrogenasa COO - C = O CH3 COO - OH – C – H CH3
- 19. Clases de Enzimas: ligasas MaríaM Unión de dos moléculas, atrapando energía . Al degradarse ATP en ADP se libera energía Glucosa Glucosa 6 P P ATP ADP Glucoquinasa Mg++ CH20H 0H 0H 0H
