CVPAP y CVPAT: consideraciones anestésicas en pacientes con conexión venosa pulmonar anómala
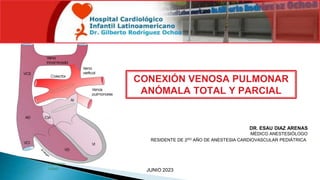
- 1. CONEXIÓN VENOSA PULMONAR ANÓMALA TOTAL Y PARCIAL JUNIO 2023 DR. ESAU DIAZ ARENAS MÉDICO ANESTESIÓLOGO RESIDENTE DE 2DO AÑO DE ANESTESIA CARDIOVASCULAR PEDIÁTRICA.
- 2. CONEXIÓN VENOSA PULMONAR ANÓMALA TOTAL Y PARCIAL Conexión Venosa Pulmonar Anómala Total (CVPAT) Conexión Venosa Pulmonar Anómala Parcial (CVPAP) Andropoulos D. Anesthesia for Congenital Heart Disease. Tercera edicion. Editorial Wiley,. Hoboken, New Jersey EEUU: 2015: p-474-475. Edwards 1953 1ra clasificación: Brody 1942
- 3. Se encuentra entre el 1% y 2% del total de las cardiopatías Incidencia en el primer año de vida del 2 % Más frecuente en el sexo masculino en una relación 2:1 Se asocia a pocos síndromes genéticos Flores M. Cardiopatías congénitas en niños. Capitulo XV. P-1272-1280. Epidemiología
- 4. Clasificación anatómica propuesta por Darling Supracardíaco (50%) Intracardíaco (35%) Infracardíaco (15%) Mixto (7%) Flores M. Cardiopatías congénitas en niños. Capitulo XV. P-1272-1280.
- 5. Clasificación clínico, fisiopatológico y hemodinámica Flores M. Cardiopatías congénitas en niños. Capitulo XV. P-1272-1280. Obstructiva CVPAT No Obstructiva Compresión extrínseca del vaso colector. Disminución del calibre del vaso colector Obstrucción intracardíaca a nivel del tabique interauricular
- 6. Fisiopatología Flores M. Cardiopatías congénitas en niños. Capitulo XV. P-1272-1280. Cardiopatía con mescla completa SpO2 = relación entre Qp:Qs GC sistémico = CIA?
- 7. Fisiopatología CVPAT NO OBSTRUCTIVA Flores M. Cardiopatías congénitas en niños. Capitulo XV. P-1272-1280. CVPAT supracardiaca Vida Fetal? Al nacer e iniciarse el FSP Gran flujo cavidades derechas Con dilatación e hipertrofia progresiva FO o CIA = cortocircuito D-I Tamaño del VI depende de CIA Hipodesarrollo de cavidades izquierdas
- 8. Fisiopatología CVPAT OBSTRUCTIVA Flores M. Cardiopatías congénitas en niños. Capitulo XV. P-1272-1280. CVPAT infracardiaca Puede existir a cualquier nivel No existe sobrecarga de volumen Sobrecarga de presión por aumento en los pulmones Aumento de presión venocapilar pulmonar Edema pulmonar Impide la oxigenación = cianosis Con aumento de las RVP
- 9. Cuadro clínico Varía si la CVPAT es obstructiva o no obstructiva. CVPAT no obstructiva Andropoulos D. Anesthesia for Congenital Heart Disease. Tercera edicion. Editorial Wiley,. Hoboken, New Jersey EEUU: 2015: p-474-475. Se presentan en el 2do y 3cer mes de vida Poca ganancia de peso polipnea Sx de dificultad respiratoria importante Cianosis moderada Insuficiencia cardiaca Abombamiento paraesternal izquierdo trastornos acido-base. IRB ?
- 10. Cuadro clínico Varía si la CVPAT es obstructiva o no obstructiva. CVPAT obstructiva Andropoulos D. Anesthesia for Congenital Heart Disease. Tercera edicion. Editorial Wiley,. Hoboken, New Jersey EEUU: 2015: p-474-475. Se presentan en la 1ra semana de vida Paciente críticamente enfermo Sx de dificultad respiratoria marcado Polipnea , Cianosis moderada Insuficiencia cardiaca Importante taquicardia trastornos acido-base severos Agregados pulmonares (edema pulmonar) Hígado congestivo y aumentado de tamaño
- 11. Consideraciones anestésicas en la CVPAT Andropoulos D. Anesthesia for Congenital Heart Disease. Tercera edicion. Editorial Wiley,. Hoboken, New Jersey EEUU: 2015: p-474-475. CVPAT obstruida (Previo a la derivación) Maximizar la PO2 con soporte ventilatorio PEEP (significativa) Presión Inspiratorias altas FiO2 altas Evitar la Acidosis metabólica Mantenimiento de la estabilidad hemodinámica (Inotrópicos) NO: previo a la derivacion = containdicado = hipoxemia ETE = contaidicado (incluso en los no obstruidos) Útil monitorizar: PAP, PAI, PVC
- 12. Consideraciones anestésicas en la CVPAT Andropoulos D. Anesthesia for Congenital Heart Disease. Tercera edicion. Editorial Wiley,. Hoboken, New Jersey EEUU: 2015: p-474-475. CVPAT obstruida (posterior a la derivación) NO = CVPAT obstruido = uso empírico NO = CVPAT sin obstruccón = estar disponible HAP perioperatoria ocurre hasta en un 50% de los pacientes Evitar las crisis de HAP: FiO2 100% Hiperventilación Alcalinización sistémica Profundidad anestésica (relajación muscular) Oxido naítrico Tambien se ha empleado: sildenafilo, sulfato de Mg, y PGE1
- 13. Consideraciones anestésicas en la CVPAT Andropoulos D. Anesthesia for Congenital Heart Disease. Tercera edicion. Editorial Wiley,. Hoboken, New Jersey EEUU: 2015: p-474-475. CVPAT obstruida (posterior a la derivación) Función pulmonar comprometida por doble lesión pulmonar: Edema pulmonar preoperatorio (obstrucción venosa pulmonar) Respuesta inflamatoria sistemica a la CEC Disminución distensibilidad pulmonar Gradiente arterial- alveolar Ventilación en modalidad presión control Uso de PEEP
- 14. Consideraciones anestésicas en la CVPAT Andropoulos D. Anesthesia for Congenital Heart Disease. Tercera edicion. Editorial Wiley,. Hoboken, New Jersey EEUU: 2015: p-474-475. CVPAT obstruida (posterior a la derivación) Presiones de llenado de AI pueden estar elevadas (tamaño pequeño y baja distensibilidad de AI y VI) Durante destete de CEC: PA bajas evita la distención excesiva La PAP con frecuencia son iguales o mayores que las sistémicas Manejo cuidadoso de los líquidos (curva de Frank-Starling?) Optimización de la FC y ritmo Apoyo inotrópico mejora GC (milrinone) Arritmias perioperatorias: taquicardias supraventriculares (20%)
Notas del editor
- CONEXIÓN VENOSA ANÓMALA PULMONAR TOTAL Y PARCIAL Cardiopatía en la cual las venas pulmonares no drenan a la aurícula izquierda como ocurre normalmente, sino que drenan a la aurícula derecha, ya sea directamente o a través de una vena sistémica o sistema venoso que va a desembocar a la aurícula derecha.
- Término propuesto por Edwards en 1953 y aceptado actualmente. Si todas las venas pulmonares drenan en una forma anormal, se hablará de conexión venosa pulmonar anómala total (CVPAT); pero, si solo es una o varias venas pulmonares, se hablará de conexión venosa pulmonar anómala parcial (CVPAP), siendo esta la primera clasificación que fue propuesta por Brody en 1942.
- Según diferentes publicaciones, dicha conexión es una patología que se encuentra entre el 1% y 2% del total de las cardiopatías; pero, si se toma la incidencia en el primer año de vida, esta se reporta en el 2% de las cardiopatías y, en lo relacionado al drenaje anómalo infradiafragmático, es más frecuente en el sexo masculino en una relación 2:1 (hombres: mujeres). Se asocia a pocos síndromes genéticos, dentro de los que se puede mencionar el síndrome de “ojo de gato” (coloboma del iris y atresia anal). En el 30% de los casos se asocia con vicios de rotación (asplenia y poliesplenia).
- Clasificación Aunque se han propuesto varias clasificaciones para la CVPAT —entre ellas, la muy importante anatomoembriológica de Neil20—, seguimos la propuesta por Darling, de bastante aceptación, quien clasifica anatómicamente esta patología según el sitio en el que se conectan las venas pulmonares. Cabe aclarar que estas dos clasificaciones son prácticamente complementarias. Así pues, Darling divide los drenajes venosos anómalos en los siguientes grupos: a) Supracardíaco: es la variedad de conexión venosa anómala más frecuente (alrededor del 50% de todos los casos) y ocurre cuando las venas pulmonares drenan o se conectan a la vena cava superior derecha (VCSD), a la vena cava superior izquierda (VCSI) y a la vena innominada, siendo esta última el sitio más frecuente: 3-4 veces más frecuente que a la vena cava superior o a alguna de sus tributarias. b) Intracardíaco: cuando las venas pulmonares drenan o se conectan directamente a la aurícula derecha o al seno coronario. En cuanto a frecuencia, es el grupo intermedio, al presentarse en cerca del 35% de los casos. c) Infracardíaco: es el tipo de drenaje venoso pulmonar anómalo menos frecuente (alrededor del 15% de los casos) y ocurre cuando el drenaje o conexión venosa pulmonar va a desembocar a la vena cava inferior o a alguna de sus tributarias; más frecuentemente a la vena porta . d) Mixto: ocurre cuando las venas pulmonares drenan o se conectan a más de uno de los sitios mencionados. Esto sucede en cerca del 7% del total de los casos.
- Desde el punto de vista clínico, fisiopatológico y hemodinámico, la CVPAT puede ser obstructiva o no obstructiva, según exista o no obstrucción en el drenaje, como su nombre lo indica. Puede existir obstrucción al drenaje venoso pulmonar: a) Por compresión extrínseca del vaso colector. b) Por disminución del calibre del vaso colector. Estos dos primeros mecanismos son prácticamente constantes en los casos con conexión anómala infradiafragmática, pero puede ocurrir también ocasionalmente en la supradiafragmática. c) Por obstrucción intracardíaca a nivel del tabique interauricular, ya sea por la presencia de un foramen oval permeable pequeño o de una comunicación interauricular (CIA) restrictiva y, excepcionalmente, por obstrucción en la desembocadura del seno coronario.
- Fisiopatología Es una cardiopatía con mezcla completa, cuya saturación de oxígeno depende de la relación del flujo pulmonar: flujo sistémico(QP:QS). El gasto cardíaco sistémico depende del tamaño de la comunicación interauricular.
- En la CVPAT no obstructiva, como ocurre generalmente en la CVPAT supracardíaca, no hay alteración de la fisiología en la vida fetal, pero, al nacer el niño e iniciarse el flujo a través de los pulmones y dependiendo de la velocidad con que bajen las resistencias pulmonares, llegará un gran flujo a las cavidades derechas, las cuales se dilatan y se hipertrofian progresivamente. Esto indica que en esta patología existe un gran cortocircuito de izquierda a derecha en el sitio del drenaje del colector y, a partir de este sitio, habrá un aumento de la saturación sanguínea, dado que ésta es sangre oxigenada. También habrá un cortocircuito de derecha a izquierda a nivel auricular, por aumento de la presión en la aurícula derecha en relación con la izquierda. Dependiendo del tamaño del foramen oval o de la comunicación interauricular, va a haber una mayor o menor cantidad de la mezcla sanguínea que pasa a las cavidades izquierdas y a la aorta. Así, si la comunicación interauricular es grande, va a haber mayor flujo sanguíneo que pasa a dichas cavidades y esto mejora el pronóstico del paciente y le permite vivir más tiempo con poca sintomatología; si por el contrario existe un foramen oval pequeño o la comunicación interauricular es pequeña, hay gran sobrecarga del volumen de las cavidades derechas, lo que hace que el paciente entre rápidamente en insuficiencia cardíaca derecha, mientras que el flujo sistémico estará disminuido. La sobrecarga derecha que inicialmente es principalmente de volumen se asocia más tarde a la sobrecarga de presión, dada por el aumento de las resistencias pulmonares, lo cual ocurre en forma prematura y progresiva. El flujo sanguíneo llega con dificultad al ventrículo izquierdo, lo que hace que este se observe ligeramente hipodesarrollado lo mismo que la aorta ascendente, mientras que la aurícula izquierda generalmente es hipoplásica, lo que está en favor de que el tamaño del ventrículo izquierdo depende del tamaño de la comunicación interauricular, como ya se mencionó. En estos casos, al existir una restricción a nivel del tabique interauricular, habrá aumento importante del flujo pulmonar, propiciándose la presencia de edema pulmonar y además, disminución del gasto cardíaco. Por otra parte, cuando no existe obstrucción, el comportamiento hemodinámico varía dependiendo de si el paciente vive a nivel del mar o a grandes alturas, pues en este último caso es muy acelerada la evolución hacia la hipertensión pulmonar severa, por lo que la insuficiencia cardíaca se instaura precozmente.
- En la CVPAT OBSTRUCTIVA Aunque el prototipo de este grupo es la CVPAT infracardíaca o infradiafragmática, puede existir una obstrucción en los otros tipos, incluyendo el supracardíaco, ya sea en la unión del colector o por compresión extrínseca del colector por alguna estructura como alguno de los bronquios, etc. En este grupo no existe la sobrecarga de volumen que existe en el drenaje venoso pulmonar anómalo no obstruido, excepción hecha del drenaje venoso pulmonar anómalo obstruido a nivel intracardíaco; en cambio, existe sobrecarga de presión por aumento de esta en los pulmones. Lo más importante en el drenaje venoso pulmonar anómalo obstruido es el aumento de presión venocapilar pulmonar que lleva a edema intersticial y a franco edema pulmonar, precozmente después del nacimiento y, en forma retrógrada, a aumento de las resistencias pulmonares por lo cual, disminuye el flujo pulmonar anterógrado, siendo este un aspecto contrario a lo que ocurre cuando no hay obstrucción en la que haya considerable aumento del flujo pulmonar. El edema pulmonar impide la oxigenación de la sangre y esto asociado al poco flujo que llega a las cavidades derechas por la obstrucción origina cianosis precoz en la vida posnatal. El poco flujo que llega a las cavidades izquierdas y a la aorta explica el hipodesarrollo de estas estructuras. En el drenaje venoso pulmonar anómalo obstruido a nivel intracardíaco, existe relevante sobrecarga de volumen y presión, como ya se mencionó, y las cavidades izquierdas están hipodesarrolladas.
- Clínica La clínica también variará si la CVPAT es obstructiva o no obstructiva. Observación Los pacientes con CVPAT no obstructiva, si no se han diagnosticado antes, generalmente se presentan entre el segundo y tercer mes de vida en promedio, presentando poca ganancia de peso, polipnea y un síndrome de dificultad respiratoria importante, cianosis moderada que mejora con el oxígeno y, la mayoría de las veces, insuficiencia cardíaca. Un hallazgo significativo a la observación incluso después del primer mes de vida es el “abombamiento” o prominencia paraesternal izquierda, como signo de notable crecimiento del ventrículo derecho. Por el contrario, en la CVPAT obstructiva encontramos a los pacientes críticamente enfermos en la primera semana de vida con cianosis, dificultad respiratoria marcada e insuficiencia cardíaca47.
- Por el contrario, en la CVPAT obstructiva encontramos a los pacientes críticamente enfermos en la primera semana de vida con cianosis, dificultad respiratoria marcada e insuficiencia cardíaca.
- El manejo previo a la derivación del paciente con TAPVR obstruido generalmente incluye maximizar la PaO2 con soporte ventilatorio, que puede incluir niveles significativos de presión positiva al final de la espiración (PEEP), presiones inspiratorias y FiO2, evitando la acidosis metabólica y manteniendo la estabilidad hemodinámica con el uso de medicamentos inotrópicos según sea necesario. El óxido nítrico inhalado previo a la derivación está contraindicado porque la dilatación arteriolar pulmonar y el aumento del flujo sanguíneo pulmonar ante una obstrucción anatómica distal fija empeorarán la mecánica pulmonar y, a menudo, paradójicamente, empeorarán la hipoxemia. La ecocardiografía transesofágica suele estar contraindicada debido al riesgo de mayor compresión y obstrucción de las venas pulmonares incluso en presencia de TAPVR no obstruido. Es útil la monitorización perioperatoria de las presiones arteriales pulmonar, auricular izquierda y venosa central.
- Después de la derivación, el óxido nítrico debe usarse empíricamente en el caso de TAPVR obstruido y debe estar fácilmente disponible en TAPVR sin obstrucción. La hipertensión pulmonar perioperatoria ocurre hasta en el 50% de los pacientes y es un factor de riesgo importante de mortalidad temprana. Las crisis hipertensivas pulmonares pueden evitarse empleando hiperventilación, uso de oxígeno al 100%, alcalinización sistémica, sedación, parálisis y óxido nítrico. El sildenafilo, el sulfato de magnesio y la prostaglandina E1 se han utilizado en algunos pacientes para tratar la hipertensión pulmonar grave [164]. Se ha informado hipertensión pulmonar paradójica con hipotensión sistémica a partir del uso posoperatorio de óxido nítrico en pacientes con obstrucción auricular preoperatoria y ventrículo izquierdo disfuncional y con poca distensibilidad. Se cree que esta hipertensión pulmonar paradójica se debe a aumentos agudos en el flujo sanguíneo pulmonar y la precarga excesiva resultante en el lado izquierdo no distensible .
- La función pulmonar puede verse comprometida después de la derivación como resultado de dos lesiones pulmonares: edema pulmonar preoperatorio secundario a obstrucción venosa pulmonar; y la respuesta inflamatoria de la CEC. Disminuye la distensibilidad pulmonar y se desarrolla un gran gradiente arterial-alveolar. La distribución de gas pulmonar se puede optimizar con el uso de ventilación con control de presión y alterando la PEEP para mejorar la distensibilidad pulmonar.
- Después de la reparación, las presiones de llenado de la aurícula izquierda pueden estar elevadas debido al tamaño pequeño y la baja distensibilidad de la aurícula y el ventrículo izquierdos. Aceptar presiones arteriales bajas durante el destete de la CEC ayudará a evitar la distensión excesiva del lado izquierdo "no preparado". Las presiones de la arteria pulmonar con frecuencia son iguales o, a veces, mayores que las presiones sistémicas inmediatamente después del retiro del bypass. Si el ventrículo derecho funciona adecuadamente, esta situación suele tolerarse bien durante períodos breves, ya que la PVR disminuye en la primera hora después de la derivación. El manejo cuidadoso de los líquidos, la optimización de la frecuencia y el ritmo cardíacos y el apoyo inotrópico mejorarán el gasto cardíaco. El marcapasos cardíaco temporal también puede ser útil. Las arritmias perioperatorias, especialmente las taquicardias supraventriculares, ocurren hasta en 20% de los pacientes. Si se tolera, un inovasodilatador como la milrinona disminuirá el trabajo del ventrículo izquierdo y mejorará el gasto cardíaco. Es importante reconocer que la curva de Frank-Starling es muy plana en el ventrículo izquierdo pequeño y no distensible, y la administración de solo unos pocos mililitros de líquido puede hacer que el ventrículo izquierdo se sobredistienda y falle.