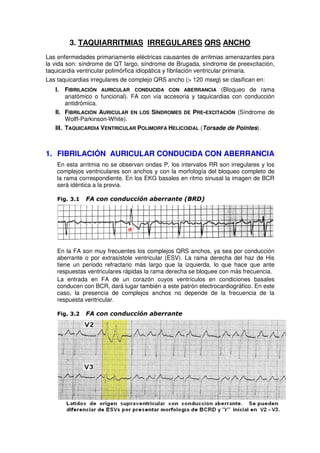
Taquiarritmias irregulares QRS ancho
- 1. 3. TAQUIARRITMIAS IRREGULARES QRS ANCHO Las enfermedades primariamente eléctricas causantes de arritmias amenazantes para la vida son: síndrome de QT largo, síndrome de Brugada, síndrome de preexcitación, taquicardia ventricular polimórfica idiopática y fibrilación ventricular primaria. Las taquicardias irregulares de complejo QRS ancho (> 120 mseg) se clasifican en: I. FIBRILACIÓN AURICULAR CONDUCIDA CON ABERRANCIA (Bloqueo de rama anatómico o funcional). FA con vía accesoria y taquicardias con conducción antidrómica. II. FIBRILACIÓN AURICULAR EN LOS SÍNDROMES DE PRE-EXCITACIÓN (Síndrome de Wolff-Parkinson-White). III. TAQUICARDIA VENTRICULAR POLIMORFA HELICOIDAL (Torsade de Pointes). 1. FIBRILACIÓN AURICULAR CONDUCIDA CON ABERRANCIA En esta arritmia no se observan ondas P, los intervalos RR son irregulares y los complejos ventriculares son anchos y con la morfología del bloqueo completo de la rama correspondiente. En los EKG basales en ritmo sinusal la imagen de BCR será idéntica a la previa. Fig. 3.1 FA con conducción aberrante (BRD) En la FA son muy frecuentes los complejos QRS anchos, ya sea por conducción aberrante o por extrasístole ventricular (ESV). La rama derecha del haz de His tiene un periodo refractario más largo que la izquierda, lo que hace que ante respuestas ventriculares rápidas la rama derecha se bloquee con más frecuencia. La entrada en FA de un corazón cuyos ventrículos en condiciones basales conducen con BCR, dará lugar también a este patrón electrocardiográfico. En este caso, la presencia de complejos anchos no depende de la frecuencia de la respuesta ventricular. Fig. 3.2 FA con conducción aberrante
- 2. 2. FIBRILACIÓN AURICULAR EN LOS SÍNDROMES DE PRE-EXCITACIÓN En esta arritmia no se observan ondas P, los intervalos RR son muy irregulares, la respuesta ventricular es muy rápida y los complejos QRS son anchos con un empastamiento inicial que corresponde a la onda delta. Típicamente, la anchura de los complejos varía latido a latido en función de la velocidad de conducción de la vía anómala. El síndrome de WPW no siempre está presente en el EKG basal. Sin que se sepa la causa, la FA es más frecuente en los pacientes con WPW que en los controles. En ocasiones puede ser la presentación del WPW y, generalmente, no suele haber otra cardiopatía orgánica subyacente. Esta arritmia ha de sospecharse siempre que exista FA con QRS ancho, por las importantes implicaciones terapéuticas que conlleva, ya que están contraindicados todos los fármacos que bloquean o enlentecen la conducción por el NAV (digoxina, calcioantagonistas, -bloqueadores) por favorecer la conducción por la vía accesoria, pudiéndose transmitir al ventrículo una cantidad muy elevada de estímulos auriculares y desembocar en una fibrilación ventricular. Los fármacos más empleados son los del grupo Ia, Ic y III, aunque si se requiere una rápida vuelta al ritmo sinusal es preferible la cardioversión eléctrica, dada la elevada posibilidad de desembocar en una FV. Para el tratamiento a largo plazo es más segura la ablación por radiofrecuencia de la vía anómala. En el contexto del WPW pueden derivar tres grandes tipos de arritmias: − Taquicardia ortodrómica: el estímulo baja por el sistema de conducción y sube por la vía accesoria (vía lenta que conduce por la ley del todo o nada) hacia las aurículas. Es de QRS estrecho, más frecuente en varones con inicio y fin bruscos y presentan onda P retrógrada (negativa inferior, positiva en V1 y aVR), pero puede no verse si la frecuencia de la taquicardia es alta. − Taquicardia antidrómica: el funcionamiento es a la inversa, por lo que se trata de una taquicardia de QRS ancho y obliga a diagnóstico diferencial con la TV. − FA preexcitada: la arritmia más importante y menos frecuente, por tratarse de una FA que conduce parte por tejido normal y parte por la vía accesoria, por lo que es de alta frecuencia. El tipo más frecuente de arritmia en el síndrome de WPW corresponde a la denominada TPSV ortodrómica (variedad común de TPSV). En estos casos se establece una taquicardia por macrorreentrada en que el circuito está compuesto por la vía nodo-hisiana, ventrículo, haz paraespecífico (haz de Kent) y aurícula. El componente anterógrado del circuito está dado por las vías normales y el retrógrado por el haz paraespecífico El complejo QRS será angosto (al menos que aparezca bloqueo de rama), con un intervalo PR normal o prolongado y un intervalo HV normal. La despolarización auricular necesariamente deberá ocurrir después de la despolarización ventricular. El desencadenamiento de este tipo de taquicardia ocurre por la presencia de extrasístoles conducidas por una sola de las vías, retornando posteriormente por la otra. El análisis del EKG de superficie, no sólo permite diagnosticar correctamente este síndrome, sino que también ayuda a localizar el haz anómalo en la medida que los complejos QRS tengan un grado suficiente de preexcitación. Los haces paraespecíficos pueden localizarse en la región ánteroseptal, en las paredes libres o en la región pósteroseptal. La forma poco común de TPSV en el síndrome WPW corresponde a la denominada taquicardia antidrómica. En estos casos los complejos QRS tienen un grado máximo de preexcitación. El circuito está dado por el haz paraespecífico
- 3. participando en la conducción anterógrada y la vía normal en la conducción retrógrada. En pacientes con taquicardias preexcitadas, no es infrecuente que tengan más de un haz, pudiendo en estos casos establecerse un macrocircuito con participación de ambos haces, sin que la vía normal juegue un rol en el mecanismo de la taquicardia. Las vías accesorias, y más si son múltiples, favorecen la aparición de FA. Esta arritmia se puede presentar como una taquicardia de QRS estrecho o de QRS ancho, bien sea por preexcitación (conducción por la vía accesoria) o bien por aberrancia o bloqueo de rama en el haz de His. La FA conducida a los ventrículos a través de una vía accesoria puede desencadenar, si la respuesta ventricular es rápida, síncope e incluso fibrilación ventricular y muerte súbita. Otras arritmias observadas con cierta frecuencia en los casos de SWPW son fibrilación auricular (FA) y flúter auricular. En casos de haces paraespecíficos con períodos refractarios cortos ( 250 mseg), puede alcanzarse altas frecuencias ventriculares durante ellas, ya que muchos impulsos auriculares podrán despolarizar los ventrículos a través del haz anómalo con consiguiente deterioro hemodinámico y con riesgo de que los pacientes presenten FV y muerte súbita. Fig. 3.3 FA en un paciente con síndrome de preexcitación La aparición de FA en un paciente con WPW puede producir una conducción preferente por la vía accesoria en vez de por la vía normal de conducción desarrollando respuesta ventricular muy rápida con mala tolerancia hemodinámica y que puede desembocar en FV. El diagnóstico EKG se establece por: ritmo irregular, FC elevada, QRS ancho (conducción por vía accesoria) de morfología cambiante y algunos latidos con QRS estrecho (conducción por nodo AV).
- 4. La Fibrilación Auricular Pre-excitada se presenta con un patrón electrocardiográfico característico consistente en taquicardia irregular con un complejo QRS ancho, con frecuencia alta y con morfología similar de todos los complejos QRS (lo que la diferencia de las taquicardias ventriculares polimórficas, que son también rápidas e irregulares pero en las que los QRS van variando latido a latido en cada derivación). Es característico que de vez en cuando se intercalen uno o varios latidos con un complejo QRS estrecho. Después de las taquicardias reentrantes auriculoventriculares, la fibrilación auricular (FA) es la arritmia más frecuente en el síndrome de WPW, con una prevalencia que oscila entre el 10 y el 38%. La FA preexcitada puede inducir colapso hemodinámico y muerte súbita. Esta arritmia se produce principalmente en la tercera y quinta década de la vida. Durante la FA el menor intervalo R-R preexcitado está asociado con el riesgo de padecer muerte súbita. Por tanto, esta arritmia debe considerarse una urgencia y ser tratada rápidamente. Si no existe inestabilidad hemodinámica el fármaco de elección es la procainamida; si la hubiera, lo indicado es la cardioversión eléctrica. Wolff, Parkinson y White señalaron en su artículo original que los pacientes con preexcitación ventricular tienen una mayor predisposición a experimentar fibrilación y aleteos auriculares que la población general. Esta arritmia suele ser paroxística más que persistente o permanente y su aparición sería facilitada por la coexistencia de cardiopatías subyacentes. La fibrilación auricular puede ser iniciada por una taquicardia supraventricular por macrorreentrada o por taquicardia auricular. La taquicardia ortodrómica constituye el 100% de las taquicardias del síndrome de WPW en niños menores de 1 año, y el 90% en todas las edades. En el síndrome de Wolff-Parkinson-White la Fibrilación Auricular se presenta como una taquicardia irregular con QRS ancho y es parte del grupo denominado taquicardias preexcitadas. El antecedente de la presentación en ritmo sinusal de un patrón electrocardiográfico de síndrome de WPK unido a la presencia de un intervalo R-R irregular durante la taquicardia son elementos clave para el diagnóstico inmediato. El mecanismo involucrado en la génesis del flúter y de la FA en el síndrome de WPW no ha sido del todo aclarado. Aquellos pacientes que presentan haces ocultos (sin capacidad manifiesta de conducción anterógrada) no tienen riesgo de desarrollar FA preexcitadas, pero sí TPSV ortodrómicas o FA sin preexcitación. La FA en el síndrome de WPW debe ser diferenciada de una FA ordinaria con QRS ancho por aberración y conduciendo por el nodo AV. La principal característica diferencial de la FA preexcitada (FAP) es que en los primeros 40 mseg del complejo QRS en las 12 derivaciones del EKG coinciden con la morfología de los primeros 40 mseg (zona de la onda delta) del EKG en ritmo sinusal con preexcitación. Cuando la frecuencia ventricular es muy elevada y los QRS son muy aberrantes se puede diagnosticar erróneamente como taquicardia ventricular. La FAP puede presentarse básicamente de dos formas: una, cuando el ritmo auricular desorganizado es conducido a los ventrículos por el sistema normal de conducción alternando intermitentemente con conducción anterógrada por la vía accesoria (Figura 13.4); la otra, cuando los impulsos fibrilatorios de las aurículas llegan al ventrículo por la vía accesoria (Figura 13.5), esta forma tiene peor pronóstico.
- 5. Fig. 3.4 FA en el síndrome WPW: FA intermitentemente preexcitada Fig. 3.5 FA en el WPW: FA conduciendo constantemente por la vía
- 6. La Fibrilación Auricular Preexcitada es una entidad que se observa en pacientes con antecedentes de TPSV y se caracteriza por complejos ventriculares muy aberrantes y atípicos, que se pueden alternar con complejos QRS angostos y alcanzar frecuencias ventriculares 200 latidos / minuto con intervalos RR 250 milisegundos. Si un ventrículo se estimula hasta frecuencias entre 250 – 300 / minuto se puede inducir una FV, que es la causa por la cual una FA preexcitada puede terminar en muerte súbita en personas sanas. El tratamiento de la misma es la cardioversión eléctrica inmediata. Evitar en dichos pacientes los fármacos que depriman la conducción por el nodo AV (ß-bloqueadores, calcioantagonistas, adenosina y digoxina) ya que, en caso de desarrollar FA, favorecerán la conducción por la vía accesoria y la aparición de respuesta ventricular muy rápida. Complicaciones.- En algunos casos la FAP es la arritmia de debut en paciente con síndrome de WPW pudiendo producir síncope y muerte súbita. La FA en presencia de vías accesorias con períodos refractarios anterógrados muy cortos puede generar frecuencias ventriculares elevadas con el consiguiente riesgo de Fibrilación Ventricular. En estos pacientes el riesgo de muerte súbita se estima en hasta 0,10% paciente / año y no es fácilmente predecible. La FAP puede presentarse por primera vez entre los 10 y 72 años, aún una década después. Los pacientes con síndrome de WPW y FA son de mayor edad que los que no tienen FA (45 años vs 34 años) y es más frecuente en hombres que en mujeres (74% vs 53%). Una historia de síncope forma parte de los factores de riesgo independientes para la presentación de una FA. Manejo clínico.- Cuando coexisten el síndrome de WPW y FA no deben usarse -bloqueadores, bloqueadores de canales de calcio ni digoxina. Estos fármacos agravan la situación clínica y pueden precipitar colapso hemodinámico debido a sus propiedades depresoras de la conducción del nodo AV, lo que facilita la conducción anterógrada por la vía accesoria. La droga de elección es la procainamida, aunque propafenona, flecainida y disopiramida también se han usado. Si hay compromiso hemodinámico el tratamiento de elección es la cardioversión eléctrica sincrónica. El grupo del Dr. Raimundo Carmona Puerta (Argentina) considera que esta situación es una urgencia electrofisiológica, por lo que la ablación de la vía accesoria debe ser practicada a la brevedad. Todo hallazgo de preexcitación ventricular del tipo WPW debe ser sometido a evaluación electrofisiológica para definir riesgo y conducta. Se sabe que muchas vías accesorias estarán siempre sin manifestarse clínicamente, pero también se sabe que cualquiera de ellas puede costar impredeciblemente una vida. 3. TAQUICARDIA VENTRICULAR POLIMORFA HELICOIDAL TAQUICARDIA VENTRICULAR POLIMÓRFICA.- Taquicardia ventricular que cursa con variación de la morfología de los complejos QRS en una misma derivación. Si la morfología de los complejos QRS varía indistintamente de un latido a otro se denomina taquicardia ventricular polimórfica y si la variación de la morfología es cíclica se denomina taquicardia ventricular polimórfica tipo torsades de pointes (puntas torcidas).
- 7. Fig. 3.6 Taquicardia ventricular polimórfica Fig. 3.7 TV Polimórfica tipo Torsades de Pointes En la taquicardia ventricular polimórfica, así como para el QT largo y el síndrome de Brugada se ha involucrado un desbalance autonómico como parte de los mecanismos inductores de estas arritmias. Por ello, los episodios de síncope o muerte súbita frecuentemente están asociados con ejercicio o estrés. . Fig. 3.8 TV Polimórfica y Fibrilación ventricular La TV polimórfica catecolaminérgica, el síndrome QT largo y el síndrome de Brugada son enfermedades arritmogénicas hereditarias. Comparten una susceptibilidad genéticamente determinada a la taquicardia ventricular y a la muerte cardiaca súbita, en ausencia de anomalías estructurales reconocibles del corazón. Estos síndromes tienen una prevalencia estimada por debajo de 5 en 10.000 son, por definición, enfermedades raras. La taquicardia ventricular sostenida polimorfa se clasifica: (1) Con intervalo QT normal: cardiopatía isquémica aguda, miocardiopatía dilatada, miocardiopatía hipertrófica, enfermedad de Chagas, síndrome de Brugada; (2) Con intervalo QT prolongado: adquirido y congénito. SÍNDROME DE BRUGADA.- Descrito en 1992 por los hermanos Brugada, se caracteriza por síncope o muerte súbita, en relación con taquiarritmias ventriculares, en personas con corazón estructuralmente sano y con patrón EKG de elevación del ST en V1 a V3 y morfología similar a la de un bloqueo de rama derecha. La muerte cardiaca súbita es una muerte inesperada de origen cardiaco que ocurre en menos de una hora después de haber iniciado los síntomas. Está determinado por más de 100 mutaciones de un gen en el cromosoma 3. Este síndrome es una canalopatía de origen genético con transmisión autosómica dominante y penetrancia incompleta ocasionada por una variedad de mutaciones de los genes que dan origen a la proteína de los canales de sodio cardíacos; algunas de ellas además asociadas al síndrome de QT largo variante 3 –SQTL3–. Los mecanismos celulares e iónicos de las alteraciones EKG y de las arritmias están originados por una actividad anormal de los canales iónicos (anomalía del funcionamiento de los canales de sodio en el epicardio del tracto de salida del ventrículo derecho).
- 8. Su prevalencia, muy variable, se estima entre 5 y 60 por 10.000 habitantes, siendo mayor en los países asiáticos. Se caracteriza por electrocardiograma (EKG) con patrón de aparente bloqueo de rama derecha (BRD) y manifiesta alteración de la repolarización ventricular, que consiste en supradesnivel persistente del punto J y del segmento ST que cae con lentitud y finaliza en una onda T negativa en derivaciones precordiales derechas V1, V2 y V3 (onda J idiopática) con dos variantes morfológicas específicas (convexa y cóncava o en silla de montar), QTc normal, episodios sincopales y/o paro cardiorrespiratorio con tendencia elevada al desarrollo de taquicardia ventricular polimorfa (TVP) muy rápida (de 260 a 352 latidos / minuto) que a menudo degenera en fibrilación ventricular (FV) y muerte súbita. Fig. 3.9 Síndrome de Brugada La asociación de BRD, supradesnivel persistente del punto J y del segmento ST de V1 a V2 o V3, con QTc normal, en pacientes masculinos de mediana edad, con corazón estructuralmente normal y recuperados de un episodio de muerte súbita por TVP/ FV caracterizan el síndrome clínica y electrocardiográficamente. La sola presencia del patrón electrocardiográfico, en ausencia de los eventos de TVP/ FV, no debe considerarse síndrome de Brugada y es mejor denominarlo “patrón Brugada del EKG”. Fig. 3.10 Síndrome de Brugada. Patrón tipo 1 De forma general, existen tres patrones electrocardiográficos del síndrome de Brugada; el tipo 1 es el único de importancia clínica, el resto no cobra importancia si no se convierte en tipo 1.
- 9. Tipo 1: Elevación del punto J 2 mm, con elevación convexa del ST y gradual descenso en su porción terminal seguido de onda T negativa, que muchas veces se puede confundir con la imagen del bloqueo incompleto de rama derecha. Tipo 2: Elevación del punto J 2 mm, con una elevación del ST de 1 mm o más, en forma de silla de montar, y gradualmente descendente en su porción terminal, manteniéndose 1 mm por encima de la línea basal seguido de onda T positiva o bifásica. También se le conoce como síndrome pseudo-Brugada. Tipo 3: es como el tipo 2, excepto que la elevación del ST es de 1 mm por encima de la línea basal, seguido de onda T positiva. Es necesario plantear diagnóstico diferencial con IAM, sobre todo del VD, miocarditis aguda, tromboembolismo pulmonar agudo, hiperpotasemia, displasia arritmogénica del VD, enfermedad de Chagas y, especialmente, con BRD asociado con repolarización precoz. Fig. 3.11 Síndrome de Brugada tipo 1.- Desplazamiento de 3 mm del punto J con supradesnivel del ST de convexidad superior y negativización asimétrica de la onda T en V1, V2 y V3. Patrón de BRD RSr´ en V1 y V2 con prolongación del QRS (120 mseg). Las manifestaciones electrocardiográficas de la enfermedad son fluctuantes, pudiendo permanecer ocultas o muy atenuadas en muchos casos, dificultando el diagnóstico; por lo que resulta importante prestar atención a los criterios diagnósticos establecidos del Brugada, sus variantes electrocardiográficas, conocer la presencia de fluctuaciones espontáneas en su aparición, y los modos de intentar desenmascararlo cuando existe la sospecha. Sin embargo, la imagen diagnóstica puede ser variable, pasando por periodos con EKGs prácticamente normales, u otros mostrando los patrones 2 ó 3. El tono vagal, la temperatura corporal, drogas antiarrítmicas y no cardiovasculares, o el
- 10. estado hormonal, pueden tener influencia en la manifestación del patrón típico de Brugada. En un estudio, el 51% de pacientes tuvieron fluctuaciones en su EKG entre patrones diagnósticos y no diagnósticos. Fig. 3.12 Síndrome de Brugada. ESV desencadenando FA De tal modo que en un paciente con historia de presíncope, o síncope, o de palpitaciones, o antecedentes familiares de muerte súbita, en quien se sospecha la presencia de Brugada y cuyo EKG no muestra el patrón diagnóstico típico, o en casos asintomáticos con un EKG sospechoso pero no característico, se debe realizar una búsqueda intencionada. Esta búsqueda debe incluir la toma de trazados electrocardiográficos durante un episodio febril, luego de una comida copiosa (más evidente después de la cena) o después de un ejercicio intenso. Existen fármacos que pueden desenmascarar el patrón característico del Brugada como los bloqueadores de canales de sodio (flecainide, ajmalina y procainamida), vagotónicos, agonistas -adrenérgicos, -bloqueadores y antidepresivos (desipramina). En síntesis, el patrón EKG del Brugada, se está reconociendo con mayor frecuencia, y dadas sus implicancias relacionadas con mayor riesgo de muerte súbita, es recomendable que todo médico –no solo el especialista– que atiende pacientes con EKG, tenga un alto índice de sospecha y tenga presente que éste, cuál camaleón, es cambiante en su apariencia. SÍNDROME DE QT LARGO.- El SQTL es una alteración del sistema de conducción del corazón. La alteración afecta la repolarización, subsecuentemente el restablecimiento de la carga eléctrica del miocardio luego de cada latido. El SQTL tiene las siguientes características: (1) Prolongación del QT con onda T negativa y anormal onda U negativa; (2) QTc mayor de 460 milisegundos −0,46 segundos−; (3) Síncope recurrente causado por torcedura de puntas; (4) Diagnóstico equivocado como convulsiones o síncope vasovagal; y (5) Muerte súbita. Se ha identificado anormalidades cromosómicas que afectan los canales de sodio y potasio con diferente expresión fenotípica. De acuerdo con el origen de la prolongación del QT (QTc 460 mseg) existen dos: adquirida y congénita. a) QT LARGO ADQUIRIDO.- Por fármacos: antiarrítmicos que prolongan la repolarización (clase Ic, Ia), haloperidol, aztemizol, eritromicina, clotrimazol, organofosforados, inhibidores de la proteasa, cisapride.
- 11. Por alteraciones del medio interno: hipokalemia, hipomagnesemia, hipocalcemia. Lesiones del SNC. Bradicardia sinusal, bloqueo AV. Hipotiroidismo, anorexia. b) QT LARGO CONGÉNITO.- Es una enfermedad familiar, los episodios de taquicardias por lo general se dan en jóvenes y se desencadenan por descargas adrenérgicas como el ejercicio o el estrés y pueden asociarse con síncope, con o sin convulsiones. En los pacientes con síndrome de QT largo congénito, aunque no se trata de una miocardiopatía., existe una disautonomía que genera gran dispersión de la refractariedad que se traduce en la prolongación del QT en el EKG. Estos pacientes, presentan torsión de puntas desencadenada por descarga adrenérgica por lo que los -bloqueantes son la droga de elección. Si estos fracasan, se extirpa el ganglio cervical estrellado izquierdo, responsable de la disautonomía. En los casos adquiridos, la principal medida de prevención es el diagnóstico adecuado y corrección de la causa subyacente: las más frecuentes son el uso de antiarrítmicos, en especial los del grupo I de la clasificación de Vaugham y Williams, miocardiopatías y los trastornos del sistema nervioso central. Los factores de riesgo son sexo femenino y estado post-reversión de una FA. Fig. 3.13 Síndrome de QT largo, episodios de torsión de puntas y FA El pronóstico de mortalidad después del primer episodio de síncope es de 20% en el primer año y 50% en los 10 años. Con la terapia la mortalidad puede reducirse al 3 - 4%. Los -bloqueadores previenen nuevo síncope en el 75% de pacientes y el síncope recurrente puede ser tratado con marcapasos. El paro cardiaco en estas víctimas, la mayoría niños y adolescentes, se debe a taquiarritmia ventricular. Usualmente la mayoría de los episodios de arritmias terminan solas e incluso provocan una disminución transitoria de la conciencia (síncope). Sin embargo, cuando los episodios son prolongados, la insuficiencia circulatoria producto de la arritmia puede terminar en muerte súbita.
- 12. El SQTL ha sido clasificado en una forma esporádica no familiar y dos tipos hereditarios, con sordera (síndrome de Jervell y Lange-Nielson, autosómica recesiva) y sin sordera (síndrome de Romano Ward, autosómica dominante). Ambos síndromes incluyen síncope o muerte súbita. En 1991 MT. Keating y colaboradores demostraron vinculación entre SQTL y el cromosoma 11. Los dos criterios para el diagnóstico de SQTL son inexplicable pérdida transitoria de la conciencia con un EKG anormal. Las arritmias ventriculares y el síncope suelen ser provocadas por aumento de la frecuencia cardiaca en respuesta al ejercicio o a las emociones. TORSADES DE POINTES.- Síndrome que se caracteriza por repolarización ventricular prolongada con intervalos QT mayor de 450 / msg. y episodios de taquicardia ventricular con complejos QRS con amplitud variable, pero dando la impresión de girar alrededor de una línea isoeléctrica imaginaria. Los complejos QRS son de amplitud variable con cambios continuos en su eje eléctrico, hasta 180°, con una FC entre 160 – 250 / minuto. Aunque por lo general es autolimitada. La FC muy elevada provoca síntomas como mareos o síncope, y en ocasiones puede degenerar en fibrilación ventricular (FV). La prolongación de intervalo QT refleja la demora en el proceso de repolarización ventricular y aunque esta alteración suele manifestarse en forma permanente, puede observarse solo segundos antes del inicio de la taquicardia o en el latido posterior a una pausa posextrasistolica. Fig. 3.14 TV Polimórfica tipo Torsades de Pointes (Nótese el cambio en la dirección del eje de los complejos QRS) Las TV en por alteraciones hidroelectrolíticas como hipomagnesemia e hipopotasemia se producen porque favorecen el alargamiento del intervalo QT, que promueve una dispersión de la repolarización ventricular, y con ello la aparición de TV polimórficas tipo torsades de pointes. El síncope debido a torsades de pointes no es raro, y en su forma adquirida es resultado del tratamiento con fármacos que prolongan el intervalo QT. El tratamiento consiste en interrumpir inmediatamente el fármaco sospechoso. En pacientes críticos cardiovasculares la TV polimórfica tipo “puntas torcidas” se ha relacionado por intoxicación con fármacos y anormalidades electrolíticas.
- 13. Las torsades de pointes son una forma de taquicardia ventricular polimórfica denominadas así por Dessertenne y se puede distinguir dos tipos: 1) Asociadas a SQTL y 2) No asociadas a SQTL y que tienen un acoplamiento corto. El mecanismo de las torsades todavía es controvertido y unos autores están a favor de la reentrada y otros que son originadas por postpotenciales precoces y tardíos. Por último otros piensan que los post-potenciales inician la arritmia y la reentrada la mantiene. Las torsades asociadas a SQTL tanto congénito como adquirido se caracterizan por una sucesión de complejos ventriculares cuya polaridad y amplitud varían sucesivamente como si éstos rotasen sobre la línea isoeléctrica. Las puntas unas veces van hacia arriba y otras veces van hacia abajo. Es importante hacer un EKG de 12 derivaciones para poder determinar o diagnosticar las torsades ya que en una derivación puede aparentar una TV monomórfica. Fig. 3.15 Torsades de Pointes Generalmente hay en el trazado extrasístoles ventriculares con la misma morfología que el que inicia la torsade y el acoplamiento de la extrasístole suele estar alargado del orden de 500 a 800 mseg. El QT es largo y puede presentar alternancia de la onda T o alteraciones de la misma y también ciclos largo-corto al inicio de la torsade. Las torsades tienen dependencia de la bradicardia. Suelen ser autolimitadas pero a veces pueden terminar en FV. Las torsades con acoplamiento corto alrededor de 300 mseg o menos originan el fenómeno R/T. El QT de estos pacientes es normal. Los pacientes suelen ser jóvenes y sin daño estructural cardiaco. Puede haber degeneración en FV por lo que algunos casos son incluidos como FV idiopáticas. El estudio electrofisiológico puede inducir en algunos enfermos arritmias ventriculares. Es una arritmia de mal pronóstico, que suele conducir a la parada cardiaca en poco tiempo. Tratamiento.- El retiro del fármaco desencadenante y la corrección de las anormalidades electrolíticas; así como la colocación de marcapaso agudo y a largo plazo a quienes presentan esta arritmia por bloqueo cardiaco y bradicardia sintomática, son dos Recomendaciones Clase I con Nivel de Evidencia A. El manejo con sulfato de magnesio intravenoso es razonable para pacientes con síndrome QT largo y pocos episodios de torsades de pointes. El magnesio probablemente no es eficaz en pacientes con intervalo QT normal; Clase IIa con Nivel de Evidencia B. Alcanzar concentración de potasio sérico de 4,5 a 5,0 mMol / Litro es de Clase IIb con Nivel de Evidencia B para pacientes con torsades de pointes.
- 14. FLÚTER VENTRICULAR.- Se denomina «flúter ventricular» cuando la frecuencia cardíaca es muy rápida (mayor de 200 latidos / minuto) y el EKG registra un patrón continuo, regular en zig-zag, sin una clara definición de los complejos QRS ni las ondas T. Es un estado de emergencia eléctrica intermedia entre la taquicardia ventricular y la fibrilación ventricular. El tratamiento es similar a la fibrilación ventricular. Fig. 3.16 Flúter ventricular FIBRILACIÓN VENTRICULAR.- Serie descoordinada y potencialmente mortal de contracciones ventriculares ineficaces muy rápidas, causadas por múltiples y caóticos impulsos eléctricos. Es eléctricamente similar a la fibrilación auricular, excepto que tiene un pronóstico más grave. En la fibrilación ventricular (FV), los ventrículos simplemente se estremecen y no llevan a cabo contracciones coordinadas. Debido a que el corazón no bombea sangre, la FV es una forma de paro cardíaco y es mortal, a menos que sea tratada de inmediato. Para bombear sangre hacia el cuerpo, todas las áreas del corazón normalmente se contraen al mismo tiempo. Las aurículas se contraen antes que los ventrículos. Sin embargo, durante la FV, las contracciones se vuelven desorganizadas. El ritmo cardiaco es caótico y muy rápido (hasta 300 impulsos / minuto) y se caracteriza por no ser capaz de provocar latido cardiaco eficaz; así la falta de contracción de los ventrículos provoca que la sangre apenas se bombee desde el corazón produciéndose un colapso del sistema cardiovascular y una parada cardiaca. Taquicardia y Fibrilación Ventricular son los trastornos más frecuentes en el paro del adulto. Inicia con la taquicardia sin pulso y luego pasa a la FV. En el EKG el ritmo es irregular y hay ausencia de ondas P, QRS o T. Línea de base ondulante con múltiples formas y tamaños que traducen una actividad ventricular desorganizada e ineficaz. Fig. 3.17 Fibrilación ventricular Causas de la FV: cardiopatía congénita, accidente por electrocución o lesión al corazón, ataque cardiaco, enfermedades del músculo cardiaco (como miocardiopatías), cirugía del corazón o isquemia miocárdica. Aunque la mayoría de las personas que sufren de fibrilación ventricular no tienen antecedentes previos de enfermedad cardíaca, muchos tienen factores de riesgo para enfermedad cardiovascular, tales como tabaquismo, hipertensión y diabetes.
- 15. Síntomas: Quien presente FV se desmayará súbitamente o quedará inconsciente, debido a que cerebro y músculos dejan de recibir sangre del corazón. Se manifiesta de forma súbita, con ausencia de pulso, latidos cardíacos y presión arterial. La ausencia de riego sanguíneo provoca en el paciente pérdida de conciencia, pérdida de coloración de la piel y dilatación de las pupilas. La conmoción cardíaca (Commotio cordis) es la fibrilación ventricular seguida por muerte súbita desencadenada por un golpe torácico directo, no penetrante, involuntario, sin lesión de las costillas o el esternón (y sin enfermedad cardiovascular de base). Este término se empleó por primera vez en el siglo XIX, aunque la conmoción cardíaca se describió antes, en relatos del antiguo arte marcial chino de Dim Mak (o toque de muerte), en el que los golpes en la parte izquierda del esternón causaban la muerte súbita del contrincante. La ausencia de lesión cardíaca estructural distingue a la conmoción cardíaca de la contusión cardíaca, en la que golpes de alto impacto producen lesión traumática del tejido miocárdico y el tórax. La conmoción cardíaca se produce principalmente en niños, adolescentes y adultos jóvenes, en general durante su participación en ciertos deportes. En pacientes reanimados de paro cardíaco el 75% tienen fibrilación ventricular y el resto bradicardia y asistolia. El flúter y la fibrilación ventricular llevan a la pérdida del conocimiento, convulsión, apnea y muerte, si no se toman medidas enérgicas para restaurar el ritmo cardíaco. En pacientes no hospitalizados la causa más frecuente de fibrilación ventricular es la cardiopatía isquémica; incluso puede ser la única y última manifestación de la enfermedad, constituyéndose en uno de los tres síndromes de insuficiencia coronaria aguda (junto a la angina inestable y al infarto agudo del miocardio).
- 16. AUTOEVALUACION 1. El siguiente trazado corresponde a: ( ) FA con conducción aberrante ( ) Síndrome de Brugada ( ) Flutter auricular + BAV variable 2. El siguiente trazado corresponde a: ( ) Fibrilación ventricular (FV) ( ) Flúter ventricular ( ) Las dos anteriores
- 17. 3. El siguiente trazado corresponde a: ( ) Síndrome de Brugada ( ) Miocardiopatía chagásica ( ) Síndrome QT largo congénito 4. El siguiente trazado corresponde a: ( ) Taquicardia ventricular polimórfica ( ) FA en paciente con síndrome de WPW ( ) FA conducida con aberrancia
- 18. 5. El siguiente trazado corresponde a: ( ) Fibrilación auricular asociada a preexcitación ventricular ( ) Síndrome de Brugada ( ) FA conducida con aberrancia 6. El siguiente trazado, en variedades gruesa y fina, corresponde a: ( ) Flúter ventricular ( ) Fibrilación ventricular ( ) Taquicardia ventricular polimórfica RESPUESTAS 1) Síndrome de Brugada 2) Fibrilación ventricular 3) Síndrome QT largo congénito 4) FA en paciente con síndrome de WPW 5) FA asociada a preexcitación ventricular 6) Fibrilación ventricular
- 19. BIBLIOGRAFIA 1. American Heart Association. 2005 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. International Consensus on Science. Circulation. Part 7.3: Management of Symptomatic Bradycardia and Tachycardia. Circulation 2005; 112; 67-77. 2. Luis Tercedor Sánchez y col. ARRITMIAS Y ELECTROFISIOLOGÍA CARDIACA. Rev Esp Cardiol. 2008; 61 (Supl 1): 27-36. 3. Diego Ignacio Vanegas Cadavid MD; Jorge E. Lemus Lanziano, MD. ARRITMIAS EN LA UNIDAD DE CUIDADOS INTENSIVOS. 4. Enrique Alonso Formento y col. FIBRILACIÓN AURICULAR EN UN PACIENTE CON SÍNDROME DE WOLFF-PARKINSON-WHITE. Servicio de Urgencias Hospital “Obispo Polanco” de Teruel, España. Emergencias 2008; 20:213. 5. Carmona Puerta Raimundo y col. FIBRILACIÓN AURICULAR EN EL SÍNDROME DE WOLFF-PARKINSON- WHITE. Red Fed Arg Cardiol 2005; 34: 387 -391. 6. ACC/AHA/ESC 2006. GUIDELINES FOR MANEGEMENT OF PATIENTS WITH VENTRICULAR ARRHYTHMIAS AND THE PREVENTION OF SUDDEN CARDIAC DEATH. A Report of the American College of Cardiology / American Heart Association Task Force and the European Society of Cardiology Committee for Practice Gudelines. JACC Vol 48 N° 5, September 2006. 7. Alexis Lama T. SÍNDROME DE BRUGADA: UN CAMALEÓN LETAL. Rev Méd Chile 2008; 136:1493-94 8. Jesús Almendral Garrote, Esteban Gonzáles Torrecilla, Felipe Atienza Fernández, Dolores Vigil Escribano y Angel Arenal Maiz. TRATAMIENTO DE LOS PACIENTES CON PREEXCITACIÓN VENTRICULAR. Artículo de revisión. Rev Esp Cardiol 2004; 57(9): 859-68. 9. Scottish Intercollegiate Guidelines Network (SIGN). CARDIAC ARRHYTHMIAS IN CORONARY HEART DISEASE. February 2007. 10. Ary L. Goldberger. CLINICAL ELECTROCARDIOGRAPHY: A SIMPLIFIED APPROACH. Seventh Edition. 11. Dr. Jorge González Zuelgaray, Dr. Edgardo Schapachnik. PRIMER CURSO DE ARRITMIAS POR INTERNET. Trastornos de conducción. División de Cardiología. Hospital General de Agudos Dr. Cosme Argerich – Buenos Aires – Argentina. 12. Francis Morris et al. ABC of Clinical Electrocardiography. BMJ Books, BMA House, Tavistock Square, London 2003. 13. Dr. Alfonso Martín Martínez, Dr. Ángel Moya Mitjans, Dr. Julián Pérez Villacastín. MANEJO AVANZADO DE LAS ARRITMIAS CARDÍACAS: ALGORITMOS. Laboratorios Menarini, S.A. 14. Dr. Hugo Villarroel Ábrego. ARRITMIAS CARDÍACAS. Un Manual para Estudiantes de Medicina y Médicos de Atención Primaria. 1ª Edición – San Salvador – El Salvador 2006. 15. Dra. Annerys Méndez Rosabal. ARRITMIAS CARDÍACAS Y ELECTROFISIOLOGÍA. 16. Dr. Alejandro Fajuri. MANUAL DE ARRITMIAS. 2009 17. Dr. Fernando Cabrera Bueno, Dr. J. A. Rivero Guerrero. DIAGNÓSTICO Y MANEJO DE LAS ARRITMIAS. Hospital Universitario Virgen de la Victoria. Málaga – España. 18. Zipes DP, Libby P, Bonow RO, Braunwald E. BRAUNWALD'S HEART DISEASE: A TEXTBOOK OF CARDIOVASCULAR MEDICINE. 7th ed. St. Louis, Mo; WB Saunders; 2005:852-853. 19. M. García; L. Santana; A. Ramírez y M. Sánchez-Palacios. FIBRILACIÓN VENTRICULAR TRAS LA ADMINISTRACIÓN DE SUCCINILCOLINA. Med. Intensiva v.31 N° 4. Madrid, Mayo 2007. 20. Maron BJ, Mark Estes NA. COMMOTIO CORDIS: EPIDEMIOLOGÍA, CLÍNICA, PREVENCIÓN Y TRATAMIENTO. N Engl J Med 2010; 362;917. Intramed. MD. Enrique Portugal Galdos Médico Intensivista RNE 11936 Departamento de Emergencia y Cuidados Intensivos Hospital III Juliaca - EsSalud –- RAJUL - PERÚ