Propiedades gases simulación
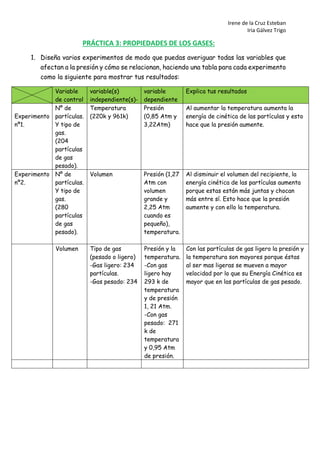
- 1. Irene de la Cruz Esteban Iria Gálvez Trigo PRÁCTICA 3: PROPIEDADES DE LOS GASES: 1. Diseña varios experimentos de modo que puedas averiguar todas las variables que afectan a la presión y cómo se relacionan, haciendo una tabla para cada experimento como la siguiente para mostrar tus resultados: Variable de control variable(s) independiente(s)- variable dependiente Explica tus resultados Experimento nº1. Nº de partículas. Y tipo de gas. (204 partículas de gas pesado). Temperatura (220k y 961k) Presión (0,85 Atm y 3,22Atm) Al aumentar la temperatura aumenta la energía de cinética de las partículas y esto hace que la presión aumente. Experimento nº2. Nº de partículas. Y tipo de gas. (280 partículas de gas pesado). Volumen Presión (1,27 Atm con volumen grande y 2,25 Atm cuando es pequeño), temperatura. Al disminuir el volumen del recipiente, la energía cinética de las partículas aumenta porque estas están más juntas y chocan más entre sí. Esto hace que la presión aumente y con ello la temperatura. Volumen Tipo de gas (pesado o ligero) -Gas ligero: 234 partículas. -Gas pesado: 234 Presión y la temperatura. -Con gas ligero hay 293 k de temperatura y de presión 1, 21 Atm. -Con gas pesado: 271 k de temperatura y 0,95 Atm de presión. Con las partículas de gas ligero la presión y la temperatura son mayores porque éstas al ser mas ligeras se mueven a mayor velocidad por lo que su Energía Cinética es mayor que en las partículas de gas pesado.
- 2. Irene de la Cruz Esteban Iria Gálvez Trigo Experimento 1
- 3. Irene de la Cruz Esteban Iria Gálvez Trigo Experimento 2
- 4. Irene de la Cruz Esteban Iria Gálvez Trigo Experimento 3
- 5. Irene de la Cruz Esteban Iria Gálvez Trigo 2. ¿Cómo la temperatura de los gases afecta al movimiento de sus moléculas? Justifica tu respuesta a partir de los resultados de simulaciones realizadas. Aporta pantallazo de la simulación que justifique tus resultados. A mayor temperatura mayor energía cinética hay en las partículas, lo que hace que éstas se muevan a velocidades mayores y aumente así la presión en el entorne en el que éstas se encuentren. Con 254 k de temperatura y 1,09 Atm y 251 partículas de gas ligero, si aumentamos la temperatura a 497k la presión aumenta a 1,94Atm. Si se baja la temperatura disminuye la energía cinética de las partículas, por lo que éstas se mueven menos y disminuye la presión Con 251 partículas de gas ligero y a 85K ahora, la presión es de 0,38 Atm.
- 6. Irene de la Cruz Esteban Iria Gálvez Trigo 3. Investiga cómo varía la presión si el volumen en el que se encuentran determinadas moléculas de gas disminuye. Explica y justifica tu respuesta aportando evidencias de la simulación donde pruebes tu respuesta (pantallazos): A) La presión aumenta porque hay más colisiones de moléculas.
- 7. Irene de la Cruz Esteban Iria Gálvez Trigo La presión aumenta considerablemente hasta el punto de que el recipiente puede llegar a explotar porque al disminuir el volumen del recipiente las partículas chocan más entre sí generando más presión y subiendo la temperatura y su energía cinética.
- 8. Irene de la Cruz Esteban Iria Gálvez Trigo 4. Compara la velocidad de las moléculas pesadas y ligeras cuando ambas están a la misma temperatura ¿Son iguales o diferentes estas velocidades? Explica y justifica tu respuesta con pantallazos de las simulaciones que hayas realizado. La velocidad de las que son más ligeras es mayor, puesto que éstas, al ser más ligeras se mueven con mayor facilidad al chocar unas con otras, lo cual hace que su presión y temperatura sea también mayor. En el caso 1, de gas pesado, con 300 partículas y a una temperatura de 282 K, la velocidad de éstas es de 411,52 m/s. En el caso 2, de gas ligero con 300 partículas y a la temperatura de 282 k, la velocidad es de 1.084,87 m/s. Como podemos observar la velocidad es mucho mayor.
- 9. Irene de la Cruz Esteban Iria Gálvez Trigo 5. Marca con una X las variables que afectan a la presión en los gases. Justifica tu respuesta a partir de los resultados con simulaciones y aporta pantallazos: XTemperatura XNúmero de partículas XVolumen XMasa de las partículas
- 10. Irene de la Cruz Esteban Iria Gálvez Trigo Todas las variables expuestas afectan a la presión de los gases: • La temperatura afecta, puesto que al aumentar ésta la Energía cinética de las partículas aumenta y con ello la presión y viceversa.
- 11. Irene de la Cruz Esteban Iria Gálvez Trigo • El número de partículas afecta, puesto que a mayor número de partículas más colisiones habrá entre las mismas y con ello aumentará la presión y viceversa.
- 12. Irene de la Cruz Esteban Iria Gálvez Trigo • El volumen del recipiente en el que se encuentra el gas afecta, pues cuanto más pequeño sea más chocarán las partículas entre sí y con esto aumentarán la presión y temperatura. Si aumenta el volumen disminuye la presión y la temperatura.
- 13. Irene de la Cruz Esteban Iria Gálvez Trigo • La masa de las partículas afecta, pues si éstas son más ligeras se desplazan a mayor velocidad, lo que hace que la presión sea mayor porque poseen más energía cinética y a su vez aumenta la temperatura. Pasa a la inversa si su masa es mayor.
- 14. Irene de la Cruz Esteban Iria Gálvez Trigo 6. ¿Podrías haber respondido a las preguntas anteriores sobre los gases y sus propiedades solo trabajando mediante libros de texto o experimentos manipulativos en el aula-laboratorio? Iria Gálvez: sí, puesto que así lo trabajé en secundaria y llegué a adquirir los conocimientos, pero es cierto que estas simulaciones son muy fáciles de usar y muy visuales y ayudan mucho a su comprensión. Irene de la Cruz: no, porque nunca di Física y Química en secundaria o bachillerato y me cuesta más imaginar los procesos que es dan a esta escala de partículas. La simulación es muy visual y me ha ayudado mucho a comprenderlo y a adquirir los conocimientos. Al principio, cuando lo dimos en clase teórica no me veía capaz de entenderlo, pero gracias a la simulación, no sólo he aprendido las propiedades de los gases, sino una manera de explicarlos. 7. A partir de las preguntas anteriores, ¿puedes justificar el interés didáctico de la simulación “gas properties” de la Universidad de Colorado? El uso de esta simulación es muy útil, puesto que la realización de estos experimentos en las aulas puede llegar a ser hasta peligroso al utilizarse elementos como mecheros y hacerse esto con alumnos de secundaria ( que tienden a ser más alborotadores) . Esta simulación permite entender los conceptos de las propiedades de los gases de una forma muy sencilla y visual, mostrando aspecto que en la vida cotidiana son difíciles de entender, pues imaginar partículas diminutas que realmente son invisibles resulta bastante complicado y más si las personas que van a hacerlo no han tenido mucho trato con contenidos de física como suele ocurrir en el caso de los alumnos de secundaria. Es muy útil además, porque con el modelo tradicional los alumnos no llegan a entender bien los fenómenos que ocurren, y solo aprenden meras fórmulas o leyes que no comprenden. Esto puede hacer que lleguen a temer a la misma asignatura de Física y Química en la que se explican los contenidos, pues al no comprender bien lo que están aprendiendo o haciendo en los ejercicios prácticos de clase pueden sentirse perdidos. Este tipo de simulaciones, al ayudar a que interioricen los conceptos, pueden incluso llegar a hacer que aumente también su autoestima al sentirse capaces de comprender los contenidos.