Tabla periodica
•Descargar como PPT, PDF•
0 recomendaciones•1,675 vistas
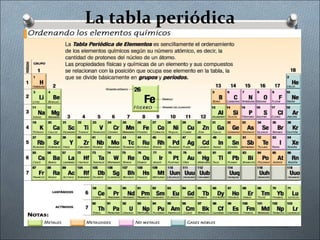
La tabla periódica clasifica los elementos químicos en grupos y períodos según sus propiedades periódicas recurrentes. Fue desarrollada por Mendeleiev y Meyer y consta actualmente de 120 elementos ordenados en 18 grupos de columnas y 7 períodos de filas. Los elementos dentro de cada grupo comparten propiedades químicas como la cantidad de electrones de valencia.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente

Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente
Propiedades de las sustancias según el tipo de enlace

Propiedades de las sustancias según el tipo de enlace
Numeros de oxidacion de los mentales y no metales.

Numeros de oxidacion de los mentales y no metales.
Principios de quimica y estructura ena1 - ejercicio 15 ley de las proporci...

Principios de quimica y estructura ena1 - ejercicio 15 ley de las proporci...
Destacado
Destacado (20)
Funciones de la administración, tipos de gerentes 1

Funciones de la administración, tipos de gerentes 1
Como tener exito en la sustentacion del trabajo de investigacion

Como tener exito en la sustentacion del trabajo de investigacion
Similar a Tabla periodica
Similar a Tabla periodica (20)
Más de Ambrocio Teodoro Esteves Pairazaman
INFLUENCIA DEL PROGRAMA “FORTALECIÉNDOME” PARA LA PREVENCIÓN DEL SÍNDROME DE BURNOUT EN LOS Y LAS DOCENTES DEL NIVEL INICIAL DE LA INSTITUCIÓN EDUCATIVA FAP “SAMUEL ORDOÑEZ VELÁSQUEZ” – CASTILLA – 2011.,Teodoro,Esteves,AmbrocioINFLUENCIA DEL PROGRAMA “FORTALECIÉNDOME” PARA LA PREVENCIÓN DEL SÍNDROME DE...

INFLUENCIA DEL PROGRAMA “FORTALECIÉNDOME” PARA LA PREVENCIÓN DEL SÍNDROME DE...Ambrocio Teodoro Esteves Pairazaman
Más de Ambrocio Teodoro Esteves Pairazaman (15)
INFLUENCIA DEL PROGRAMA “FORTALECIÉNDOME” PARA LA PREVENCIÓN DEL SÍNDROME DE...

INFLUENCIA DEL PROGRAMA “FORTALECIÉNDOME” PARA LA PREVENCIÓN DEL SÍNDROME DE...
Último
Último (20)
PP_Comunicacion en Salud: Objetivación de signos y síntomas

PP_Comunicacion en Salud: Objetivación de signos y síntomas
RESOLUCIÓN VICEMINISTERIAL 00048 - 2024 EVALUACION

RESOLUCIÓN VICEMINISTERIAL 00048 - 2024 EVALUACION
Tema 19. Inmunología y el sistema inmunitario 2024

Tema 19. Inmunología y el sistema inmunitario 2024
UNIDAD DIDACTICA nivel inicial EL SUPERMERCADO.docx

UNIDAD DIDACTICA nivel inicial EL SUPERMERCADO.docx
Lineamientos de la Escuela de la Confianza SJA Ccesa.pptx

Lineamientos de la Escuela de la Confianza SJA Ccesa.pptx
Las Preguntas Educativas entran a las Aulas CIAESA Ccesa007.pdf

Las Preguntas Educativas entran a las Aulas CIAESA Ccesa007.pdf
Santa Criz de Eslava, la más monumental de las ciudades romanas de Navarra

Santa Criz de Eslava, la más monumental de las ciudades romanas de Navarra
Tabla periodica
- 2. La tabla periódica O Desde finales del siglo XVIII, en la época de Lavoisier y Berzelius, la química comenzaba a renacer, partiendo de sus raíces alquimistas. A los 9 elementos químicos conocidos hasta la edad media , se descubrieron y agregaron a lo menos 40 elementos más. Desde ese momento se intentó clasificar los elementos químicos buscando semejanzas en su propiedades
- 3. Clasificación de los elementos químicos Por muchos años, y a medida que se descubrían nuevos elementos, los científicos los han ido agrupando y ordenando de acuerdo a determinadas propiedades comunes y han obtenido uno de los hitos más notables del siglo XX: La tabla periódica
- 4. O Históricamente, existen cuatro formas en las que se clasificaron los elementos químicos: O Metales y no metales O Las triadas O Las Octavas O La tabla Periódica actual
- 5. Tabla periódica actual La tabla periódica actual fue confeccionada por el ruso Dimitri Mendeleiev y el alemán Lothar Meyer. Consta en la actualidad con 120 elementos químicos naturales y artificiales. Está constituida por 18 líneas verticales (columnas) llamadas gruposgrupos y por 9 líneas horizontales (filas) que conforman 7 periodos.
- 6. Grupos y periodos. O Grupos: Son columnas que se designan con números romanos y las letras A y B o bien los números del 1 al 18. Los elementos que forman un grupo tienen en común la cantidad de electrones de valencia; es decir, los electrones del último nivel de energía.
- 8. O Períodos: son filas que se designan con los números del 1 al 7,constituyendo dos periodos que se encuentran debajo de la tabla periódica que corresponden a los actínidos y los lantánidos. O Los elementos químicos se pueden clasificar según su carácter metálico y de acuerdo con su configuración electrónica.
- 11. Según su carácter metálico Metales No Metales O Son brillantes O Son conductores del calor y la electricidad O Son sólidos excepto el Ga y el Hg O Son dúctiles y maleables O Son opacos O Son aislantes del calor y la electricidad O Pueden estar sólidos, líquidos o gaseosos O Son frágiles
- 12. Metaloides También se denominan semimetales o anfóteros. Son elementos químicos que se pueden comportar como metales o no metales, sus propiedades físicas son similares a las de los metales y las químicas a la de los no metales. Estos elementos son Boro, Silicio, Germanio, Arsénico, Antimonio, teluro, Polonio y Astato.
- 14. Según su configuración electrónica Representativos: Son elementos que tienen orbitales s y s-p en su último nivel de energía E. De Transición: Son elementos que tienen orbitales d y f en su último nivel de energía. Gases Nobles: Tienen todos sus orbitales completos
