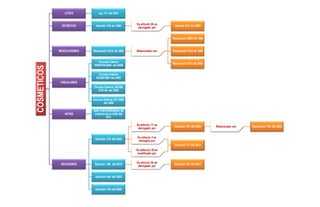
El documento resume la normatividad colombiana relacionada con los cosméticos, incluyendo leyes, decretos, resoluciones, circulares y actas. Describe las diferentes disposiciones legales que regulan aspectos como la fabricación, importación, comercialización y control de calidad de los productos cosméticos. También presenta los organismos encargados de la vigilancia y control de estos productos en Colombia.