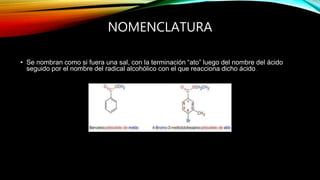
Este documento describe las propiedades y usos de dos grupos funcionales: ésteres y aminas. Los ésteres se forman por la unión de ácidos con alcoholes, generando agua. Pueden ser líquidos volátiles o sólidos cristalinos. Se hidrolizan en condiciones ácidas o alcalinas para regenerar el alcohol y el ácido. Se usan comúnmente en esencias de frutas, perfumes y antisépticos. Las aminas contienen uno o más radicales alcohólicos o aromáticos en