Estructura atómica y enlace. 4º de ESO. Diversificación
•Descargar como DOCX, PDF•
0 recomendaciones•17 vistas
resumen de estructura atómica y enlace
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Recomendados
Más contenido relacionado
Similar a Estructura atómica y enlace. 4º de ESO. Diversificación
Similar a Estructura atómica y enlace. 4º de ESO. Diversificación (20)
Principios de quimica y estructura ena3 - ejercicio 04 configuracion elect...

Principios de quimica y estructura ena3 - ejercicio 04 configuracion elect...
Números-cuánticos-y-configuración-electrónica-PSU (1).pdf

Números-cuánticos-y-configuración-electrónica-PSU (1).pdf
Diapositivas c08 relaciones_periodicas_entre_los_elementos

Diapositivas c08 relaciones_periodicas_entre_los_elementos
3. Cap 1 Algunas Propiedades Periódicas Clase de 12 abril 2018-2.pdf

3. Cap 1 Algunas Propiedades Periódicas Clase de 12 abril 2018-2.pdf
Último
Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels patrons de la plujaRealitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...

Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...Pere Miquel Rosselló Espases
Último (20)
tema 6 2eso 2024. Ciencias Sociales. El final de la Edad Media en la Penínsul...

tema 6 2eso 2024. Ciencias Sociales. El final de la Edad Media en la Penínsul...
Época colonial: vestimenta, costumbres y juegos de la época

Época colonial: vestimenta, costumbres y juegos de la época
El liderazgo en la empresa sostenible, introducción, definición y ejemplo.

El liderazgo en la empresa sostenible, introducción, definición y ejemplo.
MINEDU BASES JUEGOS ESCOLARES DEPORTIVOS PARADEPORTIVOS 2024.docx

MINEDU BASES JUEGOS ESCOLARES DEPORTIVOS PARADEPORTIVOS 2024.docx
SESION DE APRENDIZAJE PARA3ER GRADO -EL SISTEMA DIGESTIVO

SESION DE APRENDIZAJE PARA3ER GRADO -EL SISTEMA DIGESTIVO
Evaluación de los Factores Externos de la Organización.

Evaluación de los Factores Externos de la Organización.
04.UNIDAD DE APRENDIZAJE III CICLO-Cuidamos nuestro medioambiente (1).docx

04.UNIDAD DE APRENDIZAJE III CICLO-Cuidamos nuestro medioambiente (1).docx
PLAN LECTOR QUINTO 2023 educación primaria de menores Quinto grado

PLAN LECTOR QUINTO 2023 educación primaria de menores Quinto grado
Lecciones 07 Esc. Sabática. Motivados por la esperanza

Lecciones 07 Esc. Sabática. Motivados por la esperanza
POEMAS ILUSTRADOS DE LUÍSA VILLALTA. Elaborados polos alumnos de 4º PDC do IE...

POEMAS ILUSTRADOS DE LUÍSA VILLALTA. Elaborados polos alumnos de 4º PDC do IE...
Bitacora de Inteligencia Artificial y Herramientas Digitales HD4 Ccesa007.pdf

Bitacora de Inteligencia Artificial y Herramientas Digitales HD4 Ccesa007.pdf
DISEÑO DE ESTRATEGIAS EN MOMENTOS DE INCERTIDUMBRE.pdf

DISEÑO DE ESTRATEGIAS EN MOMENTOS DE INCERTIDUMBRE.pdf
cuadernillo_cuentos_de_los_valores_elprofe20 (1).docx

cuadernillo_cuentos_de_los_valores_elprofe20 (1).docx
Lineamientos de la Escuela de la Confianza SJA Ccesa.pptx

Lineamientos de la Escuela de la Confianza SJA Ccesa.pptx
Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...

Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...
Estrategia Nacional de Refuerzo Escolar SJA Ccesa007.pdf

Estrategia Nacional de Refuerzo Escolar SJA Ccesa007.pdf
Estructura atómica y enlace. 4º de ESO. Diversificación
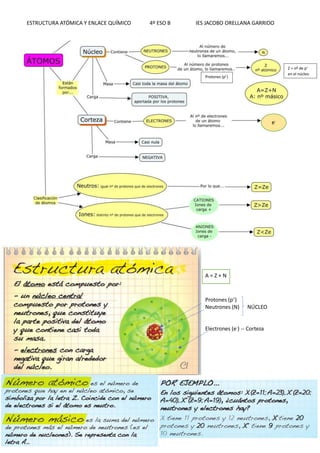
- 1. ESTRUCTURA ATÓMICA Y ENLACE QUÍMICO 4º ESO B IES JACOBO ORELLANA GARRIDO A = Z + N Protones (p+ ) Neutrones (N) NÚCLEO Electrones (e- ) -- Corteza Protones (p+) Z = nº de p+ en el núcleo e-
- 2. ESTRUCTURA ATÓMICA Y ENLACE QUÍMICO 4º ESO B IES JACOBO ORELLANA GARRIDO SI PIERDE e- -- SE TRANSFORMA EN IÓN POSITIVO EJEMPLO: (CATIÓN) 12 6C (Z = 6; N = 6; A =12) 14 6C (Z = 6; N = 8; A =14) SI GANA e- -- SE TRANSFORMA EN IÓN NEGATIVO (ANIÓN) NUNCA PUEDEN PERDER PROTONES (p+ ) METALES No Metales
- 3. ESTRUCTURA ATÓMICA Y ENLACE QUÍMICO 4º ESO B IES JACOBO ORELLANA GARRIDO ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO
- 4. ESTRUCTURA ATÓMICA Y ENLACE QUÍMICO 4º ESO B IES JACOBO ORELLANA GARRIDO PASOS PARA CONOCER LA FÓRMULA DE LOS COMPUESTOS QUE SE FORMAN CUANDO SE UNEN POR ENLACE QUÍMICO 1. IDENTIFICAR A QUÉ GRUPO DE ELEMENTOS PERTENECE (METAL, NO METAL, GAS NOBLE) 2. IDENTIFICAR EL TIPO DE ENLACE QUE SE DA ENTRE ESOS ELEMENTOS. METAL + NO METAL (ENLACE IÓNICO) NO METAL + NO METAL (ENLACE COVALENTE) METAL + METAL (ENLACE METÁLICO) 3. DETERMINAR EL Nº ATÓMICO (Z = Nº p+ ) DE LOS ELEMENTOS EN LA TABLA PERIÓDICA. ESTE Nº COINCIDE CON EL Nº DE ELECTRONES (e- ) EN LOS ELEMENTOS NEUTROS. 4. REALIZAR CONFIGURACIÓN ELECTRÓNICA (repartir los e- ) EN LOS DISTINTOS NIVELES SEGÚN LA REGLA n2 * 2 n = nivel nivel 1 n= 1 12 * 2 = 2 e- (máx) nivel 2 n = 2 22 * 2 = 8 e- (máx) nivel 3 n = 3 32 * 2 = 18 e- (máx) . . . 5. DETERMINAR EL Nº DE e- (máx) QUE CADA ELEMENTO TIENE QUE DAR, RECIBIR O SOLTAR PARA TENER 8 e- EN SU ÚLTIMA CAPA COMO LOS GASES NOBLES (REGLA DEL OCTETO). ¡CUIDADO! SI NO PUEDO DAR O SOLTAR e- NECESARIOS PARA TENER 8 e- EN LA ÚLTIMA CAPA, TAMBIEN PUEDO QUEDARME CON 2 e- COMO EL HELIO (He). Si es ENLACE IÓNICO, el METAL DA los electrones necesarios para parecerse a los gases nobles y el NO METAL RECIBE también los electrones necesarios. Si es ENLACE COVALENTE, los NO METALES, solo COMPARTEN tantos electrones como le hagan falta. Si es ENLACE METÁLICO, los METALES SUELTAN los electrones necesarios para parecerse a los gases nobles.
