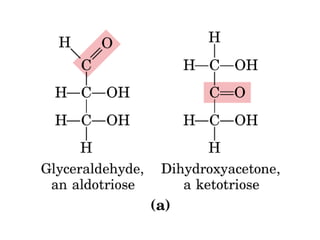
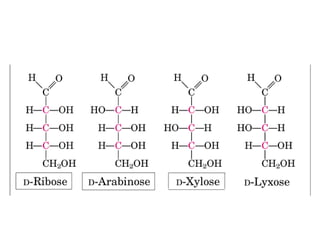
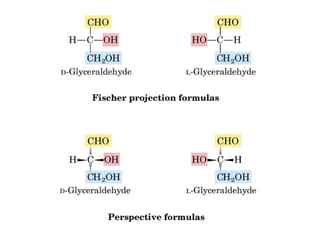
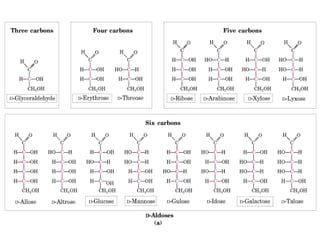
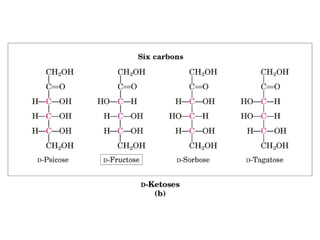
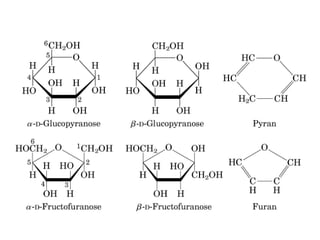
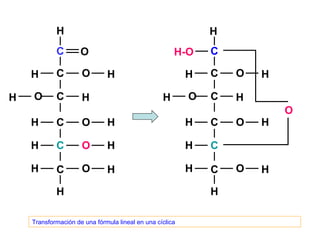
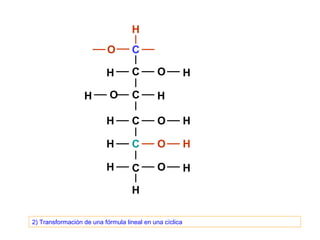
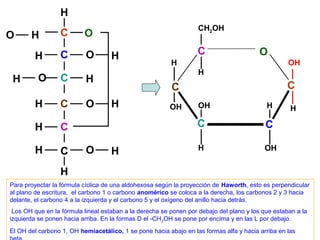
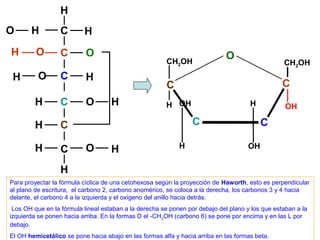
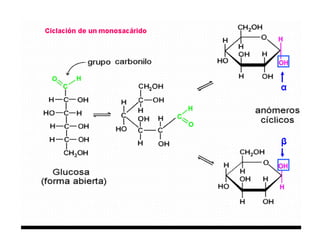
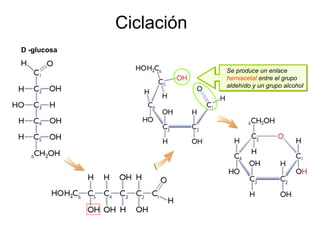
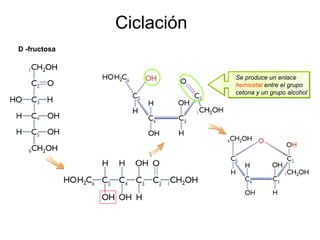
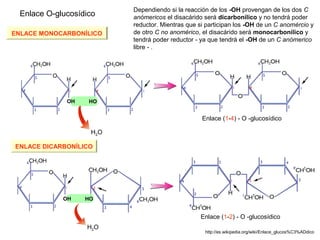
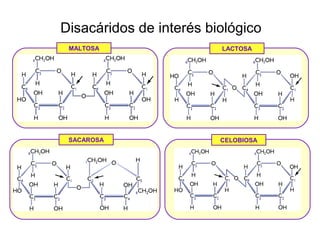
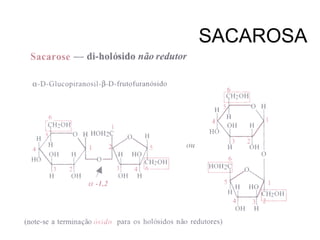
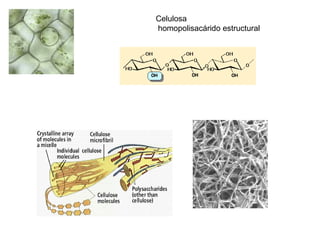
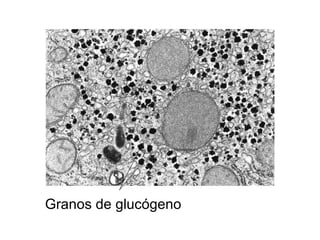
Este documento describe los carbohidratos o glúcidos, incluyendo su clasificación, estructura y funciones. Explica que los monosacáridos como la glucosa forman estructuras cíclicas en disolución. También cubre los disacáridos como la sacarosa y lactosa, así como los polisacáridos de reserva como el almidón y glucógeno y los polisacáridos estructurales como la celulosa y quitina.