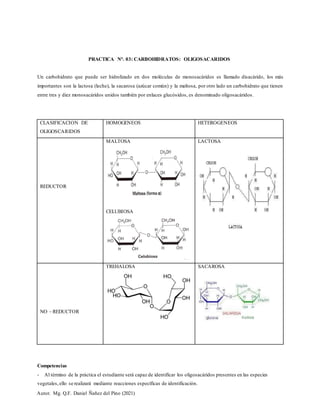
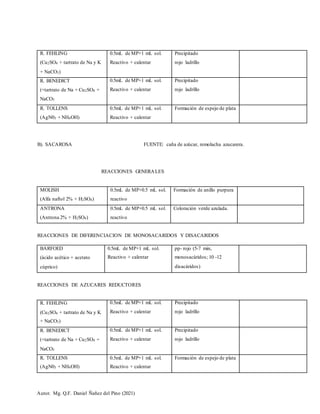
Este documento presenta los procedimientos para identificar oligosacáridos como la lactosa, sacarosa y maltosa mediante reacciones químicas específicas. Explica cómo realizar las reacciones de Molish, Antrona, Barfoed, Fehling, Benedict y Tollens para determinar la presencia de azúcares reductores y no reductores. También describe el método cuantitativo de Fehling para medir la cantidad de azúcar reductor en una muestra e incluye preguntas sobre oligosacáridos y cromatograf