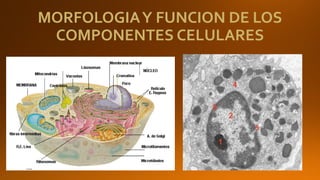
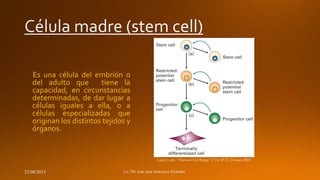
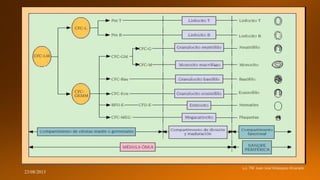
El documento describe el proceso de hematopoyesis, que incluye la producción, diferenciación y maduración de las células sanguíneas a partir de células madre hematopoyéticas en la médula ósea. Explica que existen cuatro compartimentos celulares en función del grado de maduración, dominados por las células madre hematopoyéticas, progenitores y precursores que dan lugar a las células sanguíneas maduras a través de la eritropoyesis, trombopoyesis y leucopoyesis. También detalla los