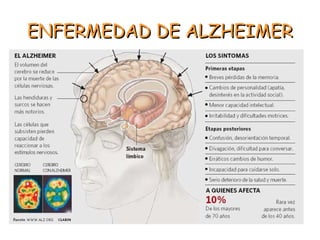
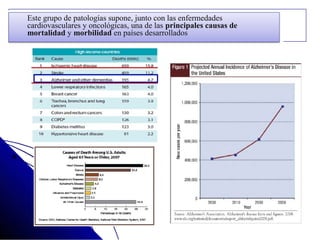
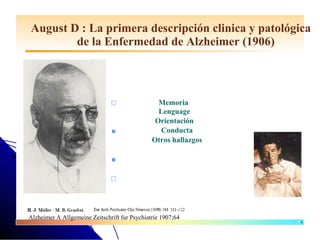
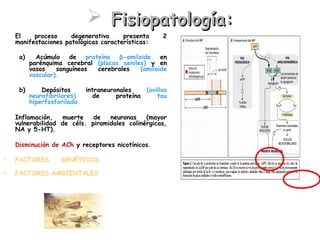
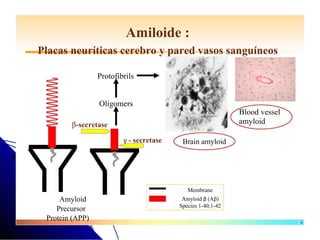
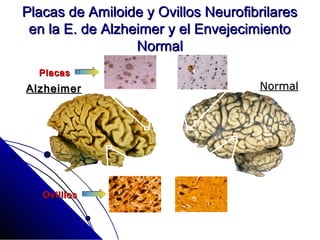
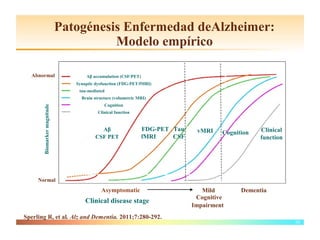
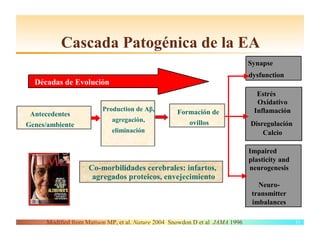
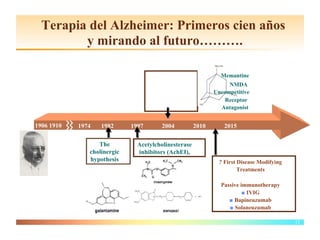
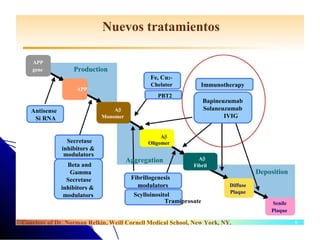
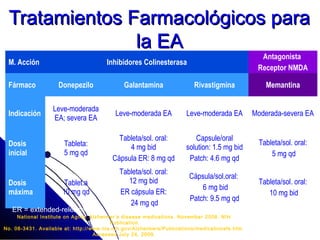
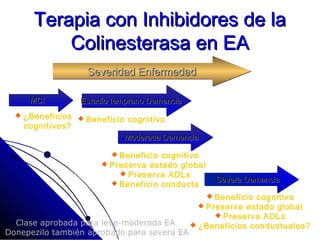
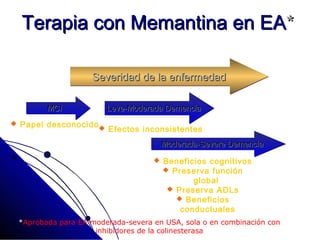
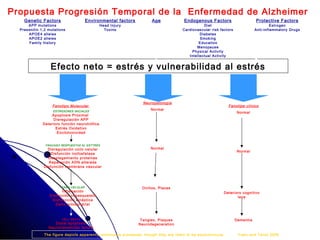
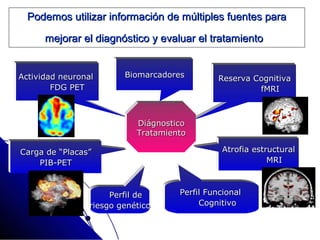
El documento detalla las características, factores de riesgo y tratamiento de la enfermedad de Alzheimer, que es una forma principal de demencia neurodegenerativa. Se describen terapias actuales y potenciales, incluyendo farmacológicas y modificadoras de la enfermedad, así como los objetivos del tratamiento, que incluyen la mejora cognitiva y funcional y el retraso en la progresión de la enfermedad. Además, se enfatiza la importancia del diagnóstico temprano y la integración de biomarcadores para una mejor práctica clínica.