PRESENTACION_DE_BUDD_CHIARI.ppt
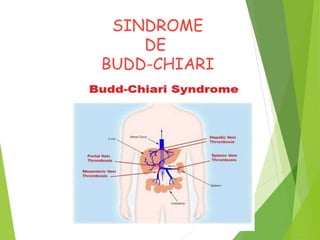
- 2. SINDROME DE BUDD- CHIARI Enfermedad muy rara, caracterizada por la obstrucción de las venas suprahepáticas o de la cava inferior. La consecuencia de esta obstrucción venosa es el aumento de la presión hidrostática en los sinusoides hepáticos que, si es lo suficientemente intensa, ocasionará una necrosis hepatocitaria hemorrágica alrededor de la vena centrolobulillar.
- 3. En caso de persistencia del proceso obstructivo, en estas zonas de necrosis aparecerán zonas de fibrosis cicatrizal uniendo las venas centrolobulillares entre sí o la vena centrolobulillar con la vena porta, pudiendo llegar a producir una cirrosis Descrita por primera vez por Budd en 1885 y posteriormente en 1889 por Chiari Es más frecuente en mujeres jóvenes y se estima una prevalencia de 2,4 casos por millón
- 4. En la mitad de los casos se desconoce las causas de la enfermedad De entre las causas conocidas, la más frecuente es la trombosis de las venas suprahepáticas por síndrome de hipercoagulabilidad
- 6. PRESENTACIÓN CLÍNICA Clínicamente, el síndrome de Budd Chiari se presenta en la mayoría de casos como un cuadro de inicio súbito consistente en dolor abdominal, ascitis y hepatomegalia Se distinguen formas clínicas: una subaguda, crónica y otra fulminante. La forma subaguda, la más frecuente, es de comienzo brusco y se caracteriza por hepatomegalia dolorosa, dolor abdominal, vómitos y ascitis, se pueden objetivar signos de hipertensión portal como esplenomegalia y varices esofágicas que pueden sangrar.
- 7. También puede existir un derrame pleural que puede ser hemorrágico. Aumento de las transaminasas, hiperbilirrubinemia y descenso en el tiempo de protrombina se produce en un período de tiempo más prolongado que suele oscilar entre 2 semanas y 6 meses. La forma crónica el dato clínico más característico es la existencia de una ascitis rica en proteínas, de difícil tratamiento. Estos enfermos también presentan esplenomegalia y varices esofágicas. En esta fase, la biopsia hepática evidencia un parénquima hepático con importante alteración de la estructura por banda de fibrosis que unen las venas centrolobulillares
- 8. La forma fulminante es una forma clínica muy infrecuente (menos del 5%) que puede aparecer cuando la obstrucción es rápida y extensa, produciéndose una intensa necrosis hepática, puede aparecer en pacientes que al no recibir un tratamiento adecuado, habitualmente mediante anticoagulación, sufren fenómenos de retrombosis de las venas suprahepáticas que pueden provocar que un paciente, con una forma más o menos controlada de síndrome de Budd-Chiari, pueda presentar un brusco deterioro clínico.
- 9. • La clínica se inicia con dolor abdominal, vómitos, hepatomegalia dolorosa de brusca aparición, con una elevación importante de las transaminasas, ictericia, ascitis y signos de insuficiencia hepática aguda grave, con encefalopatía, insuficiencia renal y muerte.
- 10. PATOGÉNESIS El evento fisiopatológico inicial en el SBC es la obstrucción del flujo venoso comprendido entre las vénulas hepáticas y el segmento suprahepático de la vena cava inferior. La obstrucción de una sola vena hepática no es suficiente para la manifestación del síndrome, de modo que las dos venas deben estar obstruidas La consecuencia de esta obstrucción es una alteración hemodinámica compleja que incluye el aumento de la presión hidrostática capilar portal, que altera los gradientes de presión vascular
- 11. Los resultados de estos cambios hemodinámicos son la dilatación sinusoidal y la fuga de líquido al espacio intersticial, la cual pasa a través de la cápsula hepática cuando excede la capacidad de drenaje linfático En conclusión, la presión portal aumenta y la perfusión hepática por esta vía disminuye, produciendo un daño hipóxico celular
- 12. Manifestaciones asociadas a la hipertensión portal 1. Circulación colateral : 2. Hemorragia digestiva: RED VENOSA ABDOMINAL HEMORROIDES VARICES ESOFÁGICAS ROTURA DE VARICES ESOFÁGOGÁSTRICAS GASTROPATÍA DE LA HIPERTENSIÓN PORTAL ULCUS DUODENAL
- 13. 3. Encefalopatía hepática portosistémica 4. Hiperesplenismo 5. Retención hidrosalina: ASCITIS EDEMAS HIDROTÓRAX
- 14. DIAGNOSTICO El diagnóstico de sospecha es clínico: El SBC debe sospecharse en las siguientes situaciones: A. En un paciente con ascitis y hepatomegalia dolorosa. B. Ante una hepatopatía con ascitis intratable y solo leve alteración de la función hepática. C. En un fallo hepático agudo con hepatomegalia. D. Ante cualquier alteración hepática en pacientes con una enfermedad protrombótica de base.
- 15. Protocolo diagnóstico: el diagnóstico de certeza se establece mediante técnicas de imagen. La ultrasonografía asociada al doppler, suele establecer el diagnóstico y es la técnica de elección. Se recomienda confirmar el diagnóstico mediante otra prueba de imagen como el angioTAC o la angioRMN que ayudarán además a descartar procesos neoformativos. Es excepcional la necesidad de realizar flebografía o biopsia hepática para confirmar el diagnóstico; además de la medición de la presión venosa .
- 17. Laboratorio • Debe determinarse la función hepática por medio de los siguientes estudios de laboratorio: aminotransferasas, bilirrubinas, fosfatasa alcalina (FA), gammaglutamil transferasa (GGT), albúmina, pruebas de coagulación (TP, TPT), conteo de plaquetas. • En el SBC, las aminotransferasas usualmente se encuentran aumentadas hasta 5 veces el valor del límite superior, especialmente en las formas agudas y fulminantes, en esta última hay descenso en el tiempo de protrombina.
- 18. • Las bilirrubinas y la fosfatasa alcalina pueden elevarse igualmente; la albúmina sérica puede presentar una disminución moderada • El líquido ascítico es rico en proteínas (más de 20-30 g/l) y la celularidad es escasa. Cuando ésta es elevada se debe sospechar la existencia de una peritonitis bacteriana espontánea
- 20. Tratamiento inicial 1. Todos los pacientes, independientemente de los síntomas, han de recibir tratamiento anticoagulante de forma precoz y de modo indefinido para prevenir la aparición de nuevas lesiones trombóticas. Habitualmente se utiliza acenocumarol o warfarina, por la comodidad de su administración oral, para mantener un cociente internacional normalizado (INR) entre 2,5 y 3,5.
- 21. 2. Si el diagnóstico de SBC se realiza en las primeras 72 horas, puede intentarse la repermeabilización con agentes trombolíticos, como el activador tisular del plasminógeno, urocinasa o estreptocinasa. Esta opción está contraindicada en los pacientes con una enfermedad potencialmente hemorrágica o en los que se ha realizado un procedimiento invasivo, incluso paracentesis en las 24 horas previas. La experiencia con esta técnica es mínima y los resultados dispares. Las complicaciones de la trombolisis pueden ser fatales
- 22. 3. En el pequeño subgrupo de pacientes con SBC por estenosis segmentarias parciales y cortas de las venas suprahepáticas, está indicada la angioplastia para intentar corregir la estenosis y reestablecer con ello el drenaje fisiológico de las venas suprahepáticas. La mayor limitación es el desarrollo de reestenosis que obliga a la realización de sucesivas angioplastias. Para evitarlas se puede colocar una prótesis o reservar esta medida para estenosis recurrentes. La colocación incorrecta puede complicar la posterior realización de una anastomosis portosistémica o de un trasplante, por lo que debe realizarse por personal entrenado
- 23. 4. Una vez iniciado el tratamiento médico (anticoagulación, diuréticos…), debe llevarse a cabo un estrecho seguimiento (semanalmente el primer mes) para definir la mejoría o el deterioro clínico y un eventual cambio de tratamiento. 5. (Anastomosis Portosistémica Intrahepática Transyugular) El TIPS es un tratamiento muy útil, cuando el tratamiento médico ha fracasado y muestra una menor morbimortalidad que la cirugía. es factible en la mayoría de los pacientes con obstrucción o estenosis severa de la vena cava inferior (VCI)
- 24. 6. Si el TIPS no logra mejorar la condición clínica del paciente, debe indicarse un trasplante hepático ortotópico (THO). La supervivencia a largo plazo es similar a la de los trasplantados por otras causas. La aplicación de esta estrategia terapéutica escalonada proporciona una excelente supervivencia. En una serie reciente la supervivencia al año y 5 años fue del 88 y 74% respectivamente.
- 25. Dejada a su evolución espontánea el síndrome de Budd Chiari tiene una evolución mortal en semanas o meses, pero el diagnóstico y tratamiento precoz consiguen aumentar la supervivencia a largo plazo