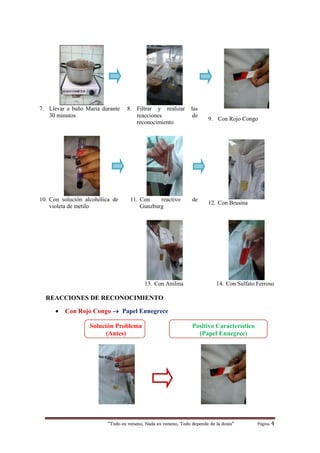
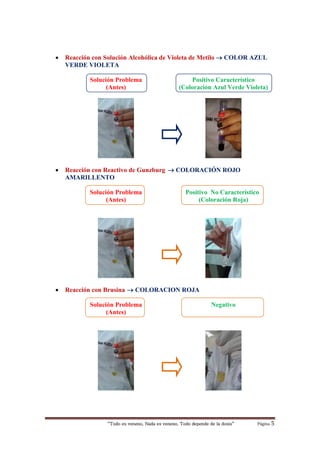
Este documento describe un experimento en el que se administró ácido nítrico a una rata por vía intraperitoneal. La rata mostró síntomas de dolor, vómito y hemorragia gástrica, y murió en 4 minutos. Se realizaron pruebas de reconocimiento que confirmaron la presencia de ácido nítrico. El documento concluye que el ácido nítrico es altamente tóxico y letal a una dosis de 10 ml, y que las pruebas de reconocimiento son necesarias para verificar una intoxicación por este comp