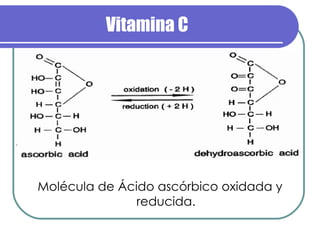
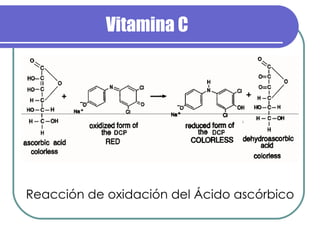
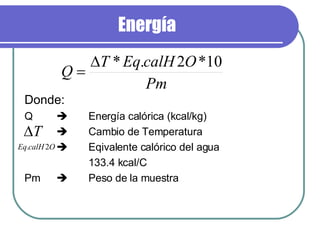
La vitamina C es un compuesto blanco soluble en agua llamado ácido ascórbico. Es esencial para los humanos pero no puede ser sintetizado por el cuerpo. Se oxida fácilmente en soluciones básicas o neutrales, perdiendo átomos de hidrógeno. El método de Tillmans se usa para detectar ácido ascórbico mediante la titulación de oxidación-reducción con 2,6-dicloroindofenol.