P2 qa
•Descargar como PPTX, PDF•
0 recomendaciones•25 vistas
Coeficiente de expansion térmica de los gases
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Recomendados
S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...

S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...CristianQuispeCerron
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
EL ESTADO GASEOSO: GASES REALES E IDEALES Y PRESION, TEMPERATURA Y VOLUMEN

EL ESTADO GASEOSO: GASES REALES E IDEALES Y PRESION, TEMPERATURA Y VOLUMEN
Principios de quimica y estructura ena2 - ejercicio 03 cambio de la p de u...

Principios de quimica y estructura ena2 - ejercicio 03 cambio de la p de u...
Similar a P2 qa
S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...

S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...CristianQuispeCerron
Similar a P2 qa (20)
S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...

S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...
VI-GASES IDEALES Y REALES, de la Universidad Nacional de Ingeniria

VI-GASES IDEALES Y REALES, de la Universidad Nacional de Ingeniria
Equilibrio termico - Estructura de la Materia y Ondas 

Equilibrio termico - Estructura de la Materia y Ondas
Más de Ramses CF
Más de Ramses CF (20)
Actividad 1.3 Tasa de crecimiento anual compuesta y divisas

Actividad 1.3 Tasa de crecimiento anual compuesta y divisas
Diagrama sinóptico ACT: 14 Descripción: Realiza un diagrama sinóptico de los ...

Diagrama sinóptico ACT: 14 Descripción: Realiza un diagrama sinóptico de los ...
INNOVACION SC LIMITS BAHIAS . ASPECTOS JURIDICOS SC LIMITS EFICIENTA TU DES...

INNOVACION SC LIMITS BAHIAS . ASPECTOS JURIDICOS SC LIMITS EFICIENTA TU DES...
CuadroComparativo Herramientas básicas de la Calidad Cuadro comparativo” Cult...

CuadroComparativo Herramientas básicas de la Calidad Cuadro comparativo” Cult...
trabajo taller de investigacionPropuesta de capacitación mediante cursos al p...

trabajo taller de investigacionPropuesta de capacitación mediante cursos al p...
El-impacto-de-la-integridad-académica-en-la-educación ensayo

El-impacto-de-la-integridad-académica-en-la-educación ensayo
Ensayo3 Legislación Aduanera Marco Jurídico del Comercio Exterior (informaci...

Ensayo3 Legislación Aduanera Marco Jurídico del Comercio Exterior (informaci...
Normatividad Ecológica en el Tránsito y Tráfico de Mercancías

Normatividad Ecológica en el Tránsito y Tráfico de Mercancías
Tercera etapa del proyecto Cultivo y Venta de hortalizas orgánicas (lechuga) ...

Tercera etapa del proyecto Cultivo y Venta de hortalizas orgánicas (lechuga) ...
Último
Último (20)
TEXTO UNICO DE LA LEY-DE-CONTRATACIONES-ESTADO.pdf

TEXTO UNICO DE LA LEY-DE-CONTRATACIONES-ESTADO.pdf
Reporte de simulación de flujo del agua en un volumen de control MNVA.pdf

Reporte de simulación de flujo del agua en un volumen de control MNVA.pdf
osciloscopios Mediciones Electricas ingenieria.pdf

osciloscopios Mediciones Electricas ingenieria.pdf
MODIFICADO - CAPITULO II DISEÑO SISMORRESISTENTE DE VIGAS Y COLUMNAS.pdf

MODIFICADO - CAPITULO II DISEÑO SISMORRESISTENTE DE VIGAS Y COLUMNAS.pdf
Controladores Lógicos Programables Usos y Ventajas

Controladores Lógicos Programables Usos y Ventajas
Voladura Controlada Sobrexcavación (como se lleva a cabo una voladura)

Voladura Controlada Sobrexcavación (como se lleva a cabo una voladura)
NTP- Determinación de Cloruros en suelos y agregados (1) (1).pptx

NTP- Determinación de Cloruros en suelos y agregados (1) (1).pptx
Propuesta para la creación de un Centro de Innovación para la Refundación ...

Propuesta para la creación de un Centro de Innovación para la Refundación ...
04. Sistema de fuerzas equivalentes II - UCV 2024 II.pdf

04. Sistema de fuerzas equivalentes II - UCV 2024 II.pdf
ANALISIS Y DISEÑO POR VIENTO, DE EDIFICIOS ALTOS, SEGUN ASCE-2016, LAURA RAMIREZ

ANALISIS Y DISEÑO POR VIENTO, DE EDIFICIOS ALTOS, SEGUN ASCE-2016, LAURA RAMIREZ
Procesos-de-la-Industria-Alimentaria-Envasado-en-la-Produccion-de-Alimentos.pptx

Procesos-de-la-Industria-Alimentaria-Envasado-en-la-Produccion-de-Alimentos.pptx
P2 qa
- 1. COEFICIENTE DE EXPANSIÓN TÉRMICA DE LOS GASES PRÁCTICA #2
- 2. Propiedades Empíricas de los Gases De los tres estados de agregación, sólo el estado gaseoso permite una descripción cuantitativa relativamente sencilla. Limitaremos la descripción a las relaciones entre propiedades tales como masa, presión volumen y temperatura. Un sistema está en equilibrio si los valores de las propiedades no cambian con el tiempo.
- 3. Un sistema se encuentra en estado o condición definidos cuando todas sus propiedades tienen valores definidos determinados por el estado del sistema. La ecuación de estado del sistema es la relación matemática que existe entre los valores de las cuatro propiedades mencionadas anteriormente.
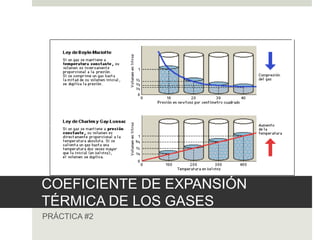
- 4. En 1662, Robert Boyle realizó las primeras medidas cuantitativas del comportamiento de los gases en relación con la presión y el volumen. 𝑝𝛼 1 𝑉 𝑝𝑉 = 𝐶 𝑝1 𝑉1 = 𝑝2 𝑉2
- 5. Posteriores experimentos de Charles demostraron que la constante C es una función de la temperatura. Gay-Lussac hizo medidas del volumen de una masa fina de gas bajo presión constante y encontró que el volumen era una función lineal de la temperatura. 𝑉𝛼𝑇 𝑉/𝑇 = 𝐶 𝑉1/𝑇1 = 𝑉2/𝑇2 𝑉 = 𝑎 + 𝑏𝑡
- 7. 0 5 10 15 20 25 30 35 -20 0 100 V(dm3) t (ºC) V0
- 8. Los experimentos de Charles demostraron que, para una masa fija de gas bajo una presión constante, el aumento relativo de volumen para cada aumento de un grado de temperatura era el mismo para todos los gases con los cuales él experimentó. V = V0 + ¶V ¶t æ è ç ö ø ÷ p t
- 9. El aumento relativo en volumen por grado a 0ªC es: Esta cantidad es el coeficiente de expansión térmica a 0ºC, para el cual empleamos el símbolo α0. a0 = 1 V0 ¶V ¶t æ è ç ö ø ÷ p V = V0 1+aT( ) V = V0aT +V0
- 10. m =V0a = ba a = m b
- 11. Montar e instalar equipo Registrar temperatura Fijar un Δh=0 Registrar altura columna de aire Encender baño y fijar 30ºC con botón pequeño Girar perilla grande a 30ºC Esperar a que se estabilice la temp y anotar altura columna de aire Repita pasos anteriores hasta obtener cinco lecturas
- 12. Tabla de Resultados Longitud de la columna de aire (cm) Volumen de aire (cm3 o ml) Temperatura (ºC)