Química Bloque V
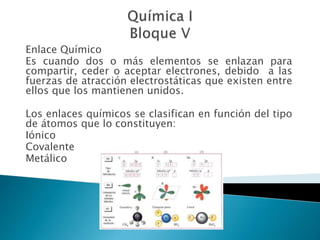
- 1. Enlace Químico Es cuando dos o más elementos se enlazan para compartir, ceder o aceptar electrones, debido a las fuerzas de atracción electrostáticas que existen entre ellos que los mantienen unidos. Los enlaces químicos se clasifican en función del tipo de átomos que lo constituyen: Iónico Covalente Metálico
- 2. La tendencia de los iones de los elementos del sistema perídico es completar sus últimos niveles de energía con una cantidad de 8 electrones de tal forma que adquiere una configuración muy estable.
- 3. Es la fuerza de atracción entre iones de carga opuesta que los mantiene unidos en un compuesto iónico. Constitución De acuerdo a sus electronegatividad, esta constituido por un metal y un no metal. Formación Se forma cuando uno o más electrones se transfieren de un átomo a otro.
- 4. Propiedades • La atracción entre iones es muy fuerte, lo que hace difícil separarlos. • Son sólidos a temperatura ambiente • Poseen gran dureza • Son solubles en disolventes polares como el agua • Son buenos conductores cuando son fundidos o en soluciones acuosas.
- 5. El enlace covalente se forma cuando la diferencia de electronegatividad no es suficiente como para que se efectúe una transferencia de electrones. Los compuestos son covalentes cuando su porcentaje de electrovalencia es menor de 50%.
- 6. Están constituidos por átomos de baja electronegatividad, y consiste en iones con carga positiva en la que los electrones de valencia débilmente sujetos. Las aplicaciones dependerá si se usa el metal en estado puro o en aleación. Propiedades Maleabilidad, ductibilidad, alta conductividad eléctrica y térmica, punto de fusión y ebullición altas, presentan brillo metálico e insolubles en agua y otros solventes.
- 7. Son el conjunto de fuerzas que mantienen unidas a las moléculas como consecuencia de la polaridad que poseen. Son las responsables del comportamiento no ideal de los gases y ejercen aún más influencia en las fases condensadas de la materia, es decir, en los líquidos y los sólidos.
- 8. Fuerzas de Van der Waals Son fuerzas de estabilización molecular; forman un enlace químico no covalente en el que participan dos tipos de fuerzas o interacciones, las de dispersión y las de repulsión. Esta se divide en: Fuerzas dipolo-dipolo (Puentes de hidrógeno) Fuerzas dipolo-dipolo incluido Fuerzas dipolo instantáneo-dipolo incluido. Fuerzas ión-ión Se establecen entre iones de igual o distinta carga, en donde, los iones con cargas de signo opuesto se atraen y los iones con carga del mismo se repelen.
- 9. Fuerzas ión-dipolo Es la atracción entre un ión y el extremo de una molécula polar y depende del tamaño del ion y la magnitud del dipolo. Fuerzas ión-dipolo incluido Se presenta entre un ión y una molécula apolar. La cercanía del ión provoca una distorsión en la nube electrónica de la molécula apolar que la convierte de modo transitorio en una molécula polarizada. En este momento se produce una atracción entre el ión y la molécula polarizada.
- 10. Fuerzas Hidrofóbicas Son fuerzas que mantienen juntas las regiones apolares de las molecular, en un medio acuoso; tienden a asociarse porque evitan interaccionar con el agua, lo hace por razones termodinámicas y se asocian para reducir el número de moléculas de agua que puedan estar en contacto con las moléculas hidrofóbicas.
- 11. Cubre el 72% de la superficie del planeta y representa entre el 50% y el 90% de la masa de los seres vivos; se puede encontrar en cualquier lugar de la biósfera y en sus tres estados de agregación de la materia, sólido, líquido y gaseoso. Es fundamental para todas las formas de vida conocidas; el 3% de su volumen es dulce, del cual el 1% es líquido y el 2% se encuentra formado en casquetes polares.
- 12. Es inodora, incolora e insípida. Su punto de ebullición es de 100ª C y congelación cero grados Celsius. Tiene una densidad de 1 gr/cm₃ Posee una tensión superficial muy elevada. Posee un calor específico de 1 cal/ªC gr. Se le considera como un disolvente universal No conduce la electricidad el agua pura.