Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Recomendados
Proyecto Integrador. Experimentando con las Leyes de los Gases. Módulo 12

Proyecto Integrador. Experimentando con las Leyes de los Gases. Módulo 12María Guadalupe Serrano Briseño
Más contenido relacionado
La actualidad más candente
Proyecto Integrador. Experimentando con las Leyes de los Gases. Módulo 12

Proyecto Integrador. Experimentando con las Leyes de los Gases. Módulo 12María Guadalupe Serrano Briseño
La actualidad más candente (20)
Actividad Integradora. Una Ley de los Gases. Módulo 12

Actividad Integradora. Una Ley de los Gases. Módulo 12
Proyecto Integrador. Experimentando con las Leyes de los Gases. Módulo 12

Proyecto Integrador. Experimentando con las Leyes de los Gases. Módulo 12
Similar a Resumen tema 5
Similar a Resumen tema 5 (20)
Más de José Miranda
Más de José Miranda (20)
Último
Último (20)
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
ACERTIJO DE POSICIÓN DE CORREDORES EN LA OLIMPIADA. Por JAVIER SOLIS NOYOLA

ACERTIJO DE POSICIÓN DE CORREDORES EN LA OLIMPIADA. Por JAVIER SOLIS NOYOLA
Tema 8.- PROTECCION DE LOS SISTEMAS DE INFORMACIÓN.pdf

Tema 8.- PROTECCION DE LOS SISTEMAS DE INFORMACIÓN.pdf
TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx

TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx
LABERINTOS DE DISCIPLINAS DEL PENTATLÓN OLÍMPICO MODERNO. Por JAVIER SOLIS NO...

LABERINTOS DE DISCIPLINAS DEL PENTATLÓN OLÍMPICO MODERNO. Por JAVIER SOLIS NO...
plande accion dl aula de innovación pedagogica 2024.pdf

plande accion dl aula de innovación pedagogica 2024.pdf
GUIA DE CIRCUNFERENCIA Y ELIPSE UNDÉCIMO 2024.pdf

GUIA DE CIRCUNFERENCIA Y ELIPSE UNDÉCIMO 2024.pdf
ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...

ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...
TECNOLOGÍA FARMACEUTICA OPERACIONES UNITARIAS.pptx

TECNOLOGÍA FARMACEUTICA OPERACIONES UNITARIAS.pptx
Resumen tema 5
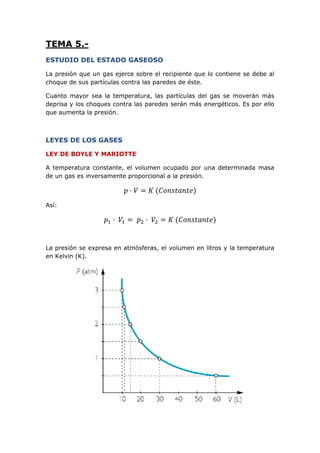
- 1. TEMA 5.- ESTUDIO DEL ESTADO GASEOSO La presión que un gas ejerce sobre el recipiente que lo contiene se debe al choque de sus partículas contra las paredes de éste. Cuanto mayor sea la temperatura, las partículas del gas se moverán más deprisa y los choques contra las paredes serán más energéticos. Es por ello que aumenta la presión. LEYES DE LOS GASES LEY DE BOYLE Y MARIOTTE A temperatura constante, el volumen ocupado por una determinada masa de un gas es inversamente proporcional a la presión. 𝑝 · 𝑉 = 𝐾 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) Así: 𝑝1 · 𝑉1 = 𝑝2 · 𝑉2 = 𝐾 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) La presión se expresa en atmósferas, el volumen en litros y la temperatura en Kelvin (K).
- 2. LEY DE CHARLES Y GAY-LUSSAC Si la presión de un gas permanece constante el volumen que ocupa una masa fija de gas es directamente proporcional a su temperatura absoluta. 𝑉 = 𝑘 · 𝑇 k es una constante de proporcionalidad. Así: 𝑉1 𝑇1 = 𝑉2 𝑇2 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) La presión se expresa en atmósferas, el volumen en litros y la temperatura en Kelvin (K). Si el volumen de un gas permanece constante, la presión que ejerce una masa fija de gas es directamente proporcional a su temperatura absoluta. 𝑝 = 𝑘 · 𝑇 k es una constante de proporcionalidad.
- 3. Así: 𝑝1 𝑇1 = 𝑝2 𝑇2 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) La presión se expresa en atmósferas, el volumen en litros y la temperatura en Kelvin (K). En el caso de que ninguna de las tres variables permanezca constante, la ecuación queda de la siguiente manera: 𝑝 · 𝑉 𝑇 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) Así: 𝑝1 · 𝑉1 𝑇1 = 𝑝2 · 𝑉2 𝑇2 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) LEY DE LOS GASES A partir de la ley de los gases podemos deducir las anteriores: 𝑝 · 𝑉 𝑇 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) 𝑠𝑖 𝑇 = 𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒: 𝑝 · 𝑉 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) 𝐿𝑒𝑦 𝑑𝑒 𝐵𝑜𝑦𝑙𝑒 − 𝑀𝑎𝑟𝑖𝑜𝑡𝑡𝑒 𝑠𝑖 𝑝 = 𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒: 𝑉 𝑇 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) 𝐿𝑒𝑦 𝑑𝑒 𝐶ℎ𝑎𝑟𝑙𝑒𝑠 𝑠𝑖 𝑉 = 𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒: 𝑝 𝑇 = 𝑘 (𝐶𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒) 𝐿𝑒𝑦 𝑑𝑒 𝐺𝑎𝑦 − 𝐿𝑢𝑠𝑠𝑎𝑐