cadena respiratoria
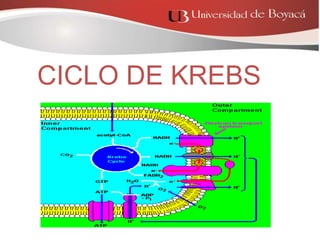
- 1. * CICLO DE KREBS * CICLO DEL ÁCIDO CÍTRICO CICLO DE KREBS
- 2. Algunas células obtienen su energía (ATP) a partir de la fermentación, degradando glucosa en ausencia de oxígeno. Para la mayoría de las células eucariotas y un gran número de bacterias que viven en condiciones aeróbicas y oxidan sus combustibles orgánicos a dióxido de carbono y agua. La glicólisis no es sino la primera etapa de la oxidación completa de la glucosa, el piruvato formado en la glicólisis en vez de ser reducido a lactato, etanol u otro producto de fermentación, sufre una oxidación mayor hasta CO2 y H2O. CICLO DE KREBS
- 3. FASE 01: PRODUCCION DEL ACETIL COa. FASE 02: OXIDACION DEL ACETILCOA. FASE 03: TRANSFERENCIA DE ELECTRONES Y FOSFORILACION OXIDATIVA CICLO DE KREBS
- 5. Matriz mitocondrial. La reacción del acetil CoA con el oxalacetato inicia el ciclo con la producción de citrato. En cada vuelta del ciclo se producen 2 de CO2 como productos de desecho, más 3 moléculas de NADH, 1 de GTP y 1 de FADH2 La energía que se almacena en los electrones fácilmente transferibles del NADH y del FADH2 será utilizada posteriormente para la producción de ATP mediante el proceso de fosforilación oxidativa. CICLO DE KREBS
- 6. CADENA RESPIRATORIA CADENA RESPIRATORIA 1.TRANSPORTE DE ELECTRONES 2. FOSFORILACION OXIDATIVA
- 7. La energía se obtiene metabólicamente en el proceso llamado cadena respiratoria oxidación de sustratos, produciendo agua y energía. Es realizada mediante una serie de enzimas que constituyen la cadena de transporte de electrones, en la que un grupo de compuestos son oxidados y reducidos alternativamente. CADENA RESPIRATORIA
- 8. • Es un conjunto de proteínas transportadoras de electrones situado en la membrana interna de la mitocondria, capaces de generar un gradiente electroquímico de protones para la síntesis de ATP. • Es un sistema multienzimático ligado a membrana interna mitocondrial que transfiere electrones desde moléculas orgánicas al oxígeno. • A ella llegan las moléculas reducidas: NADH+H+, FADH2, etc; las cuales han sido producidas en otras rutas metabólicas. CADENA RESPIRATORIA
- 9. • Es el aceptor final de los electrones que viajan por la cadena respiratoria, por lo tanto, la mayor parte del oxígeno que nosotros respiramos se usa para aceptar los electrones que pasan por la cadena respiratoria. • Después de que un átomo de oxígeno recibe dos electrones, éste reacciona con dos H+ y forma una molécula de agua. EL OXIGENO
- 10. La CTE comprende dos procesos: • Los electrones son transportados a lo largo de la membrana, de un complejo de proteínas transportador a otro. • Los protones son translocados a través de la membrana, estos significa que son pasados desde el interior o matriz hacia el espacio intermembranal. Esto construye un gradiente de protones. El O es el aceptor terminal de los electrones, combinándose con electrones e iones H+ para producir agua. CADENA RESPIRATORIA
- 11. FUNCIONES Producir energía a partir de Glúcidos, Lípidos y Proteínas. Transporta H+ y electrones a lo largo de la cadena y los conduce con el O2 para formar agua. Incorpora PO4 (fosforo inorgánico) como fuente de alta energía.
- 12. COMPONENTES DE LA CADENA RESPIRATORIA Los componentes de la cadena respiratoria son: Cinco grandes complejos proteicos con sus enzimas correspondientes. Un componente no proteico: UBIQUINONA (Q) que están embebidos en la membrana. Una pequeña proteína llamada CITOCROMO C que es periférica y se ubica en el espacio intermembranal, pero afdosado laxamente a la membrana interna.
- 13. 1. Mitocondria 2. Dinucleótidos 3. Moléculas transportadoras 4. ATP 5. ATPasa 6. Enzimas COMPONENTES DE LA CADENA RESPIRATORIA
- 14. 1. LA MITOCONDRIA • Membrana externa • Membrana interna • Espacio intermembrana • Matriz Organelo citoplasmático que se caracterizan por tener dos membranas: una externa permeable a la mayor parte de metabolitos, una interna con permeabilidad selectiva (moldeada en pliegues o crestas) y una matriz dentro de la membrana interna, formada por complejos enzimáticos, ATP, ADP, y algunos iones. La mitocondria es la fuente de energía de la célula, en su interior tiene lugar la captura de la energía derivada de la oxidación respiratoria.
- 15. El examen de las mitocondrias respirando, revela que cuando los sustratos son oxidados por la vía de las enzimas deshidrogenasas ligadas al NAD, se incorporan 3 mol de fosfato inorgánico al ADP para formar 3 mol de ATP. Por otro lado, cuando un sustrato es oxidado por la vía de las enzimas deshidrogenasas ligadas a la flavoproteína FAD, solo se forman dos moléculas de ATP. 1. LA MITOCONDRIA
- 16. 2. NUCLEOTIDOS Se requieren electrones generados a partir de la acción enzimática de las deshidrogenasas relacionadas en el ciclo de Krebs. Este complejo toma electrones y los transfieren como pares a lo largo de la cadena. Utilizan nucleótidos de Adenina NAD y de Flavina FAD actúan como aceptadores de electrones. SUTRATO REDUCIDO + NAD SUSTRATO OXIDADO + NADH + H*
- 18. COENZIMA Q CITOCROMOS 3. MOLECULAS TRANSPORTADORAS La coenzima Q es una molécula móvil que une las flavoproteínas con el citocromo b (Complejo III). Es un constituyente de los lípidos mitocondriales, se encuentra en forma de quinona oxidada en condiciones aerobias y en la forma de quinol reducido en condiciones anaeróbicas. Esta molécula junto al citocromo c son los componentes móviles de la cadena respiratoria, los cuales conectan a los compuestos fijados.
- 19. EQUIVALENTES REDUCTORES Toda la energía útil liberada durante las oxidaciones de los ag, aa y ch, queda disponible en el interior de las mitocondrias en forma de equivalentes reducidos: H+ o electrones que fluyen a través de la cadena de manera escalonada desde los componentes más electro-negativos (NAD, FAD, citocromos) hasta llegar más electropositivo (Oxígeno).
- 21. ADENOSIN TRIFOSFATO (ATP=Adenosina Trifosfato • Molécula Energética Fundamental En El Intercambio Y Transformación De Energía En El Metabolismo. 4. ATP • El nucleosido (la ribosa unida a la base, sin P) facilita y capacita a la molécula para que reconozca y se fije en enzimas especificas. • El brazo trifosfatado (3P) aporta a la molécula su reactividad química, relacionada directamente con la energía libre.
- 22. ADENOSIN DIFOSFATO Molécula energética fundamental en el intercambio y transformación de energía en el metabolismo. ADP ADP: Molécula que captura energía, libre resultante de los procesos catabólicos. ATP: Posteriormente pasa esta energía para impulsar aquellos procesos que la requieren. Cuando se efectúa trabajo, el ATP es convertido en ADP, permitiendo que ocurra más respiración, lo cual a su vez reabastece el depósito de ATP.
- 23. 5. ATPasa • Las ATPasas son el subconjunto de enzimas que son capaces de producir la hidrólisis del ATP en ADP y posterior unión de fósforo (ion fosfato) libre. Esta reacción es exergónica ya que libera energía. • Se clasifican teniendo en cuenta los iones que transporta en ATPasaH+ y ATPasaCa2+.
- 24. ATPasa H+ o ATP Sintetasas Sintetizar el ATP a partir del ADP y P, utilizando la energía del gradiente de concentración H+. ATPasaCa2+ Mantener la concentración del Ca2+ en el interior de la célula. 5. ATPasa
- 25. 6. Enzimas • Monoaminooxidasa • Acetil-CoA sintetaza • Glicerofosfato aciltransferasa • Fosfolipasa • Creatincinasa • Adenililcinasa.
- 26. COMPLEJOS DEL TRANSPORTE DE ELECTRONES COMPLEJO I: NADH –UBIQUINONA REDUCTASA COMPLEJO II: SUCCINATO UBIQUINONA REDUCTASA COMPLEJO III: UBIQUINOL CITOCROMO C – REDUCTASA COMPLEJO IV: CITOCROMO C – OXIDASA COMPLEJO V: FOSFORILACIÓN OXIDATIVA
- 27. La NADH-Q oxidorreductasa o complejo I es una proteína grande, en forma de L (girada), que cataliza la transferencia de electrones desde NADH hacia la Coenzima Q, junto con la transferencia de 4 H+ a través de la membrana: NADH + H + Q + 4 H+ NAD + QH2 + 4H+ Matriz Espacio Intermembrana COMPLEJO I NADH –UBIQUINONA REDUCTASA
- 28. COMPLEJO I NADH –UBIQUINONA REDUCTASA • Enzima responsable de recibir los electrones del NADH. • Cede los electrones al Coenzima Q (Ubiquinona – UQ). • Posee un grupo FMN, con estructura similar al FAD. También tiene una proteína Fe-S. El NADH+ H+: Pasa los electrones a través del primer complejo hasta la Ubiquinona (Co Q), los iones H+ traspasan la membrana hacia el espacio intermembrana.
- 29. En el complejo II se forma FADH2 durante la conversión de succinato en fumarato en el ciclo del ácido cítrico (CK) y luego los electrones pasan hacia Q. Es el mas pequeño de la cadena, utiliza sustancias derivadas del ciclo de Krebs y cataliza la reducción de ubiquinona a ubiquinol. SUCCINATO + COQ FUMARATO + COQH2 COMPLEJO II: SUCCINATO UBIQUINONA REDUCTASA
- 30. COMPLEJO III: COENZIMA Q CITOCROMO C – REDUCTASA • El complejo III transfiere electrones desde la coenzima Q a el citocromo C, generando un nuevo bombeo de protones al exterior.
- 31. • Complejo multienzimático con varios centros activos: citocromo b, citocromo c1 y proteína de Rieske (también contiene grupo Hierro y Azufre). • Funciona como una bomba de protones por su orientación asimétrica. Su función es producir una diferencia de protones entre el interior y el exterior de la membrana mitocondrial. Los electrones se pasan desde QH2 hacia citocromo c por medio del complejo III: QH4 + citc oxidado Q + Cit c reducido (4H)+ 4H+ + MATRIZ 4H+ espacio intermembrana COMPLEJO III: UBIQUINOL CITOCROMO C – REDUCTASA
- 32. Enzima encargada de dar los electrones de la cadena al aceptor final: la molécula de oxígeno. El complejo IV oxida el citocromo c reducido, con la reducción concomitante de O2 hacia dos moléculas de agua: Cit c reducido( 4H) + ½O2 + matriz Cit c oxidado+ H2O + 2H+ espacio intermemb. COMPLEJO IV: CITOCROMO C – OXIDASA De las cuatro H+ eliminados de la matriz, dos se usan para formar la moléculas de agua, y dos se bombean hacia el espacio intermembrana. De este modo por cada par de electrones que pasa por la cadena desde NADH o FADH2, el complejo IV bombea 2H+ a través de la membrana
- 34. Cadena respiratoria Los cuatro complejos están embebidos en la membrana mitocondrial interna, pero la Coenzima Q y Citocromo c son móviles. El flujo de electrones a través de los complejos I, III y IV da por resultado el bombeo de protones desde la matriz mitocondrial hacia el espacio intermembrana.
- 36. Cadena respiratoria La cadena está formada por una serie de enzimas diseñadas por la evolución para aceptar y ceder electrones
- 37. FOSFORILACIÓN OXIDATIVA La ATP sintetasa es un complejo proteico con canales para protones que permiten la re-entrada de los mismos. La síntesis de ATP se produce como resultado de la corriente de protones fluyendo a través de la membrana: ADP + Pi ---> ATP
- 38. Encargada de la síntesis directa del ATP, estas enzimas se visualizan como pequeñas esferas sobre la membrana interna de la mitocondria, donde se encuentra gran cantidad de estas moléculas. Los protones son transferidos a través de la membrana, desde la matriz al espacio intermembranal (como resultado del transporte de electrones que se originan cuando el NADH cede un hidrógeno). COMPLEJO V: FOSFORILACION OXIDATIVA
- 39. COMPLEJO V: FOSFORILACION OXIDATIVA La continuada producción de esos protones crea un gradiente de protones, dado que las cargas + son retiradas del interior, mientras que las - permanecen en el interior (gran parte como OH-); el pH en la cara externa de la membrana puede llegar a un pH 5,5, mientras que el pH justo en la cara interna de la misma puede llegar a 8,5. (Peter Mitchell, 1961). La diferencia de potencial electroquímico se usa para impulsar a una ATP sintetasa localizada en la membrana la cual en presencia de Pi + ADP forma ATP.
- 40. FOSFORILACIÓN OXIDATIVA Cuando los protones (H+) regresan a la matriz, lo hacen por los canales un complejo proteico llamado ATPasa. El paso de H+ permite que la proteína “gire” y se lleve a cabo la reacción ADP+Pi formando ATP.
- 43. Lanzaderas Mitocondriales La membrana externa de la mitocondria es mucho más permeable que la interna, por lo cual hay movimiento libre para muchos solutos entre el citosol y el espacio intermembranoso. Debido a que la membrana interna es sumamente selectiva generalmente se requieren diversos sistemas de transporte para transferir compuestos desde el espacio intermembranoso hasta en interior de la mitocondria. La membrana interna de la mitocondria no es permeable al NAD+ o al NADH + H+ (la mitocondria tiene su propio “pool” de estos nucleótidos). Existen dos mecanismos diferentes para el transporte hasta la mitocondria de los equivalentes de reducción contenidos en el NADH +H+ producido en el citoplasma: La lanzadera malato-aspartato. La lanzadera del glicerofosfato.
- 44. Lanzadera de Malato-Aspartato Los equivalentes de reducción contenidos en el NADH + H+ producido en el citoplasma son transferidos al oxaloacetato para formar malato, en una reacción catalizada por la enzima malato deshidrogenasa citoplasmática: El Malato puede atravesar las membranas mitocondriales y entrar en la matriz mitocondrial. Una vez allí el malato es deshidrogenado por la enzima mitocondrial malato deshidrogenasa El oxaloacetato es transaminado a aspartato, el cual sale de la mitocondria y una vez en el citosol, es transaminado a oxalacetico comenzando un nuevo ciclo. Citosol: Oxaloacetato + NADH.H+ Malato + NAD+ Mitocondria: Malato + NAD+ oxaloacetato + NADH.H+
- 45. Con esta lanzadera, los equivalentes de reducción del NADH +H+ citosólico son transferidos a dihidroxiacetona fosfato para formar glicerol 3-fosfato, en una reacción catalizada por la glicerol 3-fosfato deshidrogenasa citoplasmática, que oxida al NADH.H+ del citosol: Citosol: dihidroxiacetona-P+ NADH.H+ glicerol 3-P + NAD+ El glicerol 3-P es deshidrogenado por la glicerol 3-P deshidrogenasa mitocondrial, localizada en la superficie exterior de la membrana interna de la mitocondria. Esta enzima es una flavoproteína y los equivalentes de reducción son transferidos en la membrana interna de la mitocondria: Membrana interna: glicerol 3 (P) + FAD dihidroxiacetona (P) + FADH2 Lanzadera de Glicerol 3-P
- 46. Lanzadera de glicerol 3-P
- 47. MALATO- ASPARTATO: Células de hígado y corazón. NADH citosólico a NADH mitocondrial. Aspartato Oxaloacetato Malato. Se producen 3 moles de ATP por mol. GLICEROL 3 - FOSFATO: Células cerebrales y músculo. Entrega los electrones a FAD+ Glicerol 3-P. Se producen 2 moles de ATP por mol. LANZADERAS MITOCONDRIALES
- 48. Factores que Controlan el Proceso Respiratorio • Número y morfología de mitocondrias. • Disponibilidad de ADP y P. • Capacidad de saturación de la cadena respiratoria. • Disponibilidad de Oxígeno. • Número de proteínas asociadas a la membrana mitocondrial interna, responsables del consumo de O2 y síntesis de ATP.
- 49. Inhibidores de la CTE • Interrumpen el transporte del NADH a la CoQ: Amobarbital (fármaco), Piericidina (antibiótico) y Rotenona (insecticida): • Inhiben entre el citocromo b y citocromo c: Dimercaprol y la antimicina A. • Inhiben la citocromo oxidasa: Monóxido de carbono, H2S y Cianuro. • Inhibe la succinato deshidrogenasa que transfiere hidrogeniones a la CoQ: Carboxina , TTFA. • Inhibidor competitivo de la succinato deshidrogenasa: Malonato. • Impide la oxidación y la Fosforilacion de las mitocondrias: Oligomicina. • Inhibe fosforilación oxidativa bloqueando el ADP (transportador): Atractilósido . • Producen desacople: Dinitrocresol, Pentaclorofenol, CCCP (clorocarbonil cianuro fenil hidrazona).
- 50. Desacoplantes de la CTE • En la membrana interna hay sustancias que aumentan la permeabilidad a los protones: Forman una ruta que disipa el gradiente de protones no asociada a ATP (permiten el transporte de electrones inhibiendo la síntesis de ATP). • Detienen las rx de fosforilación pero no las de oxidación, las cuales suceden a altas velocidades y liberan energía en forma de calor (No ATP) • Tratamientos con soluciones hipotónicas, uso de detergentes, cortes mecánicos. • Sustancias de naturaleza ácido débil y permeable a través de la membrana como el 2-4- dimitrofenol, NH4+.
- 51. Inhibidores de la FO • Interrumpen el transporte del NADH a la CoQ: Amobarbital, Piericidina, Rotenona. • Inhibe la succinato deshidrogenasa que transfiere hidrogeniones a la CoQ: Carboxina , TTFA. • Impide la oxidación y la fosforilación: Oligomicina. • Inhibe fosforilación oxidativa bloqueando el ADP (transportador): Atractilósido . • Producen desacople: Dinitrocresol, Pentaclorofenol, CCCP (clorocarbonil cianuro fenil hidrazona).
- 53. ASPECTOS CLINICO • Miopatía mitocondrial mortal infantil con disfunción renal infantil mortal, comprenden disminución grave o ausencia de la mayor parte de las oxidorreductasas de la cadena respiratoria. • Encefalopatía mitocondrial, estado hereditario causado por NADH: deficiencia de complejos I y IV. • Acidosis láctica. • Infarto cerebral.
- 54. RESUMEN Casi toda la energía liberada a partir de la oxidación de los carbohidratos, grasas y proteínas se pone a disposición en las mitocondrias como equivalentes reductores (-H o electrones), los cuales se dirigen hacia la cadena respiratoria, donde pasan por un gradiente de redox de acarreadores hacia su reacción final con oxígeno para formar agua. Los acarreadores redox están agrupados en cuatro complejos de cadena respiratoria en la membrana mitocondrial interna. Tres de los cuatro complejos tienen la capacidad para usar la energía liberada en el gradiente redox para bombear protones hacia el exterior de la membrana, lo que crea un potencial electroquímico entre la matriz y el espacio de la membrana interna.
- 55. RESUMEN La ATP sintasa abarca la membrana y actúa como un motor rotatorio usando la energía potencial del gradiente de protón o fuerza matriz de protón para sintetizar ATP a partir de ADP y fosfato. De este modo, la oxidación está estrechamente acoplada a la fosforilación para satisfacer las necesidades de energía de las células. Muchos venenos bien conocidos, como el cianuro, suspenden la respiración mediante inhibición de la cadena respiratoria.
- 56. GRACIAS
