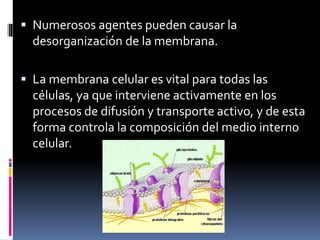
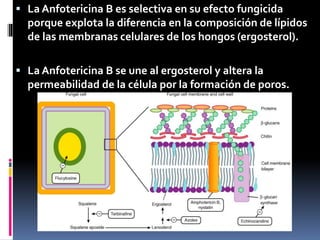
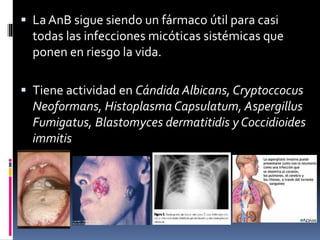
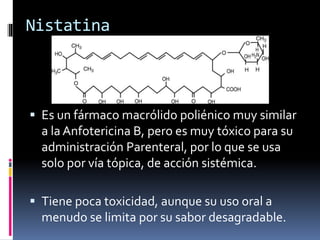
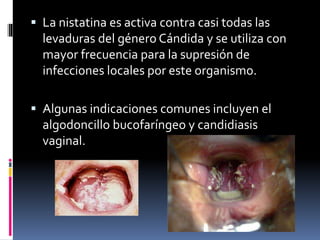
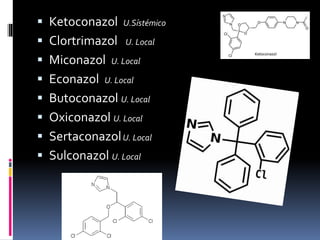
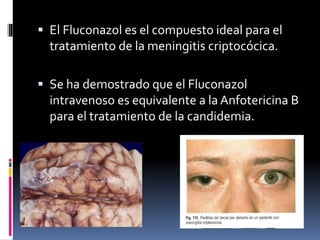
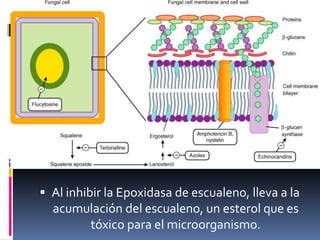
Los antibióticos de membrana como la polimixina, colistina y anfotericina B actúan alterando la permeabilidad de la membrana celular bacteriana y fúngica, causando la muerte celular. La polimixina es eficaz contra bacilos gramnegativos, mientras que la anfotericina B es un fármaco fungicida que se une al ergosterol de las membranas de hongos. Se discuten los mecanismos de acción y efectos adversos de varias clases de antifúngicos, incluyendo los azoles y la terbinafina.