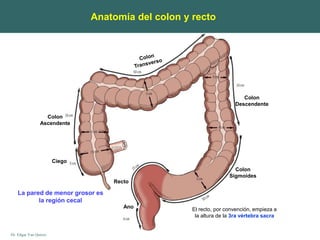
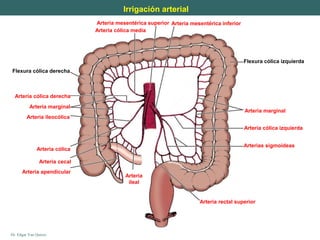
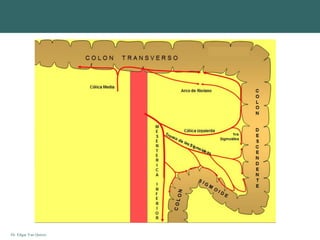
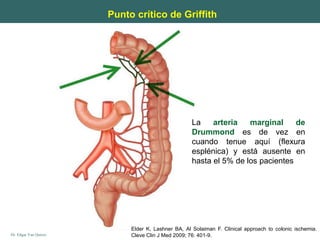
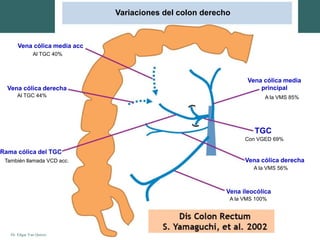
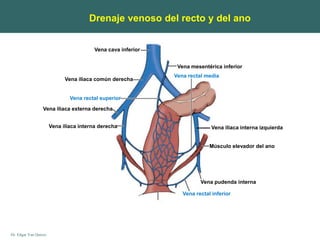
Este documento presenta la anatomía del colon y recto. Describe la irrigación arterial y drenaje venoso, así como la histología de la pared intestinal. Explica que el recto comienza a la altura de la tercera vértebra sacra y que los segmentos medios del colon son móviles a diferencia de los segmentos ascendente y descendente que están fijos. Finalmente, menciona que la pared de menor grosor es la región cecal.












































![Dr. Edgar Yan Quiroz
• Pérdida del control de crecimiento
• Causa subyacente desconocida
• Gen APC – Wnt singnaling pathway (Aumento de la B catenina)
• Microsatélite estable
• Alternación de la metilación (Hipometilación global y 3 posibles
patrones de metilación de promotores [CIMP negativo, bajo o alta]
INESTABILIDAD CROMOSOMAL](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-52-320.jpg)
















![Dr. Edgar Yan Quiroz
Lee MS, Menter DG, Kopetz S. Right Versus Left Colon Cancer Biology: Integrating the
Consensus Molecular Subtypes. J Natl Compr Canc Netw 2017; 15 (3): 411 – 419.
Resumen de las diferencias biológicas entre los CCR del lado derecho e izquierdo
Islas CpG son regiones
de ADN que conforman
aproximadamente un
40% de promotores de
los genes
[Anticuerpo IgG1 monoclonal quimérico cuya diana es el
receptor del factor de crecimiento epidérmico (EGFR)]](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-69-320.jpg)






![Dr. Edgar Yan Quiroz
Aunque la identificación de una mutación
germinal en un gen de reparación de los errores
de emparejamiento del ADN (REE), a través del
SECUENCIAMIENTO [conjunto de métodos y
técnicas bioquímicas cuya finalidad es la
determinación del orden de los nucleótidos (A, C, G
y T) en un oligonucleótido de ADN]
Síndrome de Lynch, los
pacientes generalmente se
someten a selección
considerando:
Es DEFINITIVO
para
Los antecedentes familiares y
Prueba inicial en el tejido tumoral
ANTES DEL SECUENCIAMIENTO.
Evaluación del riesgo
Síndrome de Lynch
1. Análisis inmunohistoquímico (IHQ) de la expresión de proteínas REE, que a menudo está
disminuida debido a la mutación, o
2. El análisis de la inestabilidad de microsatélites (IMS), que resulta de la deficiencia de REE
(mismatch repair) y se detecta como cambios en la longitud de los elementos de ADN
repetitivo en el tejido tumoral causados por la inserción o supresión de unidades repetidas
Una de dos pruebas iniciales diferentes se pueden realizar en muestras de cáncer colorrectal para
identificar a las personas que podrían tener el síndrome de Lynch:
Gen BRAF](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-76-320.jpg)






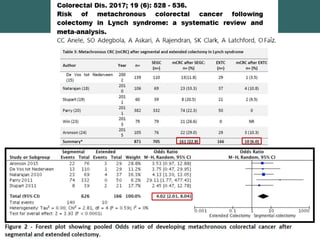
















































































![Dr. Edgar Yan Quiroz
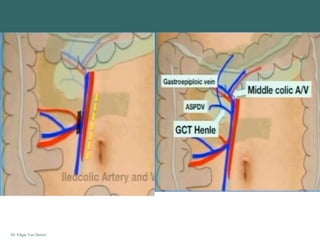
Diferencias entre la escisión mesocolónica
completa (EMC) y disección D3 Japonesa
Diferencias EMC D3
Linfadenectomía
central
EMC es la disección anatómica a lo largo
de los planos embrionarios con
preservación de la fascia visceral
intacta del mesocolon. Incluye ligadura
vascular central (LVC)
Eliminación de todas las
estaciones de ganglios
linfáticos regionales según la
localización del tumor, lo que
incluye la extracción de los
ganglios linfáticos alrededor del
origen de las arterias de
alimentación (ganglios
principales).
Longitud del
intestino a resecar
Es más radical porque incluye la
eliminación de la arcada vascular
cercana más allá del margen de 10 cm
Se determina en función de
qué ganglios linfáticos
pericólicos deben
considerarse regionales
Linfadenectomía
extendida
Disección de los ganglios linfáticos
extramesentéricos (es decir, sobre la
cabeza del páncreas y a lo largo de la
región infrapilórica [grupo 6] y
gastroepiploicos [grupo 4d y 4sb])
Estos ganglios linfáticos
extramesentéricos no se
diseccionan rutinariamente en
ninguna institución japonesa en
la actualidad](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-167-320.jpg)













































































![Dr. Edgar Yan Quiroz
No obstante, en contraste con los hallazgos de Sargent et al [Sargent 2010 No 278], un estudio
reciente en 1913 pacientes con cáncer colorrectal en estadio II del estudio QUASAR, la 1/2 de los
cuales recibió QT adyuvante, mostró que aunque el estado REEd era un factor pronóstico (la tasa
de recidiva de los tumores REEd fue del 11% frente al 26% para los tumores de dominio REEd), no
indicó el beneficio o el impacto perjudicial de la quimioterapia.
Un estudio reciente de pacientes en los ensayos CALGB 9581 y 89803 llegó a la misma conclusión
Inestabilidad de microsatélites (IMS)
Quimioterapia adyuvante en la enfermedad en estadio II](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-252-320.jpg)
![Dr. Edgar Yan Quiroz
El estado REE fue un factor pronóstico pero no predictivo del beneficio o del impacto perjudicial de
la terapia adyuvante (irinotecán más bolo de 5 FU/LV [régimen IFL]) en pacientes con cáncer de
colon en estadio II
Debido a que los pacientes con tumores IMS – A en estadio II pueden tener un buen pronóstico y
no beneficiarse de la terapia adyuvante con 5 FU, el panel recomienda considerar las pruebas de
REE para pacientes con enfermedad en estadio II.
La histología pobremente diferenciada no se considera una característica de alto riesgo para los
pacientes con enfermedad en estadio II cuyos tumores son IMS – A.
Además se deben realizar las pruebas de REE para todos los pacientes con cáncer colorrectal
diagnosticados
Inestabilidad de microsatélites (IMS)
Quimioterapia adyuvante en la enfermedad en estadio II
A una edad de 70 años o menor +
Los pacientes diagnosticados a edades más avanzadas y que cumplen con las pautas de Bethesda
para evaluar la posibilidad del síndrome de Lynch](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-253-320.jpg)























![Dr. Edgar Yan Quiroz
Capecitabina* 1250 mg/m2 VO (Se debe tomar con agua después de las comidas:30
minutos después de comer) en 2 tomas, del D1 al D14, c/3 semanas, por 24 semanas
Régimen de Roswell Park
DL Leucovorina 500 mg/m2 (o L Leucovorina 250 mg/m2) IV
durante 2 horas, seguido de
5 – FU 500 mg/m2, 1 hora después del inicio de leucovorina,
días 1,8,15,22,29 y 36 [o 1 vez/semana por 6 semanas] cada 8
semanas por 3 ciclos
5 FU/LV simplificado bisemanalmente infusional [sLV5FU2]
Leucovorina 400 mg/m2 IV durante 2 horas en el día 1, seguido de
5 FU 400mg/m2 en bolo y luego 1200 mg/m2/día por 2 días (total
2400 mg/m2 durante 46 – 48 horas) en infusión continua cada 14
días x 12 ciclos
Son opciones para
pacientes quienes no son
candidatos para terapia
oral
Tratamiento adyuvante
FOLFOX
Oxaliplatino 85 mg/m2 IV durante 2 horas, día 1
Leucovorina 400 mg/m2 IV durante 2 horas, día 1
5 FU 400 mg/m2 IV bolo durante 1 día, luego 1200 mg/m2/día x 2 días
(total 2400 mg/m2 durante 46 – 48 horas) + IV infusión continua
Repetir cada 2 semanas
CapeOx
Oxaliplatino 130 mg/m2 durante 2 horas, día 1
Capecitabina 1000 mg/m2 2 veces al día, días 1 – 14 cada 3 semanas
x 24 semanas
FLOX
5 FU 500 mg/m2 IV bolo semanalmente x 6 + leucovorina 500 mg/m2
IV semanalmente x 6, cada 8 semanas por 3 ciclos con
Oxaliplatino 85 mg/m2 IV administrado en las semanas 1,3 y 5 cada 8
semanas x 3 ciclos
Peso (Kg) x Talla (cm)
3600
Superficie
corporal =
(*) Actúa como un precursor del citotóxico 5-fluorouracilo. La incorporación del 5-FU conduce a la inhibición del ARN y síntesis proteica.](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-277-320.jpg)

















































































![Dr. Edgar Yan Quiroz
Presentación
clínica
Estudio
diagnóstico Hallazgos
Adenocarcinoma
sincrónico
metastásico
demostrado o
sospechoso
(Cualquier T,
cualquier N, M1)
• Colonoscopia
• TC tórax/ abdomen pelvis
• Hemograma, perfil bioquímico
• CEA
• Determinación del estatus del
gen KRAS y BRAF
(individualmente o como parte
del panel de secuenciación de
próxima generación [SPG])
• Biopsia, si clínicamente esta
indicado
• Considerar PET CT scan
(desde la base del cráneo hasta
la mitad del muslo) solamente
si la enfermedad M1 es
quirurgicamente
potencialmente curable en
casos seleccionados
• Evaluación por equipo
multidisciplinario, incluyendo
un cirujano experimentando en
la resección de metástasis
pulmonar y hepatobiliar
Resecable
Irresecable
(potencialmen
te convertible
o no
convertible)
Metástasis
abdominal/peritoneal
sincrónica
Metástasis
sincrónica solo
a hígado y/o
solo a pulmón
Ver tratamiento y
terapia adyuvante
Ver tratamiento y
terapia adyuvante
Ver tratamiento
primario
3
Metástasis irresecable
sincrónica de otros
sitios
Ver quimioterapia
para enfermedad
avanzada o
metastásica](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-360-320.jpg)

![Dr. Edgar Yan Quiroz
Presentación
clínica
Estudio
diagnóstico
Hallazgos
Adenocarcinoma
sincrónico
metastásico
demostrado o
sospechoso
(Cualquier T,
cualquier N, M1)
• Colonoscopia
• TC tórax/ abdomen pelvis
• Hemograma, perfil bioquímico
• CEA
• Determinación del estado del
gen tumoral para RAS y BRAF
(individualmente o como parte
de la secuenciación de próxima
generación [Panel NGS])
• Biopsia, si clínicamente esta
indicado
• Considerar PET CT scan
(desde la base del cráneo hasta
la mitad del muslo) solamente
si la enfermedad M1 es
quirurgicamente
potencialmente curable en
pacientes seleccionados
• Evaluación por equipo
multidisciplinario, incluyendo
un cirujano experimentando en
la resección de metástasis
pulmonar y hepatobiliar
Resecable
Irresecable
(potencialmen
te convertible
o no
convertible)
Metástasis
abdominal/peritoneal
sincrónica
Metástasis
sincrónica solo
a hígado y/o
solo a pulmón
Ver tratamiento y
terapia adyuvante
Ver tratamiento y
terapia adyuvante
Ver tratamiento
primario
3
Ver quimioterapia
para enfermedad
avanzada o
metastásica
Metástasis irresecable
sincrónica de otros
sitios](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-362-320.jpg)
![Dr. Edgar Yan Quiroz
TERAPIA ADYUVANTE
• Terapia sistémica (FOLFIRI
o FOLFOX o CapeOx ±
bevacizumab o FOLFIRI o
FOLFOX ± panitumumab o
FOLFIRI ± cetuximab [solo
para el gen tipo salvaje
KRAS/NRAS y tumores del
lado izquierdo]
• Considerar resección del
colon solamente si hay
riesgo inminente de
obstrucción, hemorragia
significante, perforación y
otros síntomas
relacionados con el tumor
Reevaluar para
conversión a
resecabilidad cada 2
meses si la
conversión a
resecabilidad es un
meta razonable
Conversión a
resecabilidad
Permanece
irresecable
Resección sincronizada
o resección por etapas
de colon y cáncer
metastásico
Ver terapia sistémica ±
terapia biológica
(categoría 2B para
terapia biológica)
O
Considerar observación
o un curso corto de
quimioterapia ((6 meses
de tto perioperatorio
preferentemente)
TRATAMIENTO
Hígado sincrónico irresecable y/o
solamente metástasis pulmonar
SEGUIMIENTO
Ver
seguimiento
Ver terapia sistémica](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-363-320.jpg)



![Dr. Edgar Yan Quiroz
Sin quimioterapia
previa
Quimioterapia
previa
Quimioterapia
neoadyuvante (2 – 3
meses) FOLFOX
(preferido) o CapeOx
[preferido] o
Capecitabina o 5
FU/leucovorina
(categoría 2B)
Resección
(preferido)1
y/o terapia
local
FOLFOX o CapeOx (preferido)
o
Capecitabina o 5 FU/leucovorina
No hay
crecimiento
en la
quimioterapia
neoadyuvante
Crecimiento
en la
quimioterapia
neoadyuvante
Resección
(preferido)1 y/o
terapia local
Quimioterapia
neoadyuvante
(2 – 3 meses)
FOLFOX
(preferido) o
CapeOx
[preferido] o
Capecitabina o
5
FU/leucovorina
o
Reiniciar terapia
neoadyuvante2
o
FOLFOX
u
Observación
Terapia sistémica ±
terapia biológica
(categoría 2B para
terapia biológica)
u
Observación
o
Resección
(preferido)1
y/o terapia
local
No hay
crecimiento
en la
quimioterapia
neoadyuvante
Crecimiento
en la
quimioterapia
neoadyuvante
Reiniciar terapia
neoadyuvante2
o
FOLFOX
u
Observación
Terapia sistémica ±
terapia biológica
(categoría 2B para
terapia biológica)
u
Observación
Observación (preferido para terapia previa
basada en oxaliplatino)
o
Terapia sistémica ± terapia biológica
(categoría 2B para terapia biológica)
(1) Infusión de la arteria hepática ± 5FU/leucovorina sistémica es también una opción en instituciones con experiencia tanto en
aspectos oncológicos médicos y quirúrgicos de este procedimiento
(2) Terapia perioperatoria debería ser considerada para un total de 6 meses
METÁSTASIS
METACRÓNICA
RESECABLE
TRATAMIENTO
PRIMARIO
TRATAMIENTO ADYUVANTE (6 meses de
tratamiento perioperatorio preferido)
Resección
(preferido)1 y/o
terapia local](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-367-320.jpg)
![Dr. Edgar Yan Quiroz
Re evaluar
para
conversión a
resecabilidad
cada 2 meses ,
si la
conversión a
resecabilidad
es un objetivo
razonable
• FOLFOX/CAPEOX adyuvante
previa dentro de los últimos
12 meses
• FOLFOX/CAPEOX adyuvante
previa > 12 meses
• 5 FU/LV o capecitabina previa
• No quimioterapia previa
Terapia sistémica
Resección3
Terapia
sistémica ±
biológica
(categoría 2B
para terapia
biológica
u
Observación
Terapia sistémica
Permanece
irresecable
Convertido
a resecable
(1) Bevacizumab es el agente antioangiogénico preferido basada en su toxicidad y/o costo
(2) La mutación BRAF V600E hace que la respuesta al panitumumab o cetuximab sea altamente improbable a menos que se administre
con un inhibidor de BRAF
(3) Infusión de la arteria hepática ± 5FU/leucovorina sistémica es también una opción en instituciones con experiencia tanto en aspectos
oncológicos médicos y quirúrgicos de este procedimiento
METÁSTASIS
METACRÓNICA
IRRESECABLE
TRATAMIENTO PRIMARIO TRATAMIENTO ADYUVANTE (6
meses de tratamiento
perioperatorio preferido)
(FOLFIRI o irinotecan) ±
(bevacizumab [preferido] o ziv –
aflibercept o ramucirumab) 1
o
(FOLFIRI o Irinotecan) ±
(cetuximab o panitumumab)
(únicamente gen KRAS/NRAS
cepa salvaje) 2
o
Nivolumab o pembrolizumab
(dMMR/IMS – H únicamente)
o
Irinotecan ± (cetuximab o
panitumumab) + vemurafenib
[mutación BRAF V600E positivo] 2](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-368-320.jpg)















![Dr. Edgar Yan Quiroz
Re evaluar
para
conversión a
resecabilidad
cada 2 meses ,
si la
conversión a
resecabilidad
es un objetivo
razonable
• FOLFOX/CAPEOX adyuvante
previa dentro de los últimos
12 meses
• FOLFOX/CAPEOX adyuvante
previa > 12 meses
• 5 FU/LV o capecitabina previa
• No quimioterapia previa
Terapia sistémica
Resección3
Terapia
sistémica ±
biológica
(categoría 2B
para terapia
biológica)
u
Observación
Terapia sistémica
Permanece
irresecable
Convertido
a resecable
(1) Bevacizumab es el agente antioangiogénico preferido basada en su toxicidad y/o costo
(2) La mutación BRAF V600E hace que la respuesta al panitumumab o cetuximab sea altamente improbable a menos que se administre
con un inhibidor de BRAF
(3) Infusión de la arteria hepática ± 5FU/leucovorina sistémica es también una opción en instituciones con experiencia tanto en aspectos
oncológicos médicos y quirúrgicos de este procedimiento
METÁSTASIS
METACRÓNICA
IRRESECABLE
TRATAMIENTO PRIMARIO TRATAMIENTO ADYUVANTE (6
meses de tratamiento
perioperatorio preferido)
(FOLFIRI o irinotecan) ±
(bevacizumab [preferido] o ziv –
aflibercept o ramucirumab) 1
o
(FOLFIRI o Irinotecan) ±
(cetuximab o panitumumab)
(únicamente gen KRAS/NRAS
cepa salvaje) 2
o
Nivolumab ± ipilimumab o
pembrolizumab (dMMR/IMS – H
únicamente)
o
(Irinotecan ± [cetuximab o
panitumumab] + vemurafenib
[mutación BRAF V600E positivo] 2](https://image.slidesharecdn.com/cacolon-220831084519-d2c57f2d/85/CA-COLON-384-320.jpg)