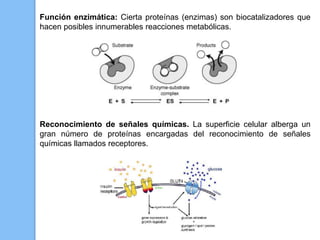
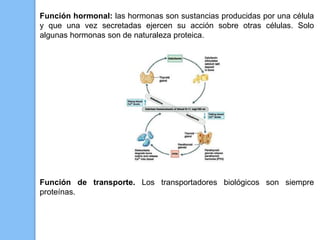
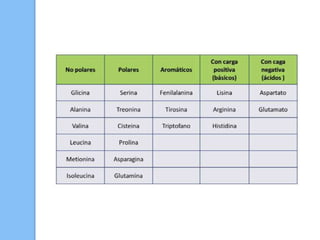
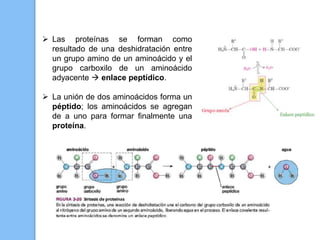
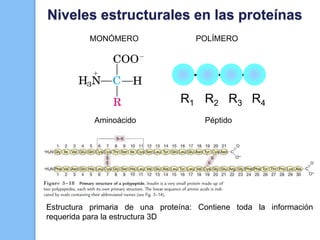
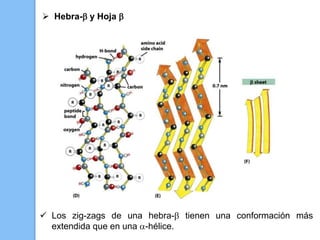
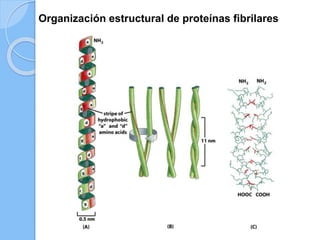
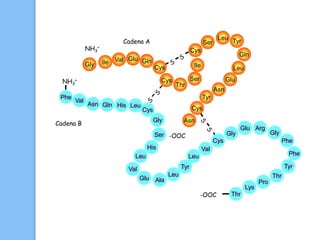
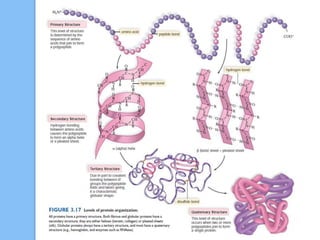
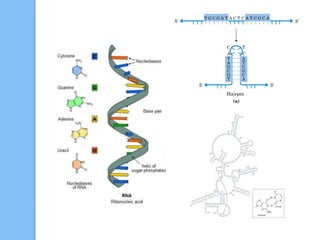
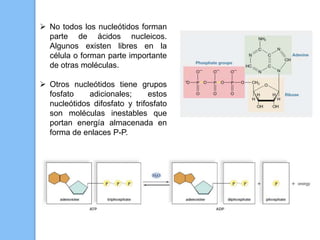
El documento describe las biomoléculas proteínas y ácidos nucleicos. Explica que las proteínas están compuestas por cadenas de aminoácidos unidos por enlaces peptídicos y adoptan diferentes estructuras como alfa hélice y hoja beta. Los ácidos nucleicos, ADN y ARN, están formados por cadenas de nucleótidos unidos por enlaces fosfodiéster entre un azúcar, una base nitrogenada y un grupo fosfato. El apareamiento de bases a través de puentes de hidrógeno permite la doble