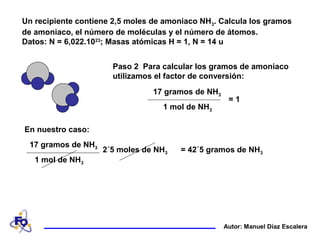
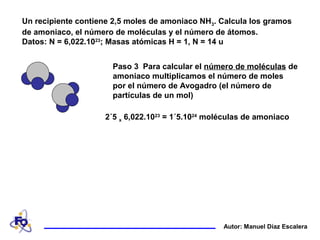
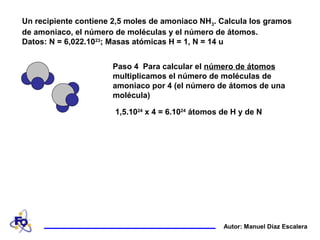
Un recipiente contiene 2,5 moles de amoniaco NH3. Se calculan los gramos de amoniaco (42,5 gramos), el número de moléculas (1,5 x 1024 moléculas) y el número de átomos (6 x 1024 átomos) mediante la conversión de moles a gramos, la multiplicación del número de moles por el número de Avogadro y la multiplicación del número de moléculas por el número de átomos por molécula.