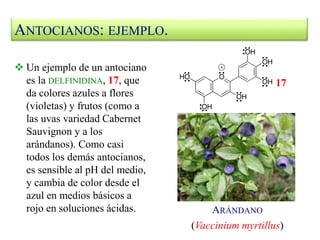
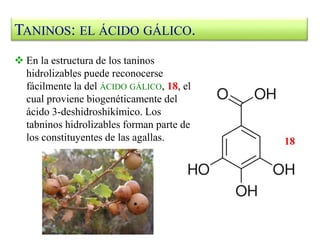
El documento describe la ruta del ácido shikímico, una ruta alternativa para la formación de compuestos aromáticos en plantas. Un intermediario clave es el ácido shikímico, que se aísla del anís estrellado y se usa para sintetizar el fármaco Tamiflu. La ruta del ácido shikímico genera metabolitos secundarios como fenoles, ácidos fenólicos, cumarinas, lignanos, flavonoides, antocianos y taninos.