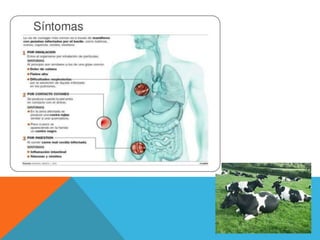
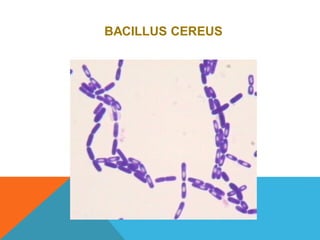
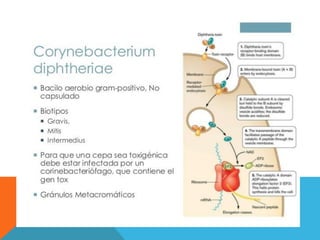
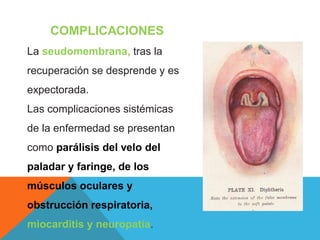
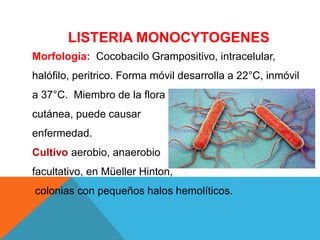
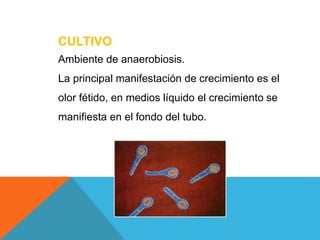
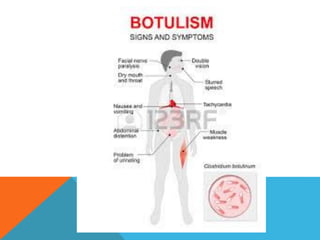
El documento describe la morfología, patogenia, y diagnóstico de varios bacilos grampositivos, incluyendo Bacillus anthracis y Corynebacterium diphtheriae, así como sus respectivos síndromes clínicos como el carbunco y la difteria. También se discuten las infecciones causadas por Bacillus cereus y Listeria monocytogenes, y se menciona el control y tratamiento para estas enfermedades. Finalmente, se abordan los clostridios, destacando el botulismo y el tétano como principales patologías asociadas.