final2.docx
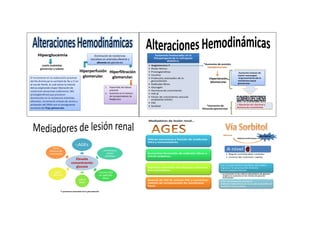
- 1. Lesión endotelial, glomerular y tubular. Disminución de resistencias vasculares en arteriolas eferente y aferente del glomérulo Hiperfiltración glomerular. Hiperperfusión glomerular 1. Hipertrofia del túbulo proximal 2. Aumento en el número de transportadores de Na/glucosa El incremento en la reabsorción proximal del Na disminuye la cantidad de Na y Cl en el asa de Henle, lo cuál activa la mácula densa originando mayor liberación de sustancias vasoactivas (adenosina, NO, prostaglandinas)que provocan disminución en la resistencia arteriolas aferentes, incremento síntesis de renina y activación del SRAA con el consiguiente aumento del flujo glomerular. Sustancias involucradas en la fisiopatogenia de la nefropatía diabética: • Angiotensina II • Óxido Nítrico • Prostaglandinas • Insulina • Productos avanzados de la glucosilación • Radicales libres • Glucagón • Hormona de crecimiento • TGF-β • Factor de crecimiento vascular endotelial (VEGF) • PKC • Sorbitol *Aumento de presión Hipertensión Glomerular -Aumento síntesis de matriz mesangial. -Engrosamiento de la membrana basal glomerular *Aumento de filtración glomerular + liberación de citocinas y factores de crecimiento. Elevada concentración glucosa *1AGEs aumenta el estrés oxidativo + producción de radicales libres activa SRAA Libera citocinas Libera factores de crecimiento . *1 productos avanzados de la glucosilación Alteran estructura y función de moléculas intra y extracelulares. Aumentan formación de radicales libres y estrés oxidativo. Modulan expresión de citocinas y factores del crecimiento. Síntesis de TGF-β, activan PKC y aumentan síntesis de componentes de membrana basal . Mediadores de lesión renal… Sorbitol aldosarreductasa A nivel : • Regula osmolaridad medular. • Control del volumen capilar. Los componentes celulares del riñón ingresan la glucosa de manera insulinodependiente. • un aumento en los valores plasmáticos de glucosa origina un aumento en los niveles de glucosa intracelular. Este incremento activa la aldosarreductasa con lo cuál aumente el sorbitol intracelular.
- 2. SRAA sistémico SRAA local: Todos se manifiestan en las células renales . La hiperglucemia aumenta la síntesis de angiotensinógeno y angiotensina II. corazón cerebro riñón Vasos sanguíneos SRAA • Aumento en síntesis de matriz mesangial • Aumento componentes de membrana basal Alteraciones estructurales • Podocitos • Células tubulares Apoptosis • PKC • Sistema Regulador JAK/STAT • Incrementa síntesis de TGF-β Activa • Flujo y presión intraglomerular por vasoconstricción. Incrementa Incrementa • síntesis de TGF-β Lesiones • Lesión Endotelial • Fibrosis tubulointersticial Anormalidadesestructurales en ND: • Expansión mesangial • Glomeruloesclerosis • Engrosamientode la membrana basal • Células endoteliales en espuma • Aplanamientoy pérdida de los podocitos • Células tubulares con depósitos de glucógeno • Atrofia tubular • Inflamación intersticial • Fibrosis intersticial • Arterioesclerosis Glomérulo Tubulointersticio Endotelio Hallazgo temprano. Pacientes con ND podocitopenia visible antes de la evidencia clínica de lesión renal. La reducción en el num de podocitos correlaciona con el grado de albuminuria. Detectados en la orina de pacientes con proteinuria. Expansión mesangial: • Secundaria a al aumento en la síntesis de los componentes de la matriz mesangial por las células mesangiales glomerulares. • Los nódulos de Kimmelstiel-Wilson representan áreas de glomeruloesclerosis nodular debido al marcado incremento de la matriz mesangial. Tubulointersticio: • En ND hay un aumento de grosor en la membrana basal tubular, fibrosis intersticial y arteriolosclerosis.
- 3. Expresión urinaria : 30 a 300µg/dL. DM-2 sin retinopatía Deterioro de función renal en ausencia de proteinuria. DM-1 Microalbuminuria Proteinuria •Microalbuminuria de corta duración. •Hb A1 menores de 8%. •Mantener PA diastólica < 90mmHg. •Concentración de Colesterol y triglicéridos normales. Disminución de función renal en ausencia de proteinuria indica un mayor grado de daño tubulointersticial Medición de la función renal DM-1: 5 años después del Dx. DM-2: cada año después de Dx. Buen control de la glucosa sérica (HbA1 < 7%) Control intensivo de la presión arterial (< 130/80 mmHg). Manejo temprano con inhibidores del SRAA. Control de: • Dislipidemia • Peso • Tabaquismo Cuidado de uso de agentes nefrotóxicos. • Medios de contraste y aminoglucósidos. Tratamiento no farmacológico Cambios en el estilo de vida – Reducción de peso – Evitar la ingesta excesiva de alcohol – Evitar la ingesta excesiva de sal – Realizar actividad física – Cambios en la alimentación – Control del estrés – Suspender tabaquismo. Control intensivo de glucosa: HbA1 menor a 7%= ND. Disminución incidencia: Microalbuminuria 39% Albuminuria 56% con control intensivo de glucosa: DM-1: DCCT Disminución incidencia: Microalbuminuri a 11% Microalbuminur ia- Albuminuria 3.5% con control intensivo de glucosa: DM-2: UKPDS Después de 8 años de seguimiento: Tx intensivo: 11.5% Tx convencional: 43.5% Pacientes que progresaron a ND: DM-1: Estudio de Kumamoto
- 4. Bloqueo de sistema renina angiotensina aldosterona SRAA • Disminuye progresión de daño renal en pacientes con DM. Independiente de efecto en TA DM-1 • APR elevada DM-2 • APR disminuida • Activación de sistemas locales del eje renina angiotensina. APR: Actividad plasmática de la renina. El efecto nefroprotector de inhibición de SRAA en DM-2 fue demostrado con el uso de antagonistasdel receptor de angiotensina II (ARA II). 3 diferentes estudios (comparando losartán o irbesartán vs placebo) mostraron que este tipo de fármacos mejoran el control de la proteinuria y disminuyen la velocidad de la progresión de daño renal. SRAA • En pacientes con ND el uso de antagonistas de aldosterona (espironolactona o eplenorona) ha demostrado disminución en la excreción urinaria de albúmina pero ningún efecto sobre la reducción de la tasa de filtración glomerular. • Con el uso de IECA o agentes ARA II puede observarse un incremento de 30% de las cifras de creatinina sérica posterior al inicio de estos medicamentos y estabilizarse a los dos meses de uso. • Un deterioro mayor de la función renal puede ser indicativo de presencia de estenosis de arteria renal. Conclusión… IECA ARA II Efecto benéfico en el control de la PA. Disminución de proteiuria. Retraso en la progresión de daño renal. D ia b e te sM e llitu s . T ra ta m ie n to . Cambio en el estilo de vida. Tx Farmacológico. GUIAS ADA/HARRION MED INTERNA ED 17/Internet.
- 5. Dia b e te sM e llitu s . • . GUIAS ADA/HARRION MED INTERNA ED 17/Internet. D ia b e te sM e llitu s . GUIAS ADA/HARRION MED INTERNA ED 17/Internet.