Equilibrio Quimico
•Descargar como PPTX, PDF•
0 recomendaciones•202 vistas
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (16)
Destacado
Destacado (20)
Relación entre respiración fotosíntesis y el ciclo de

Relación entre respiración fotosíntesis y el ciclo de
Les fenetres-labview-ne-sont-pas-toutes-rectangulaires

Les fenetres-labview-ne-sont-pas-toutes-rectangulaires
Innovación educativa con el uso de recursos educativos

Innovación educativa con el uso de recursos educativos
roles and functions of educational technology in the 21st century eduvcation

roles and functions of educational technology in the 21st century eduvcation
Similar a Equilibrio Quimico
Similar a Equilibrio Quimico (20)
Mapa conceptual, equilibrio químico. Br: Luiggy Rojas. 

Mapa conceptual, equilibrio químico. Br: Luiggy Rojas.
Último
Último (20)
Diseño Universal de Aprendizaje en Nuevos Escenarios JS2 Ccesa007.pdf

Diseño Universal de Aprendizaje en Nuevos Escenarios JS2 Ccesa007.pdf
cuadernillo_cuentos_de_los_valores_elprofe20 (1).docx

cuadernillo_cuentos_de_los_valores_elprofe20 (1).docx
ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA

ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA
Realitat o fake news? – Què causa el canvi climàtic? - La desertització

Realitat o fake news? – Què causa el canvi climàtic? - La desertització
novelas-cortas--3.pdf Analisis introspectivo y retrospectivo, sintesis

novelas-cortas--3.pdf Analisis introspectivo y retrospectivo, sintesis
DISEÑO DE ESTRATEGIAS EN MOMENTOS DE INCERTIDUMBRE.pdf

DISEÑO DE ESTRATEGIAS EN MOMENTOS DE INCERTIDUMBRE.pdf
Diapositivas unidad de trabajo 7 sobre Coloración temporal y semipermanente

Diapositivas unidad de trabajo 7 sobre Coloración temporal y semipermanente
ACERTIJO SOPA DE LETRAS OLÍMPICA. Por JAVIER SOLIS NOYOLA

ACERTIJO SOPA DE LETRAS OLÍMPICA. Por JAVIER SOLIS NOYOLA
ciclos biogeoquimicas y flujo de materia ecosistemas

ciclos biogeoquimicas y flujo de materia ecosistemas
04.UNIDAD DE APRENDIZAJE III CICLO-Cuidamos nuestro medioambiente (1).docx

04.UNIDAD DE APRENDIZAJE III CICLO-Cuidamos nuestro medioambiente (1).docx
4. MATERIALES QUE SE EMPLEAN EN LAS ESTRUCTURAS.pptx

4. MATERIALES QUE SE EMPLEAN EN LAS ESTRUCTURAS.pptx
FICHA DE LA VIRGEN DE FÁTIMA.pdf educación religiosa primaria de menores

FICHA DE LA VIRGEN DE FÁTIMA.pdf educación religiosa primaria de menores
Equilibrio Quimico
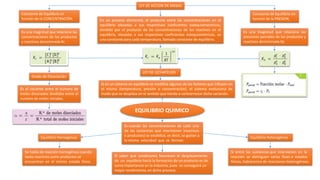
- 1. Es cuando las concentraciones de cada una de las sustancias que intervienen (reactivos o productos) se estabiliza, es decir, se gastan a la misma velocidad que se forman El saber qué condiciones favorecen el desplazamiento de un equilibrio hacia la formación de un producto es de suma importancia en la industria, pues se conseguirá un mayor rendimiento, en dicho proceso. Equilibrio Homogéneo Equilibrio Heterogéneo Se habla de reacción homogénea cuando tanto reactivos como productos se encuentran en el mismo estado físico. Si entre las sustancias que intervienen en la reacción se distinguen varias fases o estados físicos, hablaremos de reacciones heterogéneas. LEY DE ACCION DE MASAS En un proceso elemental, el producto entre las concentraciones en el equilibrio elevadas a sus respectivos coeficientes estequiomentricos, dividido por el producto de las concentraciones de los reactivos en el equilibrio, elevadas a sus respectivos coeficientes estequiometricos, es una constante para cada temperatura, llamada constante de equilibrio. Constante de Equilibrio en función de la CONCENTRACIÓN. Constante de Equilibrio en función de la PRESION. Es una magnitud que relaciona las concentraciones de los productos y reactivos denominada Kc Es una magnitud que relaciona las presiones parciales de los productos y reactivos denominada Kp Grado de Disociación Es el cociente entre el numero de moles disociados divididos entre el numero de moles iniciales. LEY DE LECHATELIER Si en un sistema en equilibrio se modifica algunos de los factores que influyen en el mismo (temperatura, presión o concentración), el sistema evoluciona de modo que se desplaza en el sentido que tienda a contrarrestar dicha variación. EQUILIBRIO QUIMICO