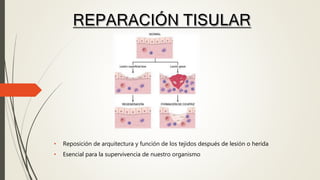
Reparación tisular
- 1. • Reposición de arquitectura y función de los tejidos después de lesión o herida • Esencial para la supervivencia de nuestro organismo
- 2. REPARACIÓN TISULAR La respuesta inflamatoria aparte de eliminar el agente patógeno permite el proceso de reparación de los tejidos. Se consigue mediante dos tipos de reacciones REGENERACIÓN • Produce por proliferación de células residuales (no lesionadas) que conservan su capacidad de división y sustitución dada por las células madre del tejido. FORMACIÓN DE CICATRIZ • Se produce por un depósito de un tejido conjuntivo formándose una cicatriz que aporta estabilidad estructural.
- 4. REGENERACIÓN CELULAR Y TISULAR CONTROL DE LA PROLIFERACIÓN CELULAR •Residuos de tejido lesionado, células endoteliales vasculares, fibroblastos proliferan reguladas por FACTORES DE CRECIMIENTO. •La replicación del ADN y la mitosis son procesos claves de la proliferación celular. •Donde en G1 la célula no se divide, en G0 ha abandonado el ciclo, en S
- 5. CAPACIDADES PROLIFERATIVAS DE LOS TEJIDOS La reparación depende en gran parte del tipo de tejido lesionado: Tejidos Labiles Tejidos Estables Permanentes
- 6. TEJIDOS LÁBILES Células en continua división. Son regenerados fácilmente después de una lesión, siempre que se conserve la reserva de células madre. Destacan las células hematopoyéticas medulares, algunos epitelios de superficie escamosos, cúbicos y cilíndricos
- 7. TEJIDOS ESTABLES Sus células permanecen en reposo con una mínima replicación. Capacidad de regeneración limitada en respuesta a una lesión. Células del parénquima de los tejidos sólidos; las células endoteliales, musculares lisas y fibroblastos.
- 8. TEJIDOS PERMANENTES Células diferenciadas de forma terminal y no proliferativas en la vida postnatal. Se produce una replicación y diferenciación limitada a partir de células madre en el encéfalo adulto No se regeneran tras una lesión, forma cicatriz Neuronas Miocitos cardiacos
- 9. CÉLULAS MADRE Capacidad de autorrenovación. Originan células hijas. Fundamentales en la regeneración tisular, desarrollo de células maduras células que nacen de las células madre
- 10. FUNDAMENTALMENTE EXISTEN 2 TIPOS DE CÉLULAS MADRE CÉLULAS MADRE EMBRIONARIAS (ME) • Se encuentran en la masa interna del blastocisto, con amplia capacidad de autorrenovación, pueden formar células de las tres capas de células germinales. CÉLULAS MADRE ADULTAS • Capacidad de autorrenovación y de estirpe (origen a células especializadas) limitada
- 11. CÉLULAS MADRE EMBRIONARIAS CÉLULAS MADRE TISULARES Dan origen a todas la células del organismo Homeostasis tisular
- 12. CÉLULAS MADRE TISULARES Las células madre tisulares son difícil de aislar en estado puro, se encuentran en los nichos de células madre de algunos órganos. Son activadas aparentemente por otras células que se encuentran en estos nichos Más estudiadas son las HEMATOPOYÉTICAS pueden ser aisladas gracias a G-CSF, para ser utilizados en tratamientos como la leucemia. Células madre mesenquimatosas que dan origen a condroblastos, osteoblastos y mioblastos.
- 13. CÉLULAS MADRE EMBRIONARIAS (ME) Amplia capacidad de autorrenovación y dan origen a todas las estirpes celulares. Derivan del blastocisto pro lo que sus descendientes portaran moléculas de HLA por lo que inducen al rechazo como en órganos transplantados. Se realizado un gran esfuerzo para producir células semejantes a ME a partir de los tejidos del paciente.
- 15. FACTORES DE CRECIMIENTO Proteínas que estimulan la supervivencia, proliferación, migración y diferenciación celular. Inducen a la proliferación mediante la unión a receptores específicos y afectación a la expresión de genes. Estos productos regulan el ciclo celular. Los factores de crecimiento estimulan la función de varios genes que controlan el crecimiento (protooncogenes).
- 16. Muchos de los factores de crecimiento implicados en la reparación son elaborados por los macrófagos y los linfocitos que se reclutan en los sitios de lesión. Otros son producidos por células parenquimatosas o estromales en respuesta a la lesión celular.
- 17. Mecanismos de señalización de los receptores de factores de crecimiento Factores de crecimiento Receptores específicos en la sup. Celular Activar señales bioquímicas en la célula Estas van a determinar la estimulación o represión de la expresión génica La transmisión de señales pueden ser: Autocrinas Paracrinas Endocrinas
- 18. CLASE DE RECEPTOR LIGANDOS MECANISMOS DE TRANSMICIÓN DE SEÑALES RECEPTORES CON ACTIVIDAD CINASA INTRÍNSECA EGF VEGF FGF HGF • La unión de ligando a la parte extracelular del receptor da la dimerización • Fosforilación los receptores se pueden ligar y activar proteínas intracelulares • Estimulan señales distales y producen proliferación celular RECEPTORES ACOPLADOS A PROTEINA G Múltiples mediadores inflamatorios Hormonas Todas las quimiocinas • 7 segmentos transmembranosos de hélice α • La unión del ligando induce el cambio en la forma inactiva ligada a GDP de la proteína G asociada a la forma activa ligada a GTP • Activa AMPc y utilización de inositol 1,4,3 trifosfato (IP3) libera Ca del RE • Son la familia de receptores mas amplia (1500) RECEPTORES SIN ACTIVIDAD ENZIMATICA INTRÍNSECA Muchas citocinas Interferones HC CSF y EPO • Son moléculas transmembranosas con dominio extracelular a q se une el ligando • la unión del ligando recluta cinasas janus (JAK)que producen fosforilación • activación de factores de transcripcion (STAT)
- 19. la reparación tisular Depende de: • Factores de crecimiento • Interacción entre las células • componentes de la MEC MEC Secuestra agua, lo que da turgencia a los tej. Blando y minerales lo que da rigidez al hueso Regula en las células -Proliferación -Desplazamiento -Diferenciación Da un sustrato para la adhesión y migración de las células Reservorio para los factores de crecimiento
- 20. MEC Remodelación continua Síntesis y degradación forma parte de la morfogenia Cicatrización de herida Fibrosis crónica Invasión y metástasis de tumores
- 21. DOS FORMAS BÁSICAS DE MEC Sintetizado por células mesenquimatos as “alambre de gallinero”
- 22. COMPONENTES DE LA MEC • Colageno • Elastina Proteínas estructurales fibrosas • Proteoglucanos • Hialuronatos Geles hidratados • Conectan los elelementos de la matriz entre otros Glucoproteínas adhesivas
- 23. Colágeno - 3 cadenas poli peptídicas - Esta se unen en forma de soga - 30 tipos de colágenos - Fibrilares (I,II,III,V) -No fibrilares : MB IV, DI IX, uniones DermoE VII Los colágenos fibrilares son importantes en la cicatrización La resistencia de esta se da por los enlaces cruzados unidos con covalentes y la enzima lisilo oxidasa Depende de la Vitamina C El déficit produce
- 24. Elastina Capacidad del tejido de retraerse y recuperar la forma basal - Paredes de los grandes vasos, Útero, piel y ligamentos Constituida Núcleo central de elastina y rodeada de una red glicoproteína fibrilina Defectos en la síntesis de fibrilina Alteraciones esqueléticas y debilidad de las paredes de la aorta
- 25. Proteoglucanos Geles hidratados Aportan elasticidad lubricación Reservorio de factores de crecimiento Formados por polisacáridos largos llamados glucosaminoglucanos unidos a un esqueleto proteico Algunas son proteínas integrales de la membrana celular que ayudan en la proliferación, migración y adhesión de las células Hialuronato Un mucopolisacárido muy grande sin núcleo de proteínas Importante en la MEC ya que se liga al agua u forma una matriz viscosa Da compresibilidad a los tejidos
- 26. Glucoproteínas adhesivas y receptores para la adhesión Vista estructural son moléculas variables Participan en: la adhesión intracelular Unión de células con la MEC Unión entre componentes de la MEC
- 27. Glucoproteínas adhesivas FIBRONECTIN A Heterodímero de 450kda Enlaces de disulfuro sintetizado por diversas células Tienen dominios que se unen a los componente de la MEC También pueden unirse a integrinas a través de un motivo tripéptido RGD PLASMÁTICO: une la fibrina al coagulo de sangre, aportando el sustrato para la reepitelización TISULAR: agregados fibrilares en cicatrización
- 28. LAMININA Glucoproteína mas abundante Heterodimero de 850 KDA En forma de cruz Conecta las células con los elementos de la MEC Unión con la membrana basal Proliferación diferenciación y motilidad de las células
- 29. Receptores para la adhesión Inmunoglobulina s Cadherinas Selectinas Integrinas moléculas de adhesión celular (CAM) En la membrana plasmática de varias celular Se une a la MEC el el motivo RGD e inicia la cascada de señales
- 30. FUNCIONES DE LA MEC Soporte mecánico Control de la proliferación celular Andamiaje para la renovación celular Establecimiento de los microambientes tisulares
- 31. regeneración en la reparación tisular La regeneración dependerá del tipo de tejidos lesionados y la gravedad del daño
- 32. Tejidos lábiles Células sanguíneas remplazadas por células madre hematopoyéticas Proliferación de células residuales y las células madre tisulares Mediado por factores de crecimiento Las células lesionadas son sustituidas con rapidez
- 33. Órganos parenquimatosos Es de proceso limitado Poca capacidad regenerativa
- 34. Resección del 90 % hígado se puede corregir por proliferación de hepatocitos Citocinas (IL-6) Factores del Crecimiento IL-6 1. Sensibilización Previa 2. Fase de Factores de Crecimiento HGF TGF-B 3. Proliferación Celular
- 35. Pasos para la formación de la cicatrización 1. Angiogenia formación de nuevos vasos sanguíneos 2. Formación de tejido de granulación Migración y proliferación de fibroblastos, deposito tejido conjuntivo, los vasos y los leucocitos 3. Reorganización del tejido fibroso para generar una cicatriz fibrosa estable
- 36. Tejido de granulación Cicatriz madura
- 37. Angiogenia Desarrollo de nuevos vasos a partir de existentes Permite que los tumores aumente de tamaño Curación en el foco de lesión Circulación colateral en los casos de isquemia
- 38. Pasos para la angiogeia Vasodilatación Permeabilidad Separación del pericito Migración y proliferación de las células endoteliales Formación de tubos Reclutamiento de células peri endoteliales Supresión de la proliferación endotelial. n NO VEGF Degradación Membrana Basal
- 40. Factores de Crecimiento implicados en la Angiogenia: VEGF FGF Angiopoyetinas
- 41. Factores de crecimiento implicados en la angiogenia Familia VEGF incluye los de tipos A a E y el factor de crecimiento placentario (PIGF). VEGF-A o VEGF es inductor de la angiogenia tras una lesión y en los tumores EGF-B y el PIGF participan en el desarrollo de los vasos en el embrión Se unen a una familia de receptores de tirosina cinasa Importante VEGFR-2 VEGF se expresan en tejidos adultos, células epiteliales adyacentes al epitelio fenestrado VEGF-C y el VEGF-D estimulan tanto la linfangiogenia como la angiogenia
- 42. VEGF estimula la migración y la proliferación de las células endoteliales Produce vasodilatación mediante la estimulación de la producción de NO Los anticuerpos para la VEGF han sido aprobados como tratamiento de algunos tumores Los dependen de la angiogenia para su diseminación y crecimiento.
- 43. Familia FGF más de 20 miembros los mas importantes FGF-1 (FGF ácido) y el FGF-2 (FGF básico) son producidos por varios tipos celulares se unen a receptores de la membrana plasmática con actividad tirosina cinasa FGF-2 esta en la angiogenia en la estimulación de la proliferación de las células endoteliales induce la migración de los macrófagos y fibroblastos hacia el área lesionada estimula la de las células epiteliales para cubrir las heridas epidérmicas.
- 44. Angiogenia Maduración de los nuevos vasos Ang1 interactúa con un receptor tirosina cinasa en las células endoteliales, llamado Tie2. el TGF-B suprime la proliferación y migración de las células endoteliales el PDGF recluta a las células musculares lisas Angiopoyetinas
- 45. En el embrión se llaman vasculogenia Hemangioblastos Angioblastos Precursor del sistema hematopoyetico
- 46. El depósito de tejido conjuntivo Aposición tejido conjuntivo Migración y proliferación de de Fibroblastos en sitio de la lesion Deposito de proteínas de la MEC Mediado por Citocinas Factores del crecimiento el PDGF, FGF-2 y TGF-B. Macrófagos, mastocitos presentes en el tejido de granulación. producen
- 47. Factores de crecimiento implicados en el depósito de MEC y en la formación de cicatriz El factor transformador del crecimiento B (TGF-B) familia de poli péptidos homólogos TGF-B1, TGF-B2 y TGF-B3 El factor activo se liga a dos receptores en la superficie celular con actividad serina- treonina cinasa estimula la fosforilación de unos factores de transcripción denominados Smad
- 48. TGF-B Citocina antiinflamatoria Limitar y termina la respuesta inflamatoria Inhibe proliferación de los linfocitos actividad de otros leucocitos TGF-B Estimula la producción colágeno, fibronectina y proteoglucanos Inhibe la degradación del colágeno Inhibidores metaloproteinasas
- 49. Factor de crecimiento derivado de las plaquetas (PDGF) familia de proteínas estrechamente relacionadas con 2 cadenas llamadas A y B se ligan a receptores que se llaman PDGFR-A y PDGFR-B almacenado en las plaquetas y liberado cuando estas se activan producen las células endoteliales, los macrófagos activados, las células musculares lisas y células tumorales. provoca la migración y la proliferación de fibroblatos Citocinas Pueden comportarse como factores de crecimiento participan en el depósito de MEC y en la formación de cicatrices la lL-1 y 13 actúan sobre los fibroblastos estimulando la síntesis de colágeno
- 50. Remodelado del tejido conjuntivo Después de la síntesis y depósito, el tejido conjuntivo de la cicatriz sigue modificándose y remodelándose Resultado final del proceso de reparación es el equilibrio entre la síntesis y la degradación de las proteínas de la MEC.
- 51. La degradación del colágeno y de otros componentes de la MEC se realiza por una familia de metaloproteinasas de la matriz (MMP), dependen del cinc Estromelisinas (tipos 3,10 y 11) degradan una serie de elementos de la MEC Gelatinasas (tipos 2 y 9) degradan el colágeno amorfo y la fibronectina Las MMP Colagenasas intersticiales (tipos 1 a 3) degradan el colágeno fibrilar
- 52. MMP Producidos por fibroblastos, macrófagos, neutrófilos, células sinoviales y algunas células epiteliales síntesis y secreción reguladas por factores de crecimiento, citocinas pueden ser rápidamente inhibidas inhibidores tisulares de metaloproteinasas (TIMP) se activan para remodelar la MEC depositada, después su actividad es interrumpida por los TIMP.
- 53. Factores que influyen en la reparación tisular Infección Nutrición glucocorticoides Variables mecánicasMala perfusiónCuerpos extraños Tipo y extensión de la lesión tisular Localización de la lesión y las características del tejido donde se a producido Alteraciones del crecimiento celular y de la producción de MEC
- 54. Excesivo deposito de colágeno en la piel que da lugar a una cicatriz elevada Deposito de tejido conjuntivo denso en la Dermis
- 56. Regeneración epitelial Formación de una cicatriz de tejido conjuntivo CICATRIZACIÓN DE HERIDAS CUTÁNEAS
- 57. CICATRIZACIÓN POR PRIMERA INTENCIÓN Lesión capa epitelial Regeneración epitelial Cicatrización de una incisión quirúrgica Limpia no infectada Muerte de pocas células de tejido epitelial y conjuntivo
- 58. Rotura focal de la continuidad de la membrana basal epitelial Muerte de un número pequeño de c. epiteliales y tejido conjuntivo El espacio de la incisión es ocupado por sangre con coagulo de fibrina Que es invadido por tejido de granulación y cubierto de epitelio nuevo CICATRIZACIÓN POR PRIMERA INTENCIÓN
- 59. Las c. basales en el margen muestra una mayor actividad mitótica Estos van a migrar hacia el coagulo de fibrina Se encuentran neutrófilos en el de la incisión
- 60. Las c. epiteliales de los márgenes migran y proliferan siguiendo la dermis Las células se encuentran en la línea media por debajo de la costra cutánea Consiguiendo así una capa delgada pero continua de epitelio
- 61. Gran parte de los neutrófilos son sustituidos por macrófagos El tejido de granulación invade el espacio de la incisión Proliferación de c. epiteliales por lo que hay una capa epidérmica gruesa
- 62. Neovascularización cuando el tejido de granulación llena el espacio de la incisión Migración de Fibroblastos Producen proteínas de la MEC Fibrillas de colágeno mas abundantes Epidermis recupera su espesor normal
- 63. Se sigue acumulando colágeno Proliferan fibroblastos Infiltrado de leucocitos, edema y disminuyen Comienza el proceso blanqueamiento
- 64. La cicatriz es tejido conjuntivo celular Casi exento de c. inflamatorias Revestido por una epidermis normal
- 65. CICATRIZACIÓN POR SEGUNDA INTENCIÓN Cuando la herida es más intensa como en úlceras, abscesos, necrosis isquémica Inflamación más intensa Abundante tejido de granulación Formación de una cicatriz grande o de granulación Contracción de la herida mediada por miofibroblastos
- 66. Se forma una costra más grande rica en fibrina y fibronectina Los defectos tisulares son más grandes, tienen mas restos necróticos exudado y fibrina Se necesita más tejido de granulación para rellenar los tejidos y así haya recrecimiento del epitelio.
- 67. MATRIZ PROVISIONAL Fibrina, plasma, fibronectina colágeno III Tejido de Granulación Cicatriz avascular Final del primer mes Epidermis intacta Implica la contracción de la herida
- 68. Las heridas bien saturadas tiene un 70% de resistencia Se recupera la d tensión cuando la síntesis de colágeno excede a la degradación La herida recupera 70-80% de la resistencia normal a los 3 meses
- 69. Depósito excesivo de colágeno y otros componentes de la MEC en un tejido Los mecanismos son los mismos que se producen en la formación de una cicatriz Esta se induce por estimulos lesivos persistentes Como las infecciones, las reacciones inmunológicas y otros tipos de lesión tisular
- 70. BIBLIOGRAFÍA William Rojas, Juan Manuel Anaya, Beatriz Aristizábal, Luz Elena Cano, Luis Miguel Gómez, Damaris Lopera. (2012). Inmunología de Rojas (17 edición). Medellín- Colombia. Ed. Corporación para Investigaciones Biológicas Vinay Kumar, Abula K. Abbas, Nelson Fausto and Richard Mitchell. (2012). Patología estructural y funcional de Robbins y Cotran. (8 edición). Madrid- España. Editorial Elsevier Ivan Roitt, Petter J. Delves M. Inmulogía: fundamentos. 2003. Buenos Aires, Argentina, Médica Panamericana Benezer, M., Mercado, E. & Pineda E. (2008). La Producción de Especies Reactivas de Oxígeno Durante la Expresión de la Resistencia a Enfermedades en Planta. Rev. mex. fitopatol vol.26 no.1 Texcoco MUÑOZ, D. R. (21 de 10 de 2015). NOTAS para el estudio de endocrinología. Obtenido de http://www.iztacala.unam.mx/rrivas/NOTAS/Notas7Patpulpar/infcronica.html
