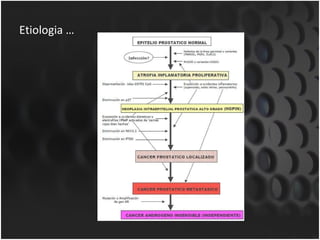
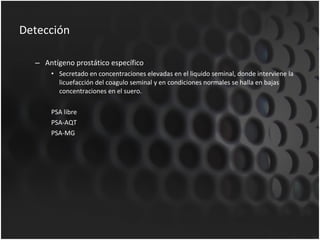
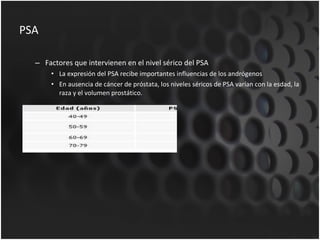
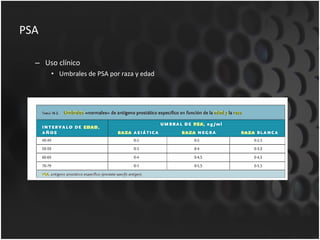
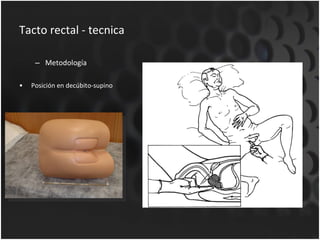
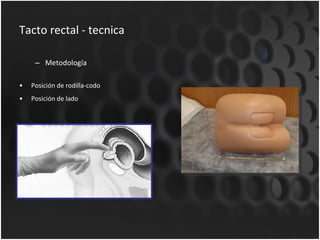
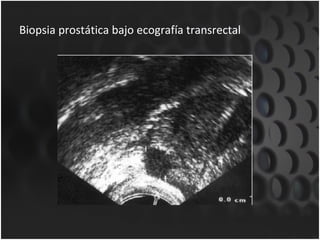
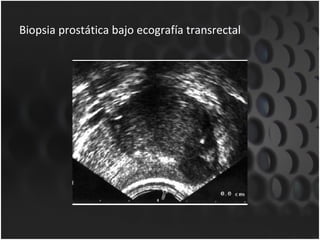
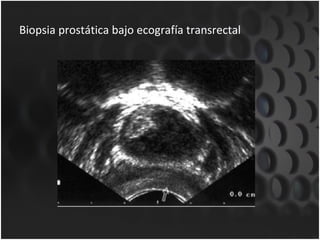
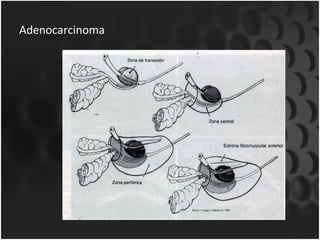
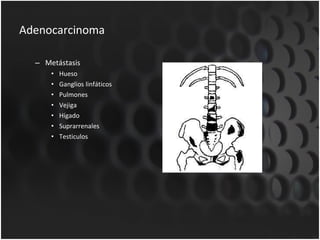
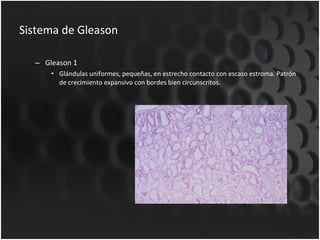
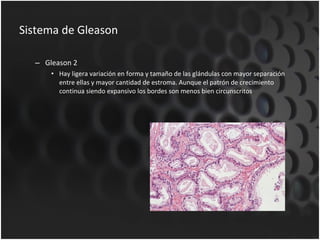
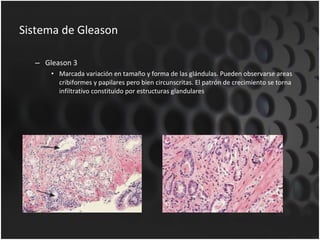
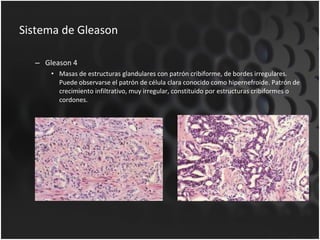
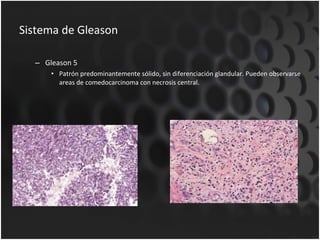
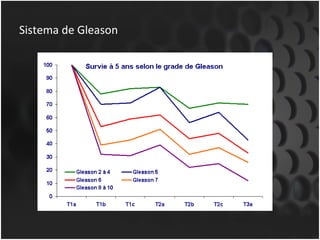
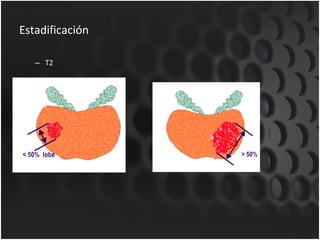
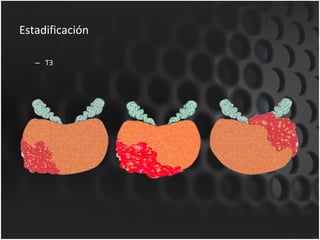
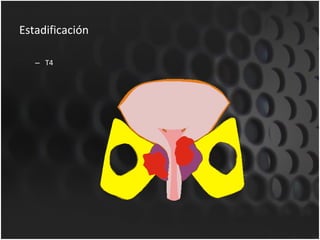
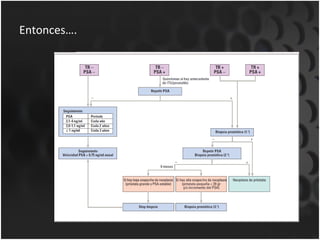
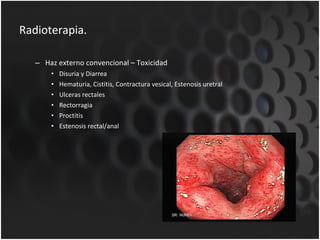
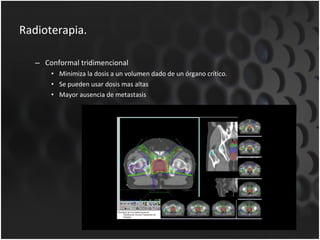
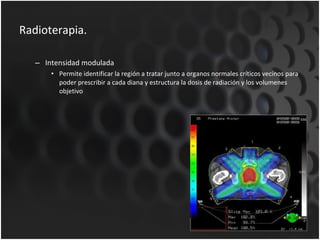
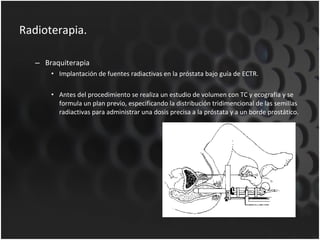
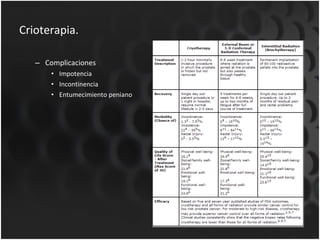
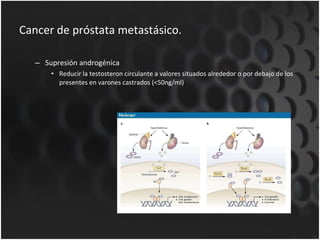
Este documento proporciona información sobre el cáncer de próstata, incluyendo su epidemiología, factores de riesgo, detección, diagnóstico, anatomía patológica y tratamientos. El cáncer de próstata es común y de lenta progresión, y su detección se realiza principalmente a través de pruebas de PSA y tacto rectal. El diagnóstico incluye biopsia prostática guiada por ecografía transrectal para confirmar el cáncer y determinar su grado y extensión mediante sistem