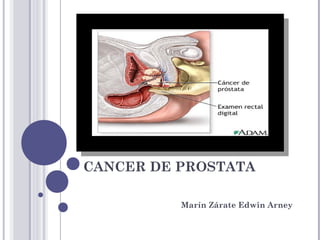
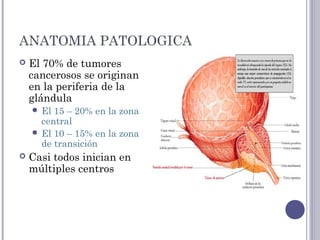
El cáncer de próstata es el tercer tumor más frecuente en varones y la tercera causa de muerte por cáncer. Su etiología es multifactorial, incluyendo factores genéticos, hormonales y ambientales. El diagnóstico se basa en el antígeno prostático específico y la biopsia prostática. El tratamiento depende del estadio y grado del cáncer, e incluye vigilancia activa, prostatectomía radical, radioterapia, braquiterapia y terapia hormonal.