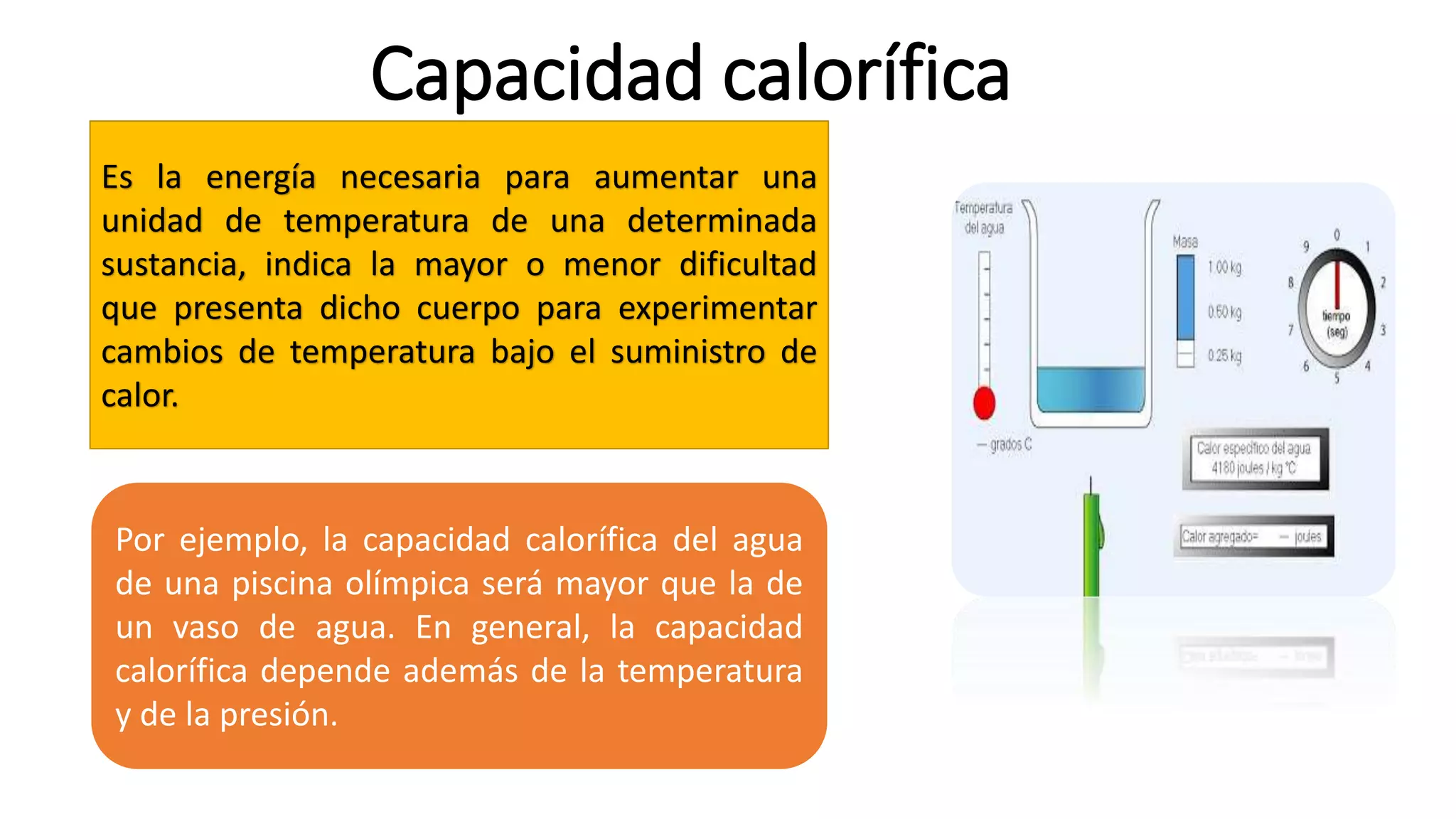
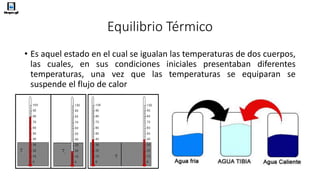
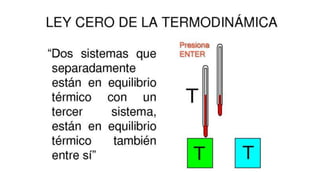
La capacidad calorífica indica la facilidad con que un cuerpo cambia su temperatura al absorber o ceder calor. Depende de factores como la sustancia, su temperatura y presión. Para los gases ideales, la capacidad calorífica depende además de si se mide a volumen o presión constante. Cuando dos cuerpos a distintas temperaturas entran en contacto, transfieren calor hasta alcanzar el equilibrio térmico a una temperatura común.