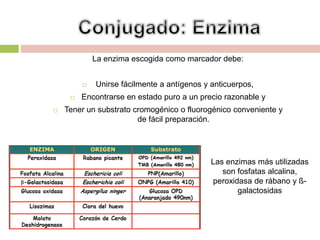
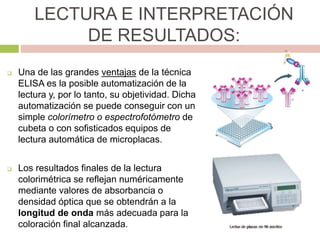
El documento describe la prueba de ELISA (Ensayo Inmunoadsorbente Ligado a Enzimas). ELISA utiliza anticuerpos o antígenos marcados con enzimas para detectar la presencia de analitos como proteínas, hormonas o microorganismos. El procedimiento involucra fijar el antígeno o anticuerpo objetivo a una placa, luego agregar la muestra, anticuerpos o antígenos conjugados con enzimas, y finalmente un sustrato que produzca un cambio de color detectable. ELISA se usa ampliamente en medic