Incrustar presentación

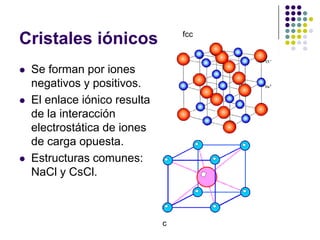
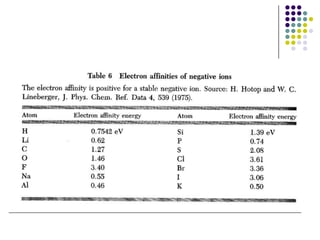




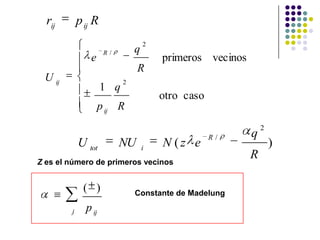

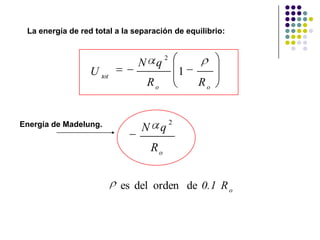

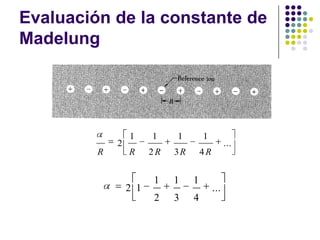

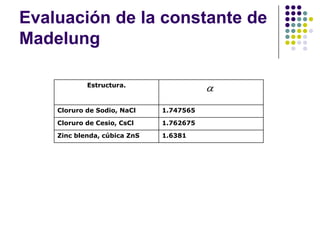
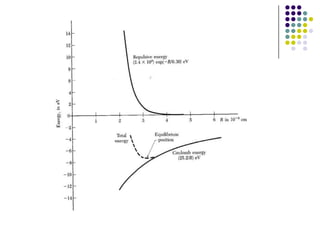
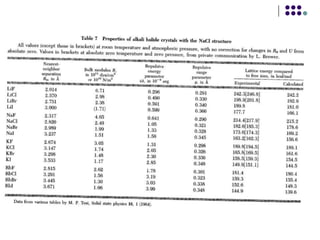

El documento describe los enlaces iónicos en cristales formados por iones con cargas opuestas. Los cristales iónicos como NaCl y CsCl tienen estructuras cristalinas comunes y su principal energía de enlace proviene de la interacción electrostática entre iones, conocida como energía de Madelung.















