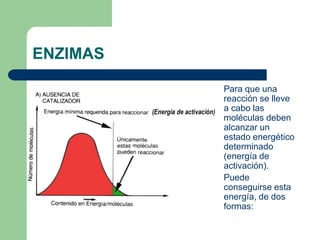
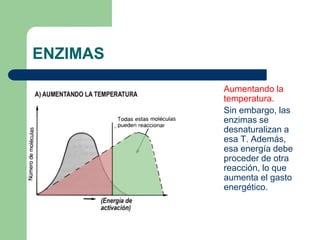
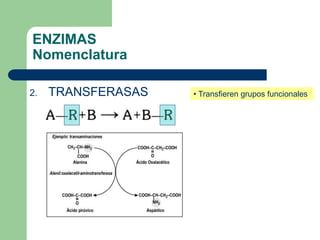
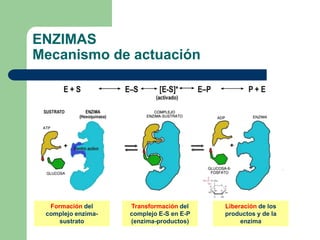
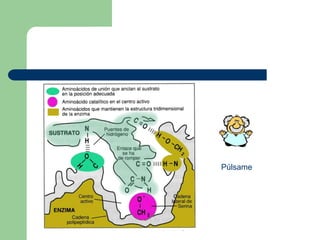
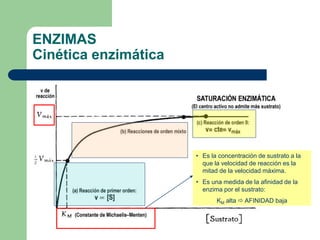
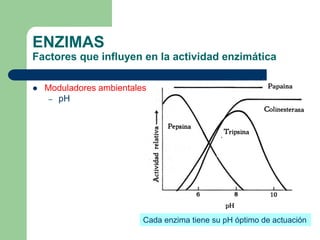
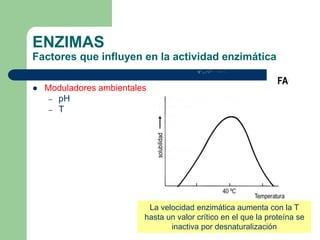
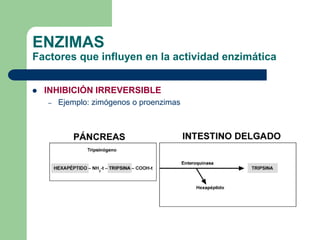
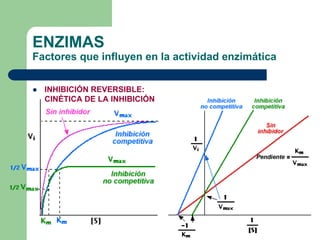
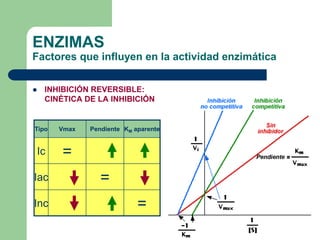
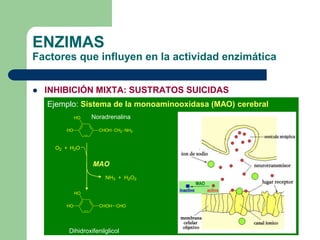
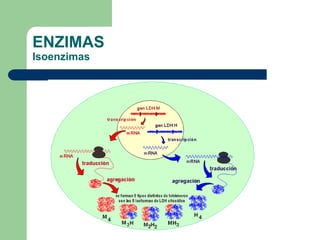
Este documento trata sobre las enzimas. Brevemente, explica que las enzimas son proteínas que actúan como catalizadores, rebajando la energía necesaria para que las reacciones bioquímicas ocurran. También describe algunas propiedades clave de las reacciones enzimáticas, como su alta eficiencia, especificidad y capacidad de regulación. Por último, resume los principales factores que influyen en la actividad enzimática, como el pH, la temperatura, los cofactores y la regulación alostérica o isoestérica