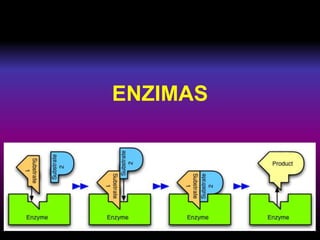
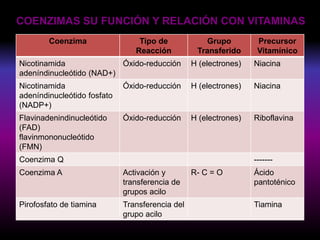
Las enzimas son proteínas globulares que catalizan reacciones químicas específicas. Pueden requerir cofactores como metales o grupos prostéticos para su actividad óptima. Las enzimas se unen a sus sustratos de forma específica, reduciendo la energía de activación de la reacción catalizada. Existen diferentes clasificaciones de enzimas según el tipo de reacción catalizada y grupos involucrados en la transferencia.