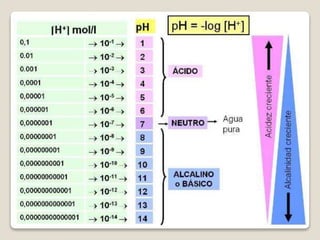
El documento trata sobre el equilibrio ácido-base en el cuerpo. Brevemente explica que el pH mide la concentración de iones de hidrógeno, y que el cuerpo mantiene la homeostasis a través de la regulación renal del bicarbonato y la compensación respiratoria del dióxido de carbono. Las alteraciones metabólicas que cambian el pH incluyen un aumento en la generación de iones hidrógeno o una pérdida de bicarbonato.



![ El pH indica la
concentración iónes
libres de hidrógeno
[H3O+] presentes en
una sustancia.
La palabra pH es la
abreviatura de "pondus
Hydrogenium".
literalmente el peso
del hidrógeno.](https://image.slidesharecdn.com/equilibrioacidobase-141209110806-conversion-gate02/85/Equilibrio-acido-base-4-320.jpg)