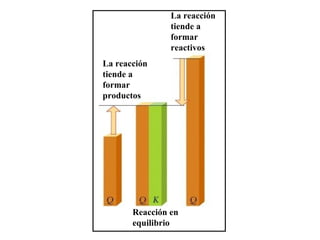
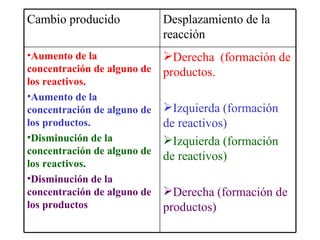
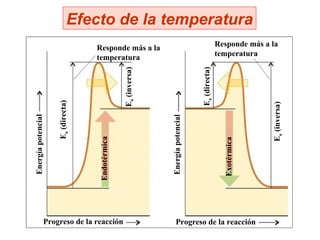
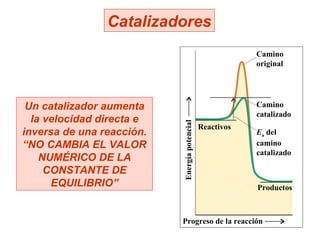
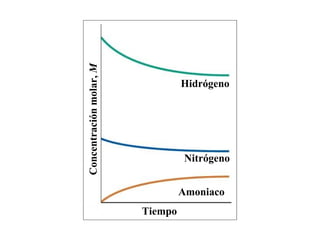
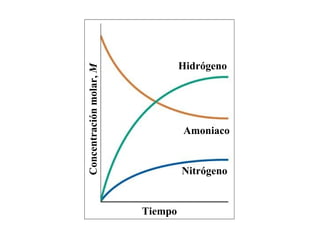
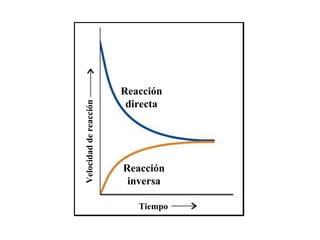
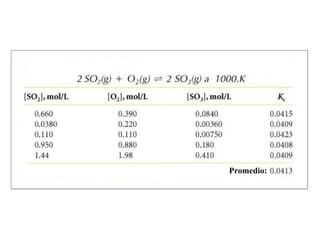
El documento describe los conceptos básicos de equilibrio químico, incluyendo las reacciones directa e inversa, la constante de equilibrio y cómo los factores como la concentración de reactivos y productos, la presión, la temperatura y los catalizadores afectan el equilibrio químico. Explica que el equilibrio químico se alcanza cuando las velocidades de la reacción directa e inversa son iguales, y que la constante de equilibrio predice la dirección preferida de la reacción y permite calcular las concent








![Equilibrios Heterogéneos Se habla de reacción homogénea cuando tanto reactivos como productos se encuentran en el mismo estado físico. En cambio, si entre las sustancias que intervienen en la reacción se distinguen varias fases o estados físicos, hablaremos de reacciones heterogéneas. Por ejemplo, la reacción: CaCO3 (s) ↔ CaO (s) + CO2 (g) se trata de un equilibrio heterogéneo. Aplicando la ley de acción de masas se cumplirá que: [CaO] · [CO2] K (constante) = ——————— [CaCO3] K C = [CO2]](https://image.slidesharecdn.com/equilibrioqumico-090910221941-phpapp02/85/Equilibrio-QuiMico-14-320.jpg)