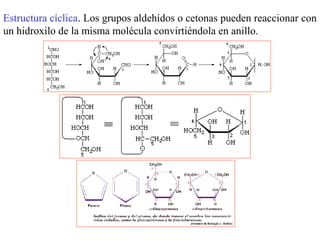
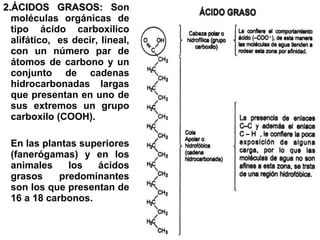
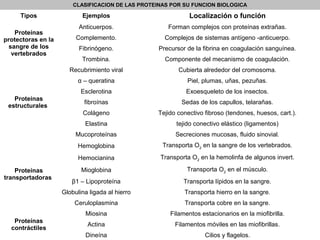
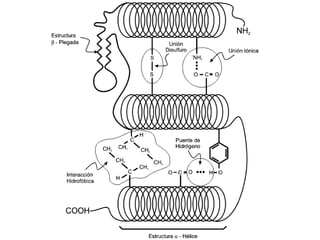
Este documento describe los glúcidos o carbohidratos, incluyendo su estructura química, clasificación, funciones y ejemplos importantes. Los glúcidos son biomoléculas formadas por carbono, hidrógeno y oxígeno que cumplen funciones estructurales, energéticas y de almacenamiento. Se clasifican en monosacáridos, disacáridos, oligosacáridos y polisacáridos. Algunos ejemplos importantes son la glucosa, almidón, celulosa y ácidos