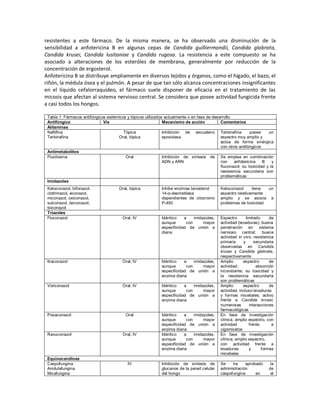
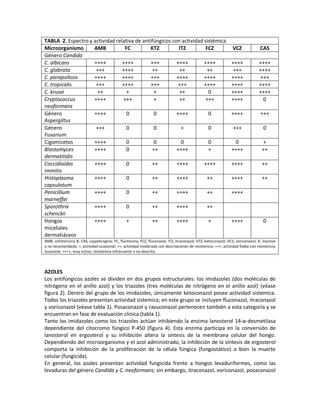
El documento describe los principales fármacos antifúngicos disponibles, incluyendo anfotericina B, formulaciones lipídicas de anfotericina B, triazoles como fluconazol e itraconazol, y equinocandinas como caspofungina. Anfotericina B y sus formulaciones lipídicas actúan uniéndose al ergosterol de la membrana fúngica, mientras que otros fármacos inhiben enzimas involucradas en la síntesis de componentes de la pared celular fúngica. Estos fárm