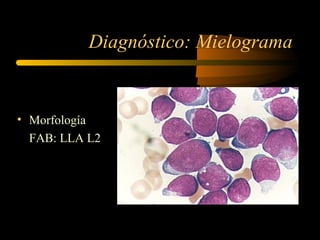
La leucemia linfoblástica aguda es una enfermedad causada por la proliferación anormal de células linfoides inmaduras en la médula ósea. Se diagnostica mediante análisis de médula ósea y se estratifica el riesgo según factores clínicos e histopatológicos. El tratamiento consiste en quimioterapia para inducción de remisión, consolidación e intensificación, así como mantención a largo plazo para prevenir recaídas.