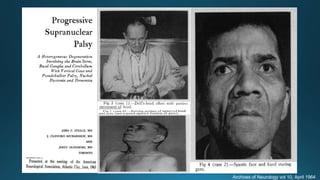
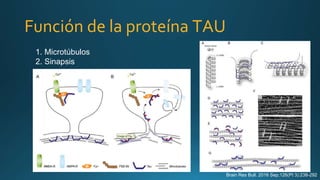
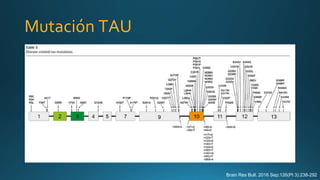
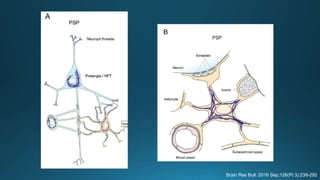
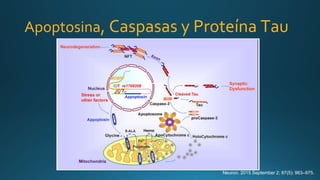
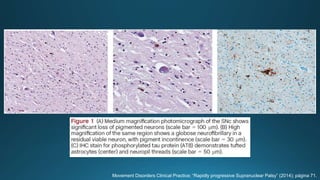
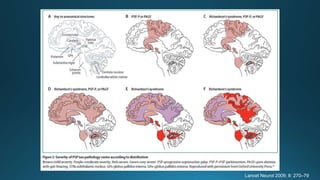
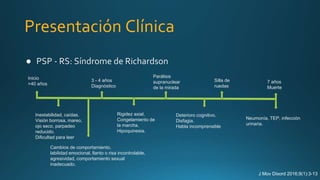
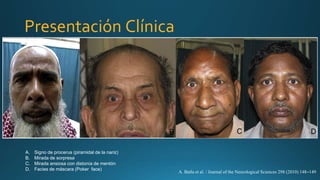
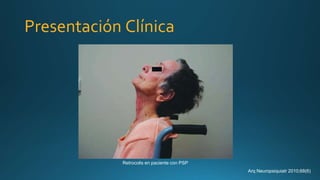
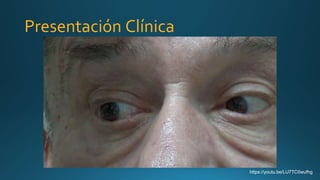
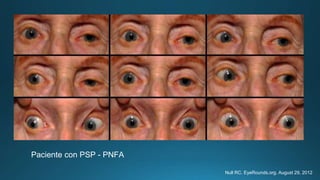
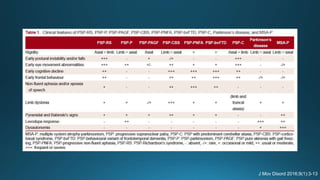
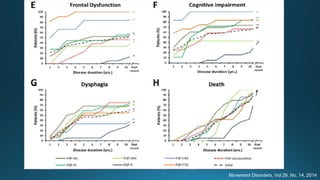
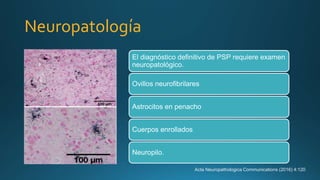
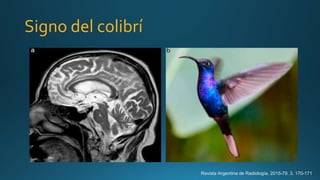
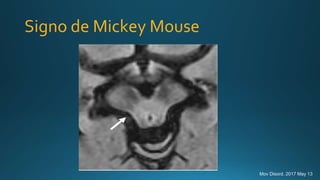
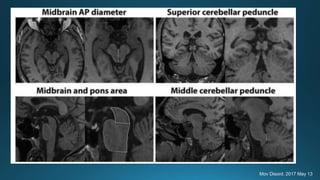
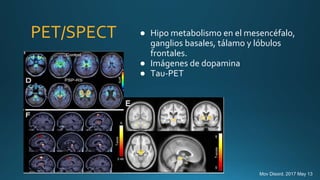
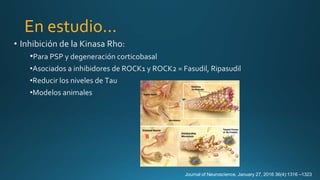
Este documento resume la parálisis supranuclear progresiva (PSP), incluyendo su historia, epidemiología, fisiopatología, presentación clínica, diagnóstico, tratamiento y opciones terapéuticas. La PSP se caracteriza por acumulaciones anormales de proteína tau en el cerebro que causan inestabilidad postural progresiva y parálisis de la mirada supranuclear. El diagnóstico definitivo requiere examen neuropatológico y se apoya en criterios clínicos como la neuroimagen