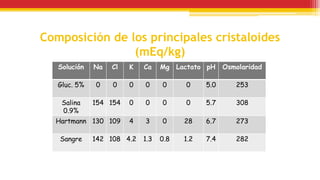
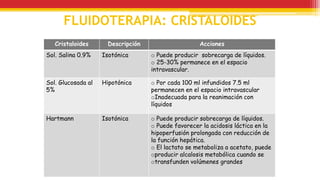
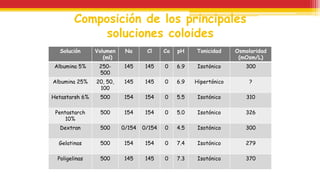
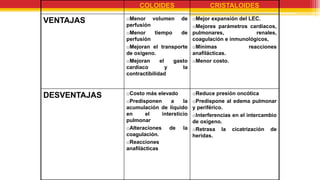
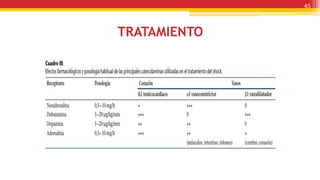
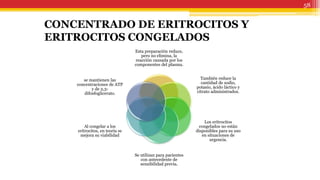
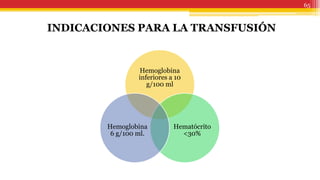
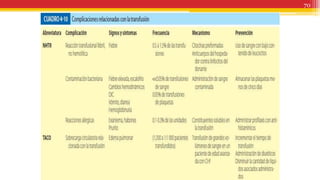
El documento trata sobre el shock y la terapia transfusional, definiendo el shock como un síndrome de perfusión sistémica inadecuada que puede ser causado por diversos factores. Se describen las diferentes formas de shock, sus causas, fisiopatología, diagnóstico y tratamiento, resaltando la urgencia en la reposición de líquidos y sangre para evitar daño multiorgánico. La transfusión de sangre, introducida a fines del siglo XIX, se fundamenta en principios de compatibilidad sanguínea establecidos por la identificación de grupos y factores Rh.