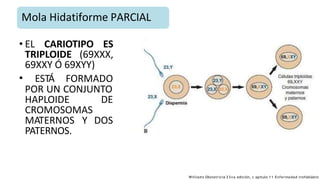
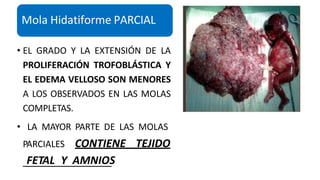
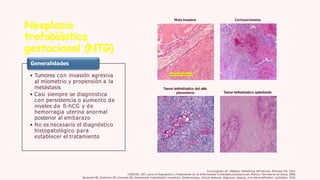
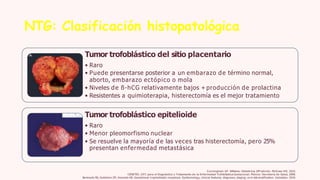
La enfermedad trofoblástica gestacional (ETG) incluye un grupo de condiciones relacionadas con la placenta, como mola completa, mola parcial y coriocarcinoma. Se presenta con niveles elevados de hCG y puede involucrar complicaciones graves, requiriendo diagnóstico y tratamiento oportuno para prevenir metástasis. El manejo incluye quimioterapia, y el seguimiento es crucial para evaluar la respuesta al tratamiento y la remisión.