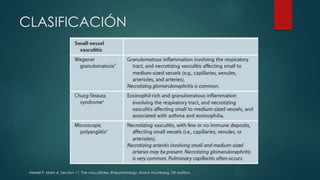
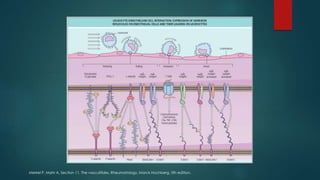
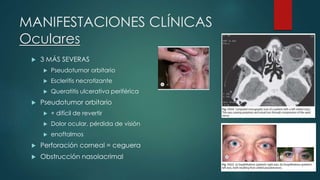
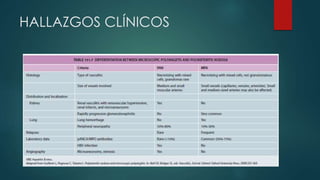
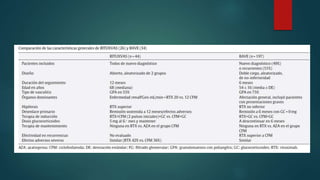
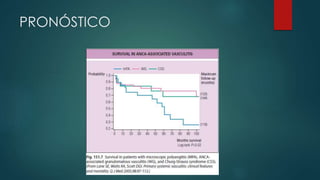
El documento aborda las vasculitis ANCA, enfocándose en la granulomatosis con poliangitis y poliangeítis microscópica, características clínicas, epidemiología, fisiopatología, clasificación, diagnóstico y tratamiento. Se describe cómo estas enfermedades inflaman los vasos sanguíneos, causando daño en diversos órganos y sus manifestaciones clínicas, como problemas respiratorios y renales. El tratamiento incluye medicamentos como ciclofosfamida y rituximab, además de abordar las recaídas y complicaciones asociadas.