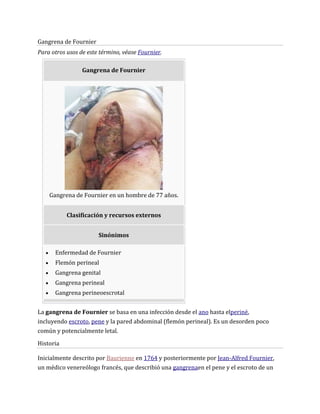
Gangrena de fournier
- 1. Gangrena de Fournier Para otros usos de este término, véase Fournier. Gangrena de Fournier Gangrena de Fournier en un hombre de 77 años. Clasificación y recursos externos Sinónimos Enfermedad de Fournier Flemón perineal Gangrena genital Gangrena perineal Gangrena perineoescrotal La gangrena de Fournier se basa en una infección desde el ano hasta elperiné, incluyendo escroto, pene y la pared abdominal (flemón perineal). Es un desorden poco común y potencialmente letal. Historia Inicialmente descrito por Baurienne en 1764 y posteriormente por Jean-Alfred Fournier, un médico venereólogo francés, que describió una gangrenaen el pene y el escroto de un
- 2. paciente en 1883 como un proceso gangrenoso de origen desconocido. Recibió apelativos tales como: «erisipela gangrenosa», «gangrena estreptocóccica del escroto» o «gangrena idiopática». Etiología Actualmente, sabemos que está causada por una infección bacteriana mixta en la que intervienen gérmenes aerobios y anaerobios. Fisiopatología La gangrena de Fournier mantiene debilitado el sistema inmunológico, en particular en pacientes afectos de alcoholismo crónico, diabetes mellitus y enfermedades tumorales malignas. Tratamiento El tratamiento consiste en la administración de antibióticos y en el desbridamiento mediante cirugía de las áreas en las que los tejidos han sido destruidos por la necrosis. La enfermedad presenta una alta tasa de mortalidad.1 RESUMEN La gangrena de Fournier es un proceso infeccioso-necrotizante de la piel del área perineogenital, que afecta a los hombres, fundamentalmente en la sexta y séptima décadas de la vida. La flora aislada en los cultivos de la lesión necrótica suele ser polimicrobiana, hallándose microorganismos aerobios y anaerobios en la mayoría de los casos. La Escherichia coli es el germen más frecuentemente identificado. Si bien en otra época, era considerada como un trastorno idiopático, en la actualidad se identifica un factor precipitante genitourinario, anorrectal o dérmico, en la mayoría de los pacientes. Existen una serie de trastornos sistémicos debilitantes del huésped, como la diabetes mellitus, el alcoholismo crónico y las neoplasias malignas, entre otros, que se asocian a esta enfermedad, y que pueden considerarse como factores de riesgo de la misma. La gangrena de Fournier en la infancia presenta unas características bacteriológicas, patogénicas, clínicas, terapéuticas y pronósticas específicas, que la diferencian de la gangrena del adulto. El tratamiento universalmente aceptado para este proceso, consiste en antibioterapia parenteral de amplio espectro y desbridamiento quirúrgico temprano y agresivo de las áreas necróticas. La tasa de mortalidad sigue siendo elevada, situándose entre el 20 y el 80%, según las series.
- 3. Finalmente, realizamos el análisis de un grupo de 7 pacientes con gangrena de Fournier (1991-1998), con el propósito de efectuar una comparación entre nuestros resultados y los observados en las series más recientes. La gangrena de Fournier es una fascitis necrotizante de etiología infecciosa, que afecta a la piel y al tejido celular subcutáneo, de comienzo súbito, y diseminación rápidamente progresiva. Se origina en escroto, pene o periné, y se extiende con cierta frecuencia a la pared abdominal anterior1-7. Esta lesión necrótica e infecciosa cutánea, aunque fue inicialmente descrita por Baurienne en 17641, debe su nombre a Jean Alfred Fournier, un venereólogo francés, quien en 1883 definió sus características, a partir del estudio de una serie personal de 5 casos, que se caracterizaban por: comienzo súbito de dolor escrotal en pacientes jóvenes y previamente sanos; progresión rápida hacia la gangrena cutánea; ausencia de etiología definida o evidente2,8-11. Se trata de una entidad de presentación infrecuente, con un número estimado de 600 casos descritos en la literatura 5,10,11, y una incidencia aproximada de un caso por cada 7.500 ingresos urológicos5,10. Aunque Fournier asimiló al proceso gangrenoso una etiología idiopática y lo describió en varones jóvenes, actualmente, los mecanismos patológicos y el foco infeccioso de la enfermedad, son identificados en la gran mayoría de los pacientes. El proceso afecta en la actualidad, a hombres por encima de los 50 años3,5,6,11,12, con trastornos sistémicos subyacentes. La mortalidad generada por la gangrena de Fournier, que alcanza el 80% en alguna de las series revisadas, pone de manifiesto la naturaleza especialmente agresiva del proceso6-10. MANIFESTACIONES CLÍNICAS Aunque en la descripción inicial de la gangrena de Fournier se identificaba el proceso con el grupo de los varones jóvenes, las publicaciones realizadas desde entonces, muestran un incremento progresivo de la edad media de los pacientes afectos. Puede decirse que en la mayoría de las series actuales, la edad media supera los 60 años2,3,5,6. En la actualidad, es excepcional encontrar este tipo de patología en recién nacidos o pacientes jóvenes. Algunos autores relacionan la edad con el pronóstico, y encuentran un mayor número de complicaciones y de mortalidad en los pacientes de mayor edad5-7. El intervalo de tiempo transcurrido desde el inicio de los síntomas específicos del proceso, hasta la solicitud de atención médica es de 2 a 7 días, por término medio3,9,22. Este periodo de tiempo determina la extensión del área necrótica e influye decisivamente en el pronóstico.
- 4. Es de vital importancia diagnosticar a los pacientes en fases tempranas de la enfermedad, aún cuando los síntomas y signos son mínimos, ya que el pronóstico se relaciona con la extensión y tiempo de evolución de la enfermedad3,5,6. Se ha observado que los pacientes de mayor edad tienen un comienzo más insidioso de la enfermedad, con un mayor intervalo desde la aparición de los primeros síntomas, hasta el desarrollo de la necrosis cutánea11. Los síntomas de presentación más habituales de la gangrena de Fournier son los de una celulitis, con dolor local, eritema, edema, aumento de tamaño del área escrotopeneana e inflamación del periné, precedidos o acompañados por fiebre o febrícula7,9-11. Si la lesión se deja evolucionar sin tratamiento, a los 3-4 días se produce gangrena cutánea (Fig. 1), con aparición de mal olor y disminución del dolor local, probablemente por destrucción de las ramas nerviosas sensitivas de la piel5,10,11. A medida que el tiempo transcurre y la lesión progresa, se va delimitando perfectamente el área necrótica, y aproximadamente a los 8-10 días del inicio de los síntomas, se aprecia un borde nítido, que la separa de la piel sana adyacente5,11. FIGURA 1. Lesión necrótica avanzada, con extensión hacia el área inguinal, respetando la piel peneana. La crepitación a la palpación del área perineo-genital, producida por enfisema subcutáneo, es un signo frecuente3,6,13,43, y se produce por el acúmulo subcutáneo de hidrógeno y nitrógeno, gases de baja solubilidad, producto del metabolismo de gérmenes anaerobios10,14. El enfisema puede extenderse en dirección posterior, hacia las nalgas, en dirección caudal, hacia el muslo, o en dirección craneal, a través de la pared abdominal anterior, alcanzando incluso la región axilar6,10,11. Náuseas, vómitos, escalofríos y postración son síntomas que también aparecen con frecuencia, reflejando la afectación sistémica producida por el cuadro infeccioso. Desde el punto de vista analítico, los pacientes suelen presentarse con leucocitosis y neutrofilia. Suele existir hiperglucemia, por la condición diabética de muchos pacientes y el cuadro infeccioso asociado. No es infrecuente una presentación inicial en forma de sepsis, con leucocitosis, coagulopatía, fiebre e hipotensión, e incluso cuadros de shock séptico, que suelen ser la causa de la muerte del enfermo 3,7,10.
- 5. ETIOLOGÍA Y FACTORES DE RIESGO La gangrena de Fournier se asocia a una serie de trastornos sistémicos subyacentes, que podemos considerar factores de riesgo 3,5,11,22. La diabetes mellitus, el alcoholismo crónico, las neoplasias malignas, el trasplante de órganos y la infección por VIH, son las patologías más habitualmente relacionadas con la gangrena de Fournier 4,10,16-18. Se trata en general de condiciones debilitantes, y estados de inmunodepresión, en los cuales los procesos infecciosos adquieren una difusión y una gravedad mayor que en la población sana 5,13,22,41. La diabetes mellitus afecta al 20-66% de los pacientes con gangrena de Fournier 5,10,13,14,29,33, siendo el factor predisponente más frecuentemente asociado a este proceso infeccioso. La diabetes constituye un factor de riesgo de padecer gangrena de Fournier por la especial susceptibilidad de estos enfermos a desarrollar infecciones bacterianas. Las razones que explican esta susceptibilidad son básicamente tres: 1) Defecto inherente en la fagocitosis, fundamentalmente la llevada a cabo por neutrófilos. 2) Neuropatía diabética con afectación del tracto urinario, como parte de un trastorno generalizado, produciendo una disfunción vesical neurógena, con el consiguiente defecto de vaciado y una mayor incidencia de infecciones urinarias. 3) Enfermedad microvascular generalizada precoz, de etiología arterioesclerótica, que afecta entre otros, a los pequeños vasos del tejido subcutáneo, produciendo una situación de isquemia crónica5,9,10,14,22. El alcoholismo crónico constituye el segundo gran factor de riesgo implicado en la etiología de la gangrena de Fournier. Su prevalencia entre los pacientes afectos de esta enfermedad es del 20- 60%9,10,13,14,29, según las publicaciones revisadas. Los motivos por los cuales el alcoholismo predispone al desarrollo de este proceso, se derivan de los trastornos inmunitarios y la disfunción hepática que presentan estos enfermos. El alcoholismo ha sido asociado a un peor pronóstico, especialmente en aquellos pacientes que presentan simultáneamente diabetes mellitus5. Los pacientes con neoplasias malignas también muestran una mayor predisposición a desarrollar gangrena de Fournier, bien por la enfermedad neoplásica en sí5,6,15,19,22, o bien por la quimioterapia utilizada para llevar a cabo el tratamiento de la misma3,16,22. Ambas situaciones comportan un estado de inmunosupresión, que facilitan el desarrollo de infecciones graves. El trasplante de órganos3,13,18, la infección por VI3,13,17, la malnutrición y el bajo nivel socioeconómico3,13, el lupus eritematoso43, la viruela23, la vasculitis por hipersensibilidad24, la infección filarial en África3,13,34 y ciertos déficits neurológicos sensitivo-motores como paraplejia, hemiplejia y tetraplejia5, son algunos de los factores asociados a la gangrena de Fournier, citados en la revisión bibliográfica efectuada.
- 6. FACTORES PRECIPITANTES Y DISEMINACIÓN DEL PROCESO El análisis de los factores precipitantes de la gangrena de Fournier, pone de manifiesto que la mayoría de los casos son secundarios a uno de los mecanismos siguientes: 1) Trastorno genitourinario, predominantemente uretral, acompañado o no de infección urinaria, que origina una infección de las glándulas periuretrales; o bien afectación por contigüidad del escroto, en aquellos pacientes con orquitis o epididimitis. 2) Patología anorrectal inflamatoria o infecciosa, con posterior extensión del proceso desde la región perianal hacia el periné y el escroto. 3) Traumatismo o lesión de la piel perineogenital y penetración directa de los microorganismos de la zona en el tejido subcutáneo5,10,17,19,23. La patología uretral, fundamentalmente la estenosis, constituye el factor precipitante más habitual en la mayoría de las series revisadas. Un posible mecanismo patogénico, que explica el desarrollo de una gangrena de Fournier a partir de una estenosis de uretra, es el siguiente: la estenosis uretral origina una dilatación preestenótica, y un incremento de la presión intrauretral cuando se realiza la contracción vesical, durante la micción. En un determinado momento, dada la fragilidad de la uretra a este nivel, se produce una pequeña disrupción de la pared uretral, que origina extravasación de orina, infectada o no, que puede ocasionar una infección de las glándulas periuretrales11,22. Algunos autores coinciden en afirmar, que aquellos pacientes con gangrena de Fournier de etiología idiopática, tienen un trastorno genitourinario subyacente no diagnosticado. En este grupo de pacientes, el mecanismo patogénico anteriormente mencionado, podría servir para explicar el proceso. Es por ello, que estos autores opinan, que todos los pacientes en los que no se identifica el foco infeccioso, deben ser sometidos a evaluación del tracto urinario inferior9,11,12,22,23. Una vez establecida la infección en las glándulas periuretrales, ésta se extiende hacia el cuerpo esponjoso, atravesando la túnica albugínea y alcanzando la fascia de Buck. Si la fascia de Buck resulta dañada, el proceso infeccioso se disemina a través de la fascia del dartos, comprometiendo la totalidad del pene y el escroto. Posteriormente la infección puede propagarse desde la fascia dartos hacia la fascia de Colles, afectando por consiguiente a la región perineal, o hacia la fascia de Scarpa, en cuyo caso el proceso se extenderá hacia la pared abdominal anterior. Esta propagación característica se lleva a cabo por la existencia de una relación de contigüidad entre la fascia dartos y las fascias de Colles y Scarpa12,13,17,19,23. Desde la fascia de Colles, el proceso puede extenderse a la fosa isquiorrectal, alcanzando entonces el espacio retroperitoneal y pararrectal. Este hecho es muy infrecuente, pero de extraordinaria gravedad10,11,22. El margen anal suele estar respetado en los pacientes con foco infeccioso genitourinario. Este dato anatómico puede ser útil para diferenciar estos pacientes de aquellos con una gangrena de origen anorrectal, ya que en estos últimos, el margen anal está afectado3,12,13,43.
- 7. Los testículos y los cuerpos cavernosos no suelen estar involucrados en el proceso necrótico, debido a su vascularización independiente24, salvo en casos de gangrena de Fournier muy evolucionados, o cuando el foco infeccioso se sitúa específicamente en una de esas localizaciones: orquitis, epididimitis, absceso escrotal, implantación de prótesis intracavernosa para disfunción eréctil18. Los factores precipitantes de origen genitourinario más frecuentemente implicados en el desarrollo de una gangrena de Fournier son la estenosis uretral3,5,9,11,12,22 y la colocación, traumática o no, de catéteres uretrales3,5,11,12,22,23. Otros trastornos urogenitales también se han relacionado con la etiología del proceso: cálculos uretrales3,12, masaje prostático3, parafimosis22, orquitis y epididimitis10,11,22 y carcinoma vesical5,11,22, son algunos de ellos. En los procesos gangrenosos de origen perianal, la propagación de la infección se produce tras una ruptura inicial del músculo esfinteriano, a continuación se propaga a través del periné, disecando la fascia de Colles, y extendiéndose anteriormente hacia escroto y pene, siguiendo la fascia del dartos, y hacia el abdomen anterior, por la fascia de Scarpa, que está conectada directamente con la de Colles3,13,22. El mecanismo de progresión de las infecciones de origen colorrectal no está del todo claro. Se ha demostrado que existen soluciones de continuidad a nivel del diafragma urogenital, que permitirían el avance del proceso infeccioso hacia el área perineogenital19. Los focos anorrectales descritos en la literatura son numerosos, siendo los más frecuentes los abscesos perianales, isquiorrectales e interesfinterianos3,5,11,19,40. Se han comunicado casos asociados a otras patologías diversas como: adenocarcinoma rectal3,19,22, adenocarcinoma de sigma3,15, diverticulitis colónica3,19,22, fístula anal, fisura anal11, biopsia de mucosa rectal, dilatación anal, apendicitis3,43, y traumatismo anorrectal35, entre otros. La gangrena de Fournier se ha descrito en relación con factores precipitantes de origen dérmico, como hidrosadenitis perineal, quiste sebáceo infectado3,5, lesiones de la piel del área genital durante el coito11,22, traumatismos cutáneos de origen térmico y mecánico5,11,22, erosión peneana por dispositivos de anillo para disfunción eréctil3,25, dispositivos de vacío para tratamiento de disfunción eréctil27. No obstante, la gangrena de Fournier con foco infeccioso cutáneo, está asociada fundamentalmente a procedimientos quirúrgicos como: vasectomía3,11,17,22,38, circuncisión3,11,17,22,38, hidrocelectomía5,11,22, orquidectomía11,17,22, hemorroidectomía5,11,22, herniorrafia22, biopsia prostática3,11,17,22, colocación de prótesis intracavernosa para disfunción eréctil3,18. Se ha descrito igualmente, asociada a inyección de heroína en vasos femorales28. ANATOMÍA PATOLÓGICAY BACTERIOLOGÍA El estudio anátomo-patológico del tejido resecado en el desbridamiento, muestra una combinación de áreas de inflamación aguda, inflamación crónica, necrosis de piel y tejido celular subcutáneo, y trombosis vascular subcutánea masiva3,5,13,22.
- 8. El cultivo del material necrótico, pone de manifiesto que la gangrena de Fournier es usualmente una infección polimicrobiana, aislándose una media de 4 microorganismos en la mayoría de los trabajos revisados. Aerobios y anaerobios se encuentran casi siempre presentes, de manera combinada, en los cultivos bacterianos de la lesión3-5,9,44. Los gérmenes anaerobios son identificados con menos frecuencia en los cultivos que los aerobios. No obstante, el mal olor característico, desprendido por las heridas de los pacientes con gangrena de Fournier, es casi patognomónico de infección por anaerobios3,11. Los microorganismos más frecuentemente aislados en los cultivos bacteriológicos de la gangrena de Fournier, son los bacilos entéricos Gram-negativos, y entre ellos destaca la Escherichia coli. Le siguen en frecuencia las diversas especies de Bacteroides y los cocos Gram-positivos, especialmente Streptococcus. Otros gérmenes usualmente implicados son los Staphilococcus y Peptostreptococcus. Es importante señalar que todos estos gérmenes forman parte de la flora bacteriana normal del aparato gastrointestinal distal y del periné3- 5,8,10,11. Proteus mirabilis,Klebsiella pneumoniae, Pseudomona aeruginosa y Fusobacterium, entre otros, son microorganismos que también se han aislado en estos pacientes, aunque su frecuencia de presentación es mucho menor4,5,9,11,22. El Clostridium, a pesar de hallarse clásicamente involucrado en la etiología de la fascitis necrotizante, se identifica con poca frecuencia en los cultivos de los pacientes con gangrena de Fournier, en las series revisadas. Las diferentes especies de Staphilococcus, son las que más usualmente se identifican en cultivo, cuando la gangrena de Fournier se produce por una lesión dérmica5,7,19. La existencia de infección polimicrobiana sugiere la importancia de una acción sinérgica de los diferentes microorganismos implicados, combinándose los mecanismos patogénicos de las distintas especies bacterianas4,6,9,10,19,39. Los mecanismos que conducen a las alteraciones histopatológicas de la gangrena de Fournier son poco conocidos, ya que a partir de gérmenes relativamente poco virulentos per se, como son los que habitualmente residen en el periné, uretra y tracto gastrointestinal bajo, se producen infecciones de gran agresividad. La progresión de la lesión se produciría por la acción sinérgica de las diferentes propiedades de las bacterias infectantes: a) Crecimiento de anaerobios sobre un tejido con poca tensión de oxígeno, tras la necrosis cutáneo- subcutánea, producida por endarteritis obliterante y trombosis de los pequeños vasos del tejido celular subcutáneo3,5,10,13. b) Efecto de los enzimas liberados por las diferentes bacterias que desencadenan una serie de alteraciones fisiopatológicas y lesionan estructuras celulares básicas, dando lugar a destrucción celular y necrosis hística. La estreptoquinasa, una fibrinolisina producida por algunos Streptococcus del grupo A, digiere la fibrina y otras proteínas celulares. La estreptodornasa, otro enzima sintetizado por el Streptococcus, da lugar a despolimerización del DNA. La hialuronidasa, generada por
- 9. diversas especies de Staphilococcus, Streptococcus y Bacteroides da lugar a una lisis del ácido hialurónico, que es un componente fundamental del tejido conjuntivo. El Bacteroides sintetiza igualmente colagenasa, una proteasa, que al destruir el colágeno, ocasiona un daño importante en la matriz extracelular3,5,9,10,13,22. La DNAasa es una proteasa producida principalmente por especies de Bacteroides, que ocasiona una desnaturalización del DNA, que a la postre da lugar a la destrucción celular. La coagulasa, producida por Streptococcus Betahemolítico y Staphilococcus, es una proteína con actividad procoagulante, que además tiene la propiedad de depositar fibrina sobre la superficie de las bacterias que la sintetizan, dificultando de este modo su fagocitosis por las células del sistema inmune. El enzima procoagulante heparinasa es liberado por diversos tipos de anaerobios, especialmente Bacteroides. La mayoría de los microorganismos aerobios sintetizan sustancias que favorecen la agregación plaquetaria y la fijación del complemento. Estas últimas sustancias, junto con la coagulasa y la heparinasa, pueden originar una coagulación intravascular, dando lugar a una trombosis vascular, que a su vez genera una situación de isquemia tisular y posterior necrosis y gangrena5,9,10,13,22. Los bacilos entéricos Gram-negativos, poseen una endotoxina de naturaleza lipopolisacárida (LPS), ligada a su membrana externa, que es responsable de la situación de colapso cardiovascular característico de la sepsis por Gram-negativos. Esta endotoxina también ha sido implicada en la destrucción tisular, ocasionada por la trombosis vascular y necrosis secundaria a la misma5,9,21. EXPLORACIONES DIAGNÓSTICAS COMPLEMENTARIAS El diagnóstico de la gangrena de Fournier es básicamente clínico. Los síntomas y signos de la enfermedad, la exploración física característica, y en ocasiones, la presencia de un factor predisponente, suelen ser suficientes para efectuar el diagnóstico del proceso3,13. En los casos más dudosos, y fundamentalmente en fases precoces del proceso, puede ser beneficioso la realización de una técnica de diagnóstico por imagen. La radiografía simple de abdomen puede poner de manifiesto la presencia de gas en el tejido subcutáneo, cuando este gas aún no es suficiente para producir la característica crepitación a la palpación3,22,30. Este dato no es patognomónico, pero sí altamente sugestivo de gangrena de Fournier, si la clínica acompañante es compatible con dicho proceso3,30. La ecografía escrotal puede ser útil, si existe duda en el diagnóstico diferencial con procesos inflamatorios intraescrotales, como orquitis o epididimitis, especialmente en la fase inicial, prenecrótica, de la gangrena de Fournier, en la que los síntomas y signos son similares. La evaluación ecográfica puede revelar la presencia de un engrosamiento de la pared escrotal; la existencia de gas subcutáneo, extendiéndose en dirección posterior, hacia el periné; y un contenido escrotal sin alteraciones ecográficas en la mayoría de los casos3,4,13,22,31. No obstante, existe un porcentaje no desdeñable de pacientes con gangrena
- 10. de Fournier (10-21%), que presentan afectación testicular3,5,9,10,14,22, en estos casos la ecografía daría un resultado falsamente negativo. La RM también ha sido utilizada en el diagnóstico de gangrena de Fournier3,13,32. Los hallazgos característicos de esta técnica son, al igual que con la ecografía, engrosamiento de la pared del escroto, presencia de gas en el tejido subcutáneo, y normalidad de testículos y epidídimos. La ventaja de la RM es que permite cuantificar, de manera más precisa la extensión de la lesión, por lo que puede ser usada en pacientes con lesiones avanzadas, para planificar los límites del desbridamiento. El TAC desempeña una función similar a la RM, como técnica de apoyo diagnóstico, en la gangrena de Fournier. Ambas técnicas de imagen también pueden ser utilizadas para efectuar el diagnóstico etiológico, en aquellos pacientes con procesos infecciosos de origen intraabdominal o retroperitoneal3,13,43. La uretrocistografía retrógrada y la anorrectoscopia pueden ser útiles a la hora de identificar el foco infeccioso, y con el fin de planificar una eventual derivación urinaria o intestinal4,11,12,14,22. GANGRENA DE FOURNIER EN LA INFANCIA La gangrena de Fournier infantil muestra importantes diferencias con respecto a la gangrena del adulto20,35,37,38 : a) Desde el punto de vista microbiológico, el Streptococcus y el Staphilococcus son los gérmenes identificados con más frecuencia, aislándose los mismos en más del 60% de los casos de gangrena de Fournier infantil. b) En cuanto al factor precipitante, también existen diferencias notables, ya que en la edad pediátrica, los focos infecciosos que más habitualmente dan lugar a este proceso necrótico son: traumatismos cutáneos, picadura de insectos, circuncisión, lesiones térmicas, enfermedad periuretral, trastornos anorrectales e infección sistémica. c) La presentación clínica también es diferente, ya que la afectación del estado general es menor en la infancia, encontrándose con cierta frecuencia una necrosis cutánea extensa con poca o nula repercusión clínica. d) Con respecto al tratamiento, un desbridamiento quirúrgico más conservador puede ser suficiente para lograr la curación, recomendando la mayoría de los autores resecar inicialmente sólo la piel claramente necrótica, practicando incisiones y drenajes, en aquellas áreas de celulitis periféricas a la lesión necrótica. e) Por último, el pronóstico de la gangrena de Fournier es sustancialmente mejor en los niños que en los adultos, presentando en la infancia una tasa media de mortalidad del 9% en las series posteriores a 1950. TRATAMIENTO
- 11. El tratamiento de la gangrena de Fournier se basa en dos pilares fundamentales: el tratamiento farmacológico agresivo, mediante antibióticos, y el desbridamiento quirúrgico amplio e inmediato de la lesión necrótica3,5,6,9-11,22. El tratamiento farmacológico debe realizarse de manera empírica mediante la combinación de tres antibióticos de amplio espectro, a dosis máximas y por vía parenteral, para proporcionar cobertura a cocos Gram-positivos, bacilos Gram-negativos y anaerobios, ya que éstos son los microorganismos potencialmente implicados en el proceso3,9,14,22. Un régimen antibiótico empíricamente efectivo sería: penicilina o ampicilina + aminoglucósido +clindamicina o metronidazol. Actualmente, y dada la efectividad de las cefalosporinas de tercera generación frente a los gérmenes Gram-negati vos, parece razonable la administración de un antibiótico de esta familia: ceftriaxona o ceftazidima, en lugar de un aminoglucósido3,9,13,14,22. El desbridamiento quirúrgico inmediato de la lesión necrótica, es una medida terapéutica imprescindible, en la que coinciden todos los autores consultados (Fig. 2). El desbridamiento quirúrgico debe llevarse a cabo en quirófano, bajo anestesia general, con el paciente en posición de litotomía dorsal, para lograr un mejor acceso y visualización del periné y la región perianal3,4,22. FIGURA 2. Tratamiento quirúrgico: amplio desbridamiento de la lesión necrótica y de aquellas áreas de viabilidad dudosa. La mayoría de los autores abogan por un desbridamiento amplio inicial, efectuando una resección de todo el área necrótica, y de todas aquellas zonas con viabilidad dudosa, incluyendo aquellas zonas sin necrosis evidente, pero que presentan celulitis o crepitación a la palpación3-5,22. En las zonas afectadas, la piel y el tejido subcutáneo se separan fácilmente de la fascia y el músculo subyacentes, por lo que se ha recomendado establecer como límite de la resección aquel punto en que esos dos planos no se separan con facilidad3,11,22. Se debe resecar toda
- 12. la piel y el tejido subcutáneo, hasta el plano fascial, que debe ser respetado ya que habitualmente no existe compromiso del mismo3,11,22. Otros autores optan por una actitud quirúrgica más conservadora, efectuando inicialmente desbridamiento sólo de aquellas áreas claramente necróticas, para realizar desbridamientos sucesivos a medida que se extiende la necrosis y se delimitan con claridad los tejidos sanos y los dañados9,11,22. Cualquiera de las dos actitudes quirúrgicas puede ser correcta, y existen trabajos que no encuentran diferencias entre las tasas de mortalidad de los pacientes tratados con ambas técnicas22. Tras el desbridamiento quirúrgico inicial es necesaria una revisión de la herida cada 12 ó 24 horas, con el fin de valorar la necesidad de una ampliación del margen de desbridamiento, por la aparición de nuevas zonas de necrosis3-5,9,11. En la mayoría de los casos el primer desbridamiento no es definitivo, siendo necesarios 3 ó 4 desbridamientos sucesivos posteriores, por término medio, para lograr la eliminación total del tejido necrótico3,5,8,10. Se deduce claramente a la luz de las series revisadas, que en la actualidad debe proscribirse el tratamiento mediante incisiones y drenajes múltiples, sin desbridamiento, ya que de este modo no se elimina el tejido gangrenoso, perpetuándose la infección. Algunos autores encuentran hasta un 100% de mortalidad cuando ésta es la única actitud quirúrgica llevada a cabo15,22. La vascularización arterial del testículo corre a cargo de la arteria espermática, la arteria deferencial y la arteria funicular 42. Este aporte sanguíneo diversificado, diferente del pene y escroto, permite preservar los testículos, en los pacientes con gangrena de Fournier 3,4,11,22. En realidad, la orquidectomía es necesaria en el 10-32% de los casos, realizándose en la mayoría de las ocasiones por una orquiepididimitis difusa o un absceso escrotal, y en pocos casos por lesión isquémica testicular3,5,9,10,14,22. Debido al amplio desbridamiento realizado en algunos casos, en los que se efectúa una resección de la totalidad del escroto, los testículos quedan completamente expuestos. En estos casos es posible crear una bolsa subcutánea en la cara interna del muslo o en la porción inferior de la pared abdominal, llevando a cabo una posterior implantación de los testículos en la misma, con el fin de protegerlos. Esta implantación habitualmente tiene un carácter transitorio, aunque en ocasiones se convierte en la ubicación definitiva de los testículos, cuando no es posible realizar ningún otro procedimiento plástico reconstructivo3,5,9,11,14,22. Se aconseja la realización de una derivación urinaria suprapúbica en aquellos pacientes con estenosis uretrales, con extravasación urinaria periu retral demostrada en la uretrografía, con flemón y/o absceso periuretral, y en general en todos aquellos pacientes que presentan un trastorno uretral, conocido o sospechado, como factor precipitante de la gangrena de Fournier, con el fin de evitar un cateterismo vesical retrógrado3,5,9,11,14,22.
- 13. En general, la mayoría de los autores recomiendan la realización de una colostomía, en aquellos pacientes con un foco infeccioso de origen anorrectal, en los que existe una afectación extensa del esfínter anal, o una perforación rectal o colónica. Por otra parte, también se puede indicar una colostomía con el propósito de evitar una contaminación del área desbridada, con material fecal3-5,10,22,43. Resulta beneficiosa la irrigación post- operatoria de la herida quirúrgica mediante peróxido de hidrógeno, que es una fuente de oxígeno, y permite la destrucción de microorganismos anaerobios5,8,10,22. También ha mostrado utilidad el uso tópico de algunos agentes antisépticos, como povidona yodada o hipoclorito sódico (solución de Dakin)3,11,22. La aplicación local de colagenasa liofilizada, un enzima que digiere los restos necróticos del tejido, ha sido utilizada por algunos autores como tratamiento adyuvante a la cirugía, obteniendo buenos resultados, con un acortamiento de la estancia hospitalaria y una disminución del número de desbridamientos quirúrgicos necesarios por paciente5. Han sido numerosos los trabajos publicados que elogian los efectos beneficiosos de la aplicación tópica de miel no elaborada, directamente sobre la herida quirúrgica, una vez efectuado el desbridamiento inicial3,5,8,10. Las sustancias contenidas en la miel desarrollan un efecto curativo actuando a varios niveles: 1) Desbridamiento de la herida, por su contenido en enzimas que digieren los restos tisulares necróticos, y estimulan la granulación del lecho de la herida. 2) Actividad antibacteriana, por su alto contenido en agentes antimicrobianos. 3) Producción de oxígeno a nivel local, con lo cual se facilita la erradicación de gérmenes anaerobios, y por otra parte se estimula el crecimiento celular epitelial, ejerciendo una actividad regenerativa tisular. En ocasiones la regeneración de la piel escrotal, facilitada por la aplicación tópica de miel es tan intensa, que los bordes de la herida están muy próximos entre sí, y posteriormente no es necesario efectuar ningún procedimiento plástico para cubrir la herida. El tratamiento de la gangrena de Fournier mediante oxígeno hiperbárico debe considerarse siempre como un tratamiento adyuvante de la cirugía, y está indicado fundamentalmente en caso de infecciones por anaerobios, sospechadas por la clínica o demostradas por el análisis microbiológico, y también en aquellos pacientes que continúan con síntomas tóxicos y mal estado general a pesar de recibir un tratamiento adecuado, y haber sido sometidos a un desbridamiento quirúrgico amplio3,22. El oxígeno hiperbárico produce incremento en la presión tisular de oxígeno, activación leucocitaria, reducción del edema por vasoconstricción, estimulación de la angiogénesis, activación de la proliferación de fibroblastos e incremento del transporte intracelular de antibióticos. El papel de este tipo de terapia en la gangrena de Fournier, y los beneficios que se pueden obtener con ella, no están claros3,5,10,22,43, aunque existen algunos estudios que observan una reducción significativa de la morbilidad y la mortalidad, si se utiliza precozmente14,36.
- 14. Una parte fundamental del tratamiento de la gangrena de Fournier son las medidas generales de soporte pre y post-operatorias. Son indispensables una rápida estabilización hemodinámica del paciente, así como una reposición intravenosa adecuada de líquidos, para corregir la hipovolemia secundaria a la hipertermia, y a la pérdida de líquido a través del área desbridada, especialmente si ésta es muy extensa. Es importante efectuar una reposición razonable de todos aquellos déficits ocasionados por la situación de sepsis del paciente: proteínas, plaquetas, factores de la coagulación, concentrados de hematíes, y otros3,22. Aquellos pacientes con cuadros sépticos graves y con pérdida tisular importante, precisan por su estado hipermetabólico, un aporte calórico mayor de lo normal. Cuando las condiciones del paciente no permiten suministrar este aporte energético por vía oral, algunos autores optan por la realización de una hiperalimentación parenteral3,5,9,14. Un estado nutricional adecuado del paciente facilita una rápida cicatrización y curación de la herida3. Una vez que el paciente se ha estabilizado clínicamente, y la herida se encuentra totalmente libre de restos necróticos y con un buen lecho de granulación, debe planearse el método reconstructivo más apropiado para cada caso7,9,22. En aquellos pacientes con pequeñas pérdidas tisulares, la cicatrización retardada suele ser suficiente para cubrir todo el defecto cutáneo3,13,43. La piel escrotal es característicamente redundante y muestra una gran capacidad regenerativa, por lo que en ocasiones se consigue recubrir áreas desbridadas de una extensión sorprendente, mediante cicatrización por segunda intención3,5,9. Cuando el defecto cutáneo es muy extenso, o el proceso de cicatrización se prolonga demasiado en el tiempo, es necesario llevar a cabo algún procedimiento plástico para reparar la herida4,22. Injertos libres de piel, colgajos pediculados, colgajos miocutáneos, y colgajos en mosaico, son las técnicas de reparación plástica más habitualmente usadas3,5,14,22. PRONÓSTICO La tasa de mortalidad de la gangrena de Fournier oscila entre el 0 y el 80%, según la serie analizada5,10,11,14,44. A pesar de la existencia de antibióticos cada vez más efectivos, del importante avance tecnológico en las medidas de soporte del paciente y de la mejor comprensión de los mecanismos etiopatogénicos de la enfermedad, la mortalidad media observada en las series más recientes, es comparable a la de las series antiguas3,11,13. La razón de esta aparente incongruencia se desconoce, una hipótesis podría ser, que la edad progresivamente mayor de los pacientes diagnosticados, eclipse los beneficios potenciales proporcionados por los avances terapéuticos3. Algunos factores, como el número de procedimientos quirúrgicos realizados, la extensión inicial del proceso necrótico, y la coexistencia de diabetes mellitus o alcoholismo, han sido implicados de manera poco concluyente en el pronóstico3,5,6,22. Por el contrario, sí parecen asociarse a una mayor mortalidad, el retraso en el inicio del tratamiento y las infecciones de origen anorrectal4,9,22,43.
- 15. La muerte se produce en la mayoría de los casos, a consecuencia de las complicaciones del proceso séptico, fundamentalmente cardiovasculares, renales, respiratorias y hematológicas, que conducen a una situación de fallo multiorgánico3,5-7. SERIE PERSONAL MATERIAL Y MÉTODO Analizamos un grupo de 7 pacientes varones, vistos y tratados de manera consecutiva en nuestro servicio, entre los años 1991 y 1998, con el diagnóstico de gangrena de Fournier. Los cambios epidemiológicos observados en la gangrena de Fournier en los últimos tiempos, han hecho que de nuestra casuística hospitalaria total, estudiemos solamente los pacientes vistos en los últimos años, con el propósito de evaluar si nuestros resultados eran concordantes con la literatura médica revisada. El diagnóstico de gangrena de Fournier, se efectuó a partir de la historia clínica y la exploración física del paciente. Todos los pacientes fueron tratados de forma empírica, con antibioterapia parenteral de amplio espectro, mediante la combinación de tres fármacos, con actividad frente a Gram- positivos, Gram-negativos y anaerobios. Se modificó el esquema terapéutico antimicrobiano según la evolución clínica o el análisis bacteriológico. Se practicó desbridamiento quirúrgico inmediato, en quirófano, bajo anestesia general, en todos los pacientes, efectuando una resección amplia y agresiva de todo el tejido gangrenoso, y de aquellas áreas con viabilidad dudosa. Se realizó drenaje suprapúbico de orina en todos aquellos pacientes que presentaban patología uretral asociada. Se efectuó revisión de la herida quirúrgica cada 24 horas, para valorar la necesidad de practicar oportunamente resecciones secundarias de tejido no viable. Asimismo, se hicieron curas locales de la herida a intervalos de 12 horas, utilizando peróxido de hidrógeno. Las áreas denudadas fueron cubiertas por cicatrización retardada o mediante procedimientos plásticos reconstructivos, según el paciente. Las variables estudiadas en cada uno de los pacientes fueron las siguientes: edad, tiempo transcurrido desde el inicio de los síntomas hasta el diagnóstico del proceso, síntomas y signos físicos del paciente en el momento del diagnóstico, datos analíticos hematológicos y bioquímicos, resultado de los hemocultivos y urocultivos, antecedentes personales y trastornos relacionados con la gangrena de Fournier. También se analizaron aquellos factores potencialmente precipitantes de la gangrena de Fournier, localización anatómica del área necrótica, estudio anatomo-patológico del tejido
- 16. desbridado, flora microbiana aislada en el cultivo del tejido necrótico, tratamiento realizado en cada paciente, estancia hospitalaria, morbilidad asociada al proceso y supervivencia. RESULTADOS La edad media de los pacientes era de 62 años (rango 50-75). El intervalo medio de tiempo transcurrido desde el inicio de los síntomas específicos del proceso, hasta la solicitud de atención médica fue de 84 horas (rango 36-144). Las manifestaciones clínicas observadas y su frecuencia de presentación fueron las siguientes: dolor (100%), fiebre (57%), hipotensión y estado de shock (29%), incremento del tamaño escrotal (100%), mal olor (100%), necrosis cutánea (100%), edema y eritema cutáneos (71%), crepitación cutánea (43%), exudación (29%). Entre los hallazgos analíticos, la leucocitosis con desviación izquierda fue una constante en todos los pacientes estudiados (100%). Se encontraron alteraciones en las pruebas de coagulación en 3 pacientes (43%). El hemocultivo demostró crecimiento bacteriano sólo en 2 pacientes, Staphilococco aureus en uno de ellos y Streptococco faecalis en el otro. El urocultivo fue positivo en dos casos. En uno de los pacientes creció Staphilococco aureus y Enterococo, mientras que en el otro se observó positividad para Escherichia coli y Enterococo. Los dos pacientes con urocultivo positivo, presentaban un foco urinario como factor precipitante de la gangrena de Fournier. En 5 de los 7 pacientes (71%) se encontraron entre sus antecedentes personales, patologías clásicamente asociadas a la gangrena de Fournier. Se identificó alcoholismo crónico y hepatopatía en 4 pacientes (57%), diabetes mellitus no insulinodependiente en 4 (57%). Alcoholismo y diabetes se encontraron asociados en 3 pacientes (43%). Un paciente (14%) presentaba como teórico factor predisponente, un adenocarcinoma prostático metastásico. El factor potencialmente precipitante del proceso fue identificado en 6 pacientes (86%), existiendo en 5 de ellos (71%) un foco genitourinario: 2 estenosis de uretra, 1 orquiepididimitis, 1 parafimosis, y 1 cateterismo uretral, para realización de uretrocistografía retrógrada, en un paciente con estenosis de uretra. En 1 paciente se detectó un foco infeccioso anorrectal, siendo éste un absceso perianal. En lo que respecta a la extensión anatómica de la lesión necrótica, observada en el momento del desbridamiento inicial, los 7 pacientes (100%) presentaban afectación escrotal de mayor o menor cuantía, hallándose limitada al escroto en 3 de ellos. Un paciente presentaba afectación de escroto y periné, en 2 pacientes el área de necrosis comprometía
- 17. escroto, periné y raíz peneana, mientras que en el paciente restante, la lesión se extendía por escroto, periné, hipogastrio, región inguinal bilateral y cara interna de ambos muslos. El examen histopatológico de la lesión reveló áreas de edema, inflamación aguda, necrosis de piel y tejido celular subcutáneo, y trombosis vascular subcutánea. En todos los pacientes se obtuvo un crecimiento polimicrobiano, en los cultivos del material necrótico resecado. Se aislaron 4 microorganismos en 1 paciente, 3 gérmenes en 5 de los pacientes, y 2 gérmenes en 1 paciente. Los gérmenes más frecuentemente aislados en el cultivo del material necrótico fueron Escherichia coli en 5 pacientes (71%), Streptococco faecalis en 4 pacientes (57%). Streptococco betahemolítico, Staphilococco aureus, Bacteroides fragilis y Peptostreptococco, fueron aislados, cada uno de ellos, en el 29% de los casos. Por último, Staphilococco coagulasa negativo, Staphilococco intermedius, Bacteroides stercoris yFusobacterium, fueron identificados en una sola ocasión (14%) (Tabla I). TABLA I DISTRIBUCIÓN DE BACTERIAS AISLADAS Y PORCENTAJE DE PACIENTES AFECTADOS En todos los pacientes se llevó a cabo tratamiento quirúrgico urgente, consistente en desbridamiento amplio y agresivo, con excisión de todo el área necrótica, y un margen de piel indemne, alrededor de la misma. Se practicaron desbridamientos posteriores, conforme se extendía la lesión gangrenosa, en 4 pacientes (57%). En 1 paciente se practicó un solo desbridamiento secundario, en 2 casos fueron necesarios 2 nuevos desbridamientos, y en 1 paciente se realizaron 5 desbridamientos. Un paciente fue sometido a tratamiento adyuvante con oxígeno hiperbárico, 48 horas después del tratamiento quirúrgico. Se practicó orquidectomía en un paciente con una orquiepididimitis subyacente. Se colocó un catéter de derivación urinaria suprapúbica en 3
- 18. pacientes (43%), que fueron aquellos que presentaban patología uretral, como factor precipitante de la gangrena de Fournier. La estancia hospitalaria media, hasta la curación del episodio de gangrena de Fournier, fue de 28 días (rango 9-52). La tasa de mortalidad en los pacientes de nuestra serie fue del 29% (2 de 7 pacientes). Las 2 muertes se produjeron por shock séptico, con desarrollo de distress respiratorio e insuficiencia renal aguda. Los 2 pacientes fallecidos ya presentaban una coagulopatía de consumo severa, en el momento del diagnóstico. En 4 de los 5 pacientes que sobrevivieron al episodio de gangrena de Fournier, la cicatrización por segunda intención fue suficiente para cubrir el defecto cutáneo ocasionado. Solamente en 1 caso la reparación del área de resección cutánea, se efectuó mediante un injerto libre de piel de la cara interna del muslo. COMENTARIOS SOBRE NUESTRA CASUÍSTICA En nuestra serie personal hemos encontrado una gran concordancia con los datos etiopatogénicos, clínicos, bacteriológicos y terapéuticos, de los trabajos revisados. La edad media de presentación fue, en nuestro caso, de 62 años. El 71% de los pacientes de nuestra serie presentaba algún factor de riesgo asociado, fundamentalmente diabetes mellitus y alcoholismo crónico. La mayoría de nuestros pacientes presentaba un foco genitourinario, como factor precipitante de la gangrena de Fournier, siendo la estenosis de uretra, la patología más frecuente en este grupo etiológico (43%). Todos nuestros pacientes presentaban una infección polimicrobiana mixta, aeróbica y anaeróbica, aislándose una media de 3 gérmenes por paciente. La Escherichia coli fue el microorganismo cultivado en más ocasiones (71%), le siguió en frecuencia el Streptococcus faecalis (57%). El tratamiento llevado a cabo en todos los casos consistió en: antibioterapia intravenosa de amplio espectro, desbridamiento quirúrgico radical, curas con peróxido de hidrógeno, revisión de la herida cada 24 horas, con desbridamientos secundarios en el 57% de los casos, por progresión de la lesión necrótica. El cierre del defecto cutáneo se efectuó mediante cicatrización por segunda intención, en la mayoría de los pacientes, tan sólo un paciente precisó reparación plástica, utilizando un injerto de piel de la cara interna del muslo. La estancia hospitalaria media en nuestra serie, fue de 28 días, y la tasa de mortalidad del 29%. CONCLUSIONES De este estudio se pueden extraer las siguientes conclusiones:
- 19. 1. La gangrena de Fournier es un proceso infeccioso necrotizante perineogenital, habitualmente polimicrobiano, originado por microorganismos aeróbicos y anaeróbicos. 2. El proceso necrótico afecta a varones en la sexta y séptima década de la vida, identificándose en la mayoría de ellos un factor precipitante subyacente de origen genitourinario, anorrectal o dérmico. La diabetes mellitus, el alcoholismo crónico, las neoplasias malignas, y otros estados de inmunodepresión del huésped, predisponen a padecer una gangrena de Fournier. 3. El desbridamiento quirúrgico inmediato y agresivo del área necrótica, es imprescindible para lograr la curación de la gangrena de Fournier. La cirugía debe acompañarse de tratamiento antibiótico intravenoso de amplio espectro, así como de las medidas de soporte adecuadas, que varían en función del estado y las complicaciones particulares de cada paciente. Existen una serie de tratamientos adyuvantes a la cirugía, como la administración de oxígeno hiperbárico y la aplicación tópica de miel sin elaborar, que han sido utilizados con el fin de disminuir la morbilidad y la mortalidad del proceso, obteniendo buenos resultados, en líneas generales. 4. La tasa de mortalidad de la gangrena de Fournier sigue siendo elevada, y similar a la registrada en las series más antiguas.
