Problema de reactivo limitante na y s
•Descargar como PPTX, PDF•
0 recomendaciones•3,314 vistas
Reacción del sodio con el azufre con reactivo limitante.
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Polaridad del enlace y porcentaje del carácter iónico

Polaridad del enlace y porcentaje del carácter iónico
Destacado
Destacado (20)
Problema de propiedad coligativa presión de vapor de una disolución

Problema de propiedad coligativa presión de vapor de una disolución
Problema de propiedad coligativa presión de vapor de una disolución

Problema de propiedad coligativa presión de vapor de una disolución
Problema de p h de una disolución de ácido benzoico y neutralización con hidr...

Problema de p h de una disolución de ácido benzoico y neutralización con hidr...
P h de una disolución de una base débil (amoníaco)

P h de una disolución de una base débil (amoníaco)
Problema de propiedad coligativa temperatura congelación de una disolución

Problema de propiedad coligativa temperatura congelación de una disolución
Química orgánica nomenclatura de un ácido carboxílico

Química orgánica nomenclatura de un ácido carboxílico
Similar a Problema de reactivo limitante na y s
Similar a Problema de reactivo limitante na y s (20)
Más de Diego Martín Núñez
Más de Diego Martín Núñez (20)
Problema resuelto reactivo limitante nitrato aluminio y sulfuro de h

Problema resuelto reactivo limitante nitrato aluminio y sulfuro de h
Problema resuelto reacción química riqueza y concentración

Problema resuelto reacción química riqueza y concentración
Problema de reacción de disolución de h cl con mármol

Problema de reacción de disolución de h cl con mármol
Problema de disolución reguladora amoniaco amónico

Problema de disolución reguladora amoniaco amónico
Problema de disolución reguladora acético acetato sin voz

Problema de disolución reguladora acético acetato sin voz
Pregunta curiosa qué ocurriría si una fuerza irresistible actuase sobre cuer...

Pregunta curiosa qué ocurriría si una fuerza irresistible actuase sobre cuer...
Cuando el hielo se derrite aumenta el nivel del agua o no sin voz

Cuando el hielo se derrite aumenta el nivel del agua o no sin voz
Ejercicio de química orgánica adición al doble enlace

Ejercicio de química orgánica adición al doble enlace
Problema de cinemática dos autobuses al encuentro mru

Problema de cinemática dos autobuses al encuentro mru
Último
Último (20)
el CTE 6 DOCENTES 2 2023-2024abcdefghijoklmnñopqrstuvwxyz

el CTE 6 DOCENTES 2 2023-2024abcdefghijoklmnñopqrstuvwxyz
Presentación de Estrategias de Enseñanza-Aprendizaje Virtual.pptx

Presentación de Estrategias de Enseñanza-Aprendizaje Virtual.pptx
Movimientos Precursores de La Independencia en Venezuela

Movimientos Precursores de La Independencia en Venezuela
BROCHURE EXCEL 2024 FII.pdfwrfertetwetewtewtwtwtwtwtwtwtewtewtewtwtwtwtwe

BROCHURE EXCEL 2024 FII.pdfwrfertetwetewtewtwtwtwtwtwtwtewtewtewtwtwtwtwe
5° SEM29 CRONOGRAMA PLANEACIÓN DOCENTE DARUKEL 23-24.pdf

5° SEM29 CRONOGRAMA PLANEACIÓN DOCENTE DARUKEL 23-24.pdf
Estas son las escuelas y colegios que tendrán modalidad no presencial este lu...

Estas son las escuelas y colegios que tendrán modalidad no presencial este lu...
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
Problema de reactivo limitante na y s
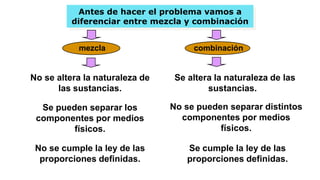
- 1. Antes de hacer el problema vamos a diferenciar entre mezcla y combinación mezcla No se altera la naturaleza de las sustancias. combinación Se altera la naturaleza de las sustancias. Se pueden separar los componentes por medios físicos. No se pueden separar distintos componentes por medios físicos. No se cumple la ley de las proporciones definidas. Se cumple la ley de las proporciones definidas.
- 2. CÁLCULOS CON REACTIVO LIMITANTE. Generalmente es necesario preparar cantidades determinadas de productos a partir de cantidades de reactivos que no son estequiométricamente exactas reactivo limitante se consume completamente reactivo en exceso queda parte sin reaccionar El reactivo limitante reacciona solamente con la cantidad adecuada de la otra sustancia hasta que se acaba, y, de la que se encuentra en exceso, queda parte sin reaccionar.
- 3. CÁLCULOS CON REACTIVO LIMITANTE. Hacemos reaccionan 4,6 g de Na (23 u) con 4 g de S (32 u) para formar Na2S. ¿Cuál es el reactivo limitante y cuál el excedente? 2 Na + S Na2S 1 mol de S2 mol de Na 32 g de S2·23 = 46 g de Na m g de S4,6 g de Na 32 (g de S) 46 (g de Na) = m (g de S) 4,6 (g de Na) 32 · 4,6 46 m = = 3,2 g de S reactivo limitante: reactivo en exceso: Na S Hemos averiguado que con 4,6 g de Na reaccionan 3,2 g de S, pero como de S había 4 g, se deduce: Vamos a calcular la masa de S que reacciona con 4,6 g de Na y el resultado lo comparamos con 4 g.
