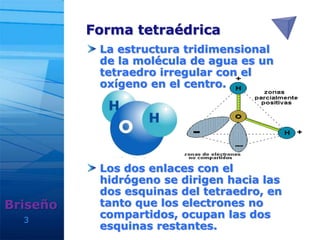
El documento describe las propiedades físico-químicas del agua, incluyendo su estructura tetraédrica, polaridad y capacidad para formar enlaces de hidrógeno. El agua es una molécula polar debido a que el átomo de oxígeno es más electronegativo que el hidrógeno, creando un polo negativo y uno positivo. Las moléculas de agua pueden unirse a través de enlaces de hidrógeno débiles, lo que contribuye a las propiedades del agua líquida y otros compuestos