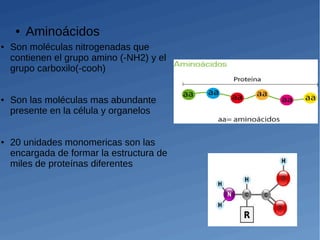
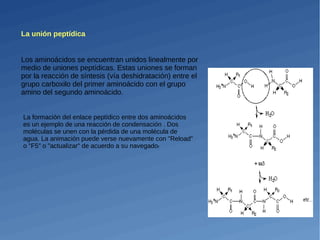
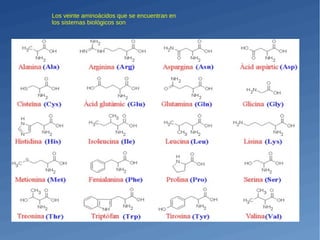
Las proteínas son moléculas complejas compuestas de aminoácidos que desempeñan un papel fundamental en los seres vivos. Se clasifican en tres grupos dependiendo de su estructura y solubilidad: proteínas fibrosas como el colágeno, proteínas globulares como la mioglobina que son solubles en agua, y proteínas de membrana como la rodopsina embebidas en membranas. Los aminoácidos se unen mediante enlaces peptídicos para formar cadenas proteicas diversas.