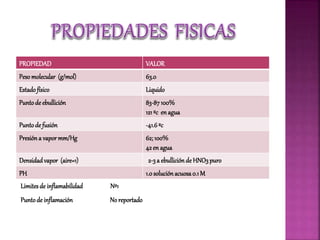
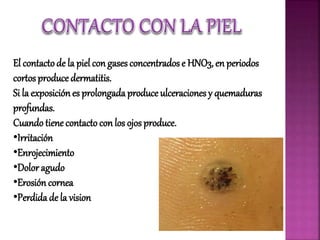
Este documento describe las propiedades y riesgos del ácido nítrico. Es un líquido incoloro y corrosivo que se descompone al calentarse, liberando agua, oxígeno y dióxido de nitrógeno. Al entrar en contacto con la piel o los ojos, puede causar quemaduras graves e incluso ceguera. La inhalación de sus vapores puede provocar irritación respiratoria, tos, dificultad para respirar y edema pulmonar. Es utilizado principalmente en la industria, laboratorios y para fabricar fertil