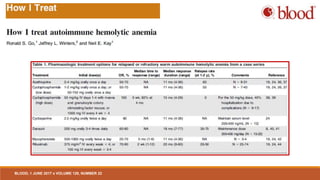
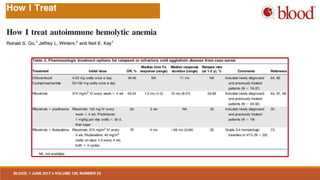
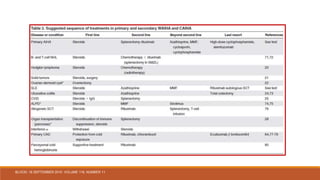
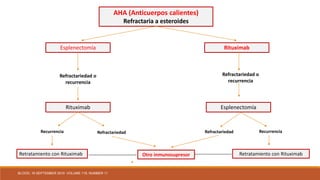
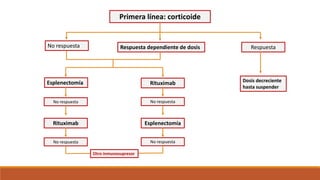
1. Las anemias hemolíticas autoinmunes de anticuerpos calientes primarios responden bien a los esteroides, pero la mayoría de los pacientes siguen siendo dependientes de los esteroides, y muchos requieren tratamiento de segunda línea como la esplenectomía o el rituximab. 2. Las anemias hemolíticas autoinmunes de anticuerpos fríos primarios responden bien al rituximab pero son resistentes a los esteroides y la esplenectomía. 3. El diagnóstico y tratamiento adecuado depende del tipo


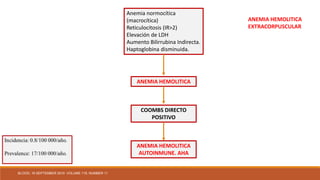






![Dos datos para tomar una decisión de tratamiento adecuada:
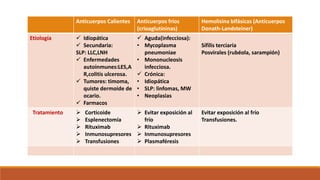
(1) ¿Qué tipo de anticuerpo está involucrado?
(2) ¿La AIHA es primaria o secundaria?
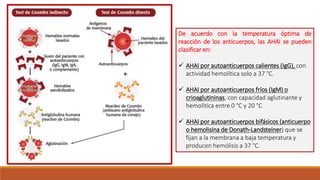
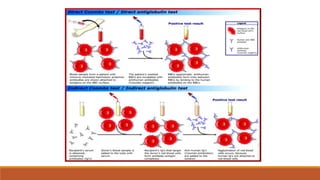
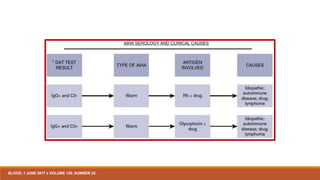
El tipo de anticuerpo se puede identificar con el uso de anticuerpos monoespecíficos para
inmunoglobulina G (IgG) y C3d.
Cuando los glóbulos rojos están recubiertos con IgG o IgG más C3d, el anticuerpo suele ser un
anticuerpo caliente (anticuerpo caliente AIHA [WAIHA]).
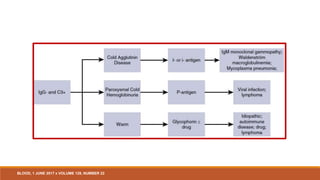
Cuando los glóbulos rojos están recubiertos con C3d solamente, el anticuerpo es a menudo un
anticuerpo frío.
BLOOD, 16 SEPTEMBER 2010 VOLUME 116, NUMBER 11](https://image.slidesharecdn.com/anemiahemoliticaautoinmuneaha-181218031444/85/Anemia-hemolitica-autoinmune-AHA-21-320.jpg)